
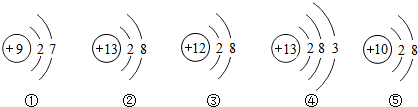
分析 A、根据决定元素种类的是核内质子数,不同种元素最本质的区别是核内质子数不同,进行分析判断.
B、根据原子中,若最外层电子数≥4,则一般为非金属元素,在化学反应中易得电子,若最外层电子数<4,则一般为金属元素,在化学反应中易失去电子.
C、通常认为最外层有8个电子(只有一个电子层的具有2个电子)的结构是一种稳定结构,当质子数>核外电子数,为阳离子;据此进行分析判断.
D、根据质子数和核外电子数的关系解答.
解答 解:A、根据决定元素种类的是核内质子数,不同种元素最本质的区别是核内质子数不同,五种粒子的核内质子数分别是9、13、12、10,表示四种元素,故选项说法正确.
B、④表示的粒子为原子,最外层电子数为3,少于4,为金属元素元素的原子,在化学反应中易失去电子,故选项说法错误.
C、②③⑤的最外层电子数均为8,均是稳定结构,但粒子⑤的质子数=核外电子数=10,为原子,故选项说法错误.
D、②表示的粒子为离子,为铝离子,粒子符号为:Al3+
答案:A; Al3+
点评 本题难度不大,考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的前提.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:初中化学 来源: 题型:解答题
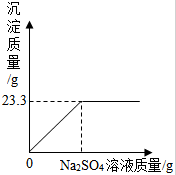 称取NaCl和BaCl2的固体混合物32.5g,加入148.8g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:
称取NaCl和BaCl2的固体混合物32.5g,加入148.8g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
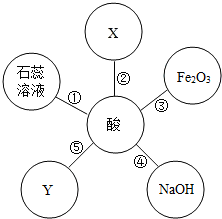 硫酸和盐酸是实验室常用的试剂,也是重要的化工原料,它们既有相似之处,又有不同之点.如下图体现了酸类物质的化学性质,其中X、Y及图中所给其他物质的类别不同.结合此图回答下列问题.
硫酸和盐酸是实验室常用的试剂,也是重要的化工原料,它们既有相似之处,又有不同之点.如下图体现了酸类物质的化学性质,其中X、Y及图中所给其他物质的类别不同.结合此图回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
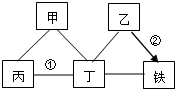 现有铁、碳酸钠、某种红色金属氧化物、稀硫酸和氢氧化钙溶液,它们之间的关系如图所示(“→”表示物质间的转化关系,“-”表示物质间可以相互反应),请回答下列问题:
现有铁、碳酸钠、某种红色金属氧化物、稀硫酸和氢氧化钙溶液,它们之间的关系如图所示(“→”表示物质间的转化关系,“-”表示物质间可以相互反应),请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
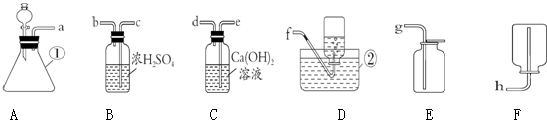
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是实验室所用浓硫酸试剂瓶上标签的部分内容,请仔细阅读后回答下列问题:
如图是实验室所用浓硫酸试剂瓶上标签的部分内容,请仔细阅读后回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
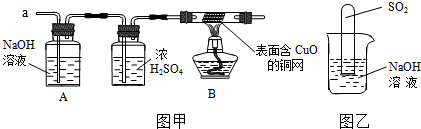
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com