
【题目】在实验室常用以下装置制取气体。
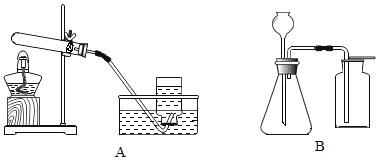
(1)选择装置A用高锰酸钾制取氧气的化学方程式为①_____,试管口放一团棉花的作用是②_____,选择此发生装置的依据③_____。
(2)用装置B制取二氧化碳的化学方程式为①_____,收集气体采用的是②_____法,实验过程中,长颈漏斗末端应位于液面下的目的是③_____。
【答案】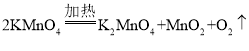 为了防止高锰酸钾粉末进入导管 反应物是固体,需要加热 CaCO3+2HCl=CaCl2+H2O+CO2↑ 向上排空气 防止二氧化碳气体逸出
为了防止高锰酸钾粉末进入导管 反应物是固体,需要加热 CaCO3+2HCl=CaCl2+H2O+CO2↑ 向上排空气 防止二氧化碳气体逸出
【解析】
(1)高锰酸钾在加热的条件下反应,生成锰酸钾、二氧化锰和氧气,反应的化学方程式为: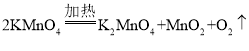 ;试管口放一团棉花的作用是:为了防止高锰酸钾粉末进入导管;选择此发生装置的依据是:反应物是固体,需要加热;
;试管口放一团棉花的作用是:为了防止高锰酸钾粉末进入导管;选择此发生装置的依据是:反应物是固体,需要加热;
(2)碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑。由于二氧化碳的密度比空气的密度大,能溶于水,因此只能用向上排空气法收集。实验过程中,长颈漏斗末端应位于液面下的目的是:防止二氧化碳气体逸出。


科目:初中化学 来源: 题型:
【题目】一定条件下,甲、乙混合后发生化学反应,测得反应前后各物质的质量变化如下表所示。下列说法中,不正确的是( )
物质 | 甲 | 乙 | 丙 | 丁 |
反应前的质量/g | 50 | 2 | 0 | 0 |
反应后的质量/g | 23 | X | 24 | 3 |
A. x的值等于2B. 甲一定是化合物
C. 该反应是化合反应D. 反应时丙和丁的质量比为8:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请完成下列实验,回答问题。
(1)某同学将氢气与空气混合,在安全保障下在老师指导下点燃,实验如下
V(H2)/V(空气) | 1:99 | 3:97 | 4:96 | 50:50 | 70:30 | 75:25 |
点火 | 不炸 | 不炸 | 炸 | 炸 | 炸 | 不炸 |
①该实验说明氢气的爆炸极限范围可能为______~______之间(用百分数表示)
②鉴于该实验爆炸的危险性,说明点燃氢气前必须验纯,验纯的操作为_____
③该实验证明水是由__________________组成的。
(2)除去下列物质中的杂质,所用试剂错误的是___
选项 | 物质 | 杂质 | 除杂试剂 |
A | 铜 | 氧化铜 | 稀硫酸 |
B | 二氧化碳 | 水蒸气 | 生石灰 |
C | 盐酸 | 硫酸 | 氯化钡溶液 |
D | 氯化钡溶 | 氯化钠溶液 | 碳酸钠溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在学习盐酸的化学性质时,甲、乙两位同学分别做了稀盐酸和碳酸钠溶液反应的实验(如图1)。
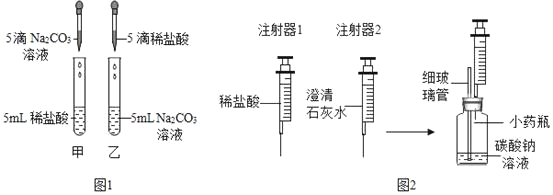
(实验现象)甲同学的实验中溶液有气泡冒出,乙同学的实验中溶液无气泡冒出。
(1)写出甲同学实验的化学反应方程式:_____。
(提出问题)乙同学的实验中溶液为什么没有气泡冒出?
(查阅资料)碳酸钠和稀盐酸反应不仅可以生成二氧化碳还可以生成碳酸氢钠
(实验)同学们设计并进行了如图2所示的实验(装置气密性良好)。
实验编号 | 实验步骤 | 实验现象 |
① | Ⅰ.用注射器1向小药瓶中缓慢注入少量的稀盐酸,边注入边振荡 | 细玻璃管中液柱略微升高 |
Ⅱ.换注射器2从瓶中缓慢抽取气体 | 澄清石灰水无明显变化 | |
② | Ⅰ.用注射器1向小药瓶中继续注入稀盐酸至较多气泡产生 | 细玻璃管中液柱明显升高 |
Ⅱ.换注射器2从瓶中缓慢抽取气体 | 澄清石灰水变浑浊 |
(2)细玻璃管在实验中的主要作用是_____;实验①中细玻璃管中液柱略微升高的原因:少量稀盐酸滴入导致小药瓶内气体体积略微压缩,_____。
(3)实验②中Ⅰ的现象是_____;实验①、②中步骤Ⅱ:注射器2必须缓慢地从瓶中抽取气体的原因是_____。
(实验反思)此反应说明反应物的量不同,产物可能不同,试另举一例:_____。
(若正确回答下列问题加4分,总分不超过60分)
在老师的帮助下,同学们利用pH传感器对相同浓度的碳酸钠溶液(pH为12)、碳酸氢钠溶液(pH为8.2)与稀盐酸反应时,pH的变化与盐酸体积的关系进行了测定,并做了如图3所示的对比图:
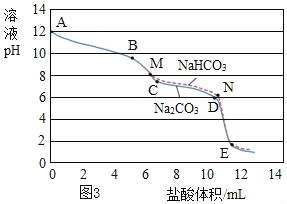
图中各线段实验现象如下表:
溶液 | 线段 | 实验现象 |
Na2CO3 | AB | 无气泡 |
BC | 有少量气泡 | |
CD | 有大量气泡 | |
DE | 几乎无气泡 | |
NaHCO3 | MN | 立即有大量气泡 |
NE | 几乎无气泡 |
(4)在AB段,溶液中的溶质有_____、_____、_____。
(5)分析图表,体现碳酸钠与稀盐酸反应分两步:
第一步反应:Na2CO3 +HCl=NaCl+NaHCO3
第二步反应的化学方程式为:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是以食盐为原料进行生产并综合利用的某些过程
(1)为除去粗盐中的CaCl2、MgCl2和Na2SO4杂质,可对应加入过量的Na2CO3、过量的NaOH以及过量的BaCl2,其中Na2CO3必须在BaCl2之_____(填“前”或“后”)。
(2)将滤液的pH调至中性应加入的试剂是_____。
(3)流程中所得饱和食盐水可用于制取纯碱等产品,其主要反应原理如图:
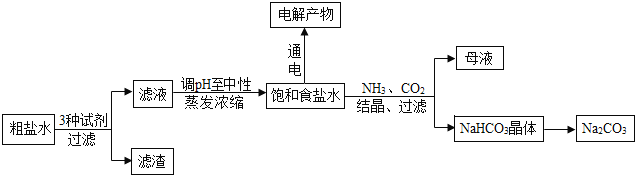
NaCl+H2O+NH3+CO2=NaHCO3↓+NH4Cl 2NaHCO3=Na2CO3+H2O+CO2↑
问:分离出NaHCO3晶体后的母液中一定含有的溶质有_____,若此母液中加入过量生石灰,则可获得一种可循环使用的物质,其化学式是_____。
(4)该流程的主要产品纯碱属于_____(填“酸”或“碱”或“盐”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确的是( )
A. 用木炭还原氧化铜制取铜:CuO+C![]() Cu+CO2 置换反应
Cu+CO2 置换反应
B. 服用含氢氧化铝的药物治疗酸过多症:2Al(OH)3+6HCl=2AlCl3+3H2O 复分解反应
C. 煅烧石灰石制生石灰:CaCO3![]() CaO+CO2↑分解反应
CaO+CO2↑分解反应
D. 用铁丝测定空气中氧气含量:3Fe+2O2![]() Fe3O4化合反应
Fe3O4化合反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分类,类比是初中化学常用的学习方法。
(1)初中化学有许多实验,若按照实验方法分类,可将实验_____(填字母)分为一类;分类的依是_____。
|
|
|
|
A.测定空气中氧气的含量 | B.探究硫在氧气中燃烧 | C.探究反应前后物质的质量关系 | D.探究酸和碱能否发生反应 |
(2)磷酸盐,磷酸氢盐的溶解性和碳酸盐相似,磷酸二氢盐和碳酸氢盐溶解性相似,则磷酸钡的溶解性为_____(填“可溶”或“微溶”或“难溶”),碳酸钙可以和水、二氧化碳(看做碳酸)反应生成碳酸氢钙,请写出向磷酸钙固体中加入磷酸(H3PO4)溶液后,固体消失的反应的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国钢铁产量居世界第一,为国民经济的发展奠定了坚实的基础,生产生活中铁和铁的化合物也有着广泛的应用。
(一)铁的广泛应用
(1)“加铁酱油”中的铁指的是_____(填“单质”或“元素”)。
(2)铁制炊具加热食物,说明铁具有的性质是_____。
(3)铁与铬、镍等金属熔合可形成“不锈钢”,用不锈钢丝和聚乙烯纤维为原料可制作耐酸防护服材料。以上叙述中没有涉及到_____(填字母)。
A 合金 B 无机非金属材料 C 合成材料 D 复合材料
(二)铁锈成分的探究
(1)下图为某兴趣小组探究铁生锈的三个实验,最先观察到铁锈的是_____(选填序号)。
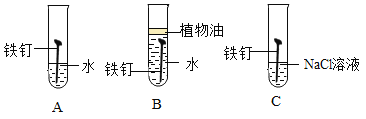
(2)铁生锈的主要过程为:Fe![]() Fe(OH)2
Fe(OH)2![]() Fe(OH)3
Fe(OH)3![]() Fe2O3xH2O
Fe2O3xH2O
次要过程为:Fe![]() FeCO3
FeCO3
写出Fe→Fe(OH)2反应的化学方程式_____。
(3)铁锈组分的确定
某铁锈成分为Fe2O3xH2O和FeCO3.为确定其组成,兴趣小组称取此铁锈样品25.4g,在科研人员的指导下用下图装置进行实验。

(查阅资料)①Fe2O3xH2O失去结晶水温度为110℃,FeCO3在282℃分解为FeO和CO2
②温度高于500℃时铁的氧化物才能被CO还原。
(1)装配好实验装置后,首先要_____。
(2)装置A中的反应为:H2C2O4(草酸)![]() CO↑+CO2↑+H2O通过B、C装置可得到干燥、纯净的CO气体,洗气瓶B中应盛放_____(选填序号)。
CO↑+CO2↑+H2O通过B、C装置可得到干燥、纯净的CO气体,洗气瓶B中应盛放_____(选填序号)。
a.浓硫酸 b.氢氧化钠溶液
(3)现控制D装置中的温度为300℃对铁锈进行热分解,直至D装置中剩余固体质量不再变化为止,冷却后装置E增重3.6g,装置F增重2.2g。则样品中FeCO3的质量m(FeCO3)=_____g。
(4)若缺少G装置,Fe2O3xH2O中x的值会_____。(选填“偏大”、“偏小”、“不变”)
(三)炼铁过程的探究
(1)进行上述实验时,应先点燃A装置中的酒精灯,后对D玻璃管加热,原因是_____。
(2)将上述300℃完全分解后的D装置中剩余固体继续升温,当温度高于500℃时,铁的氧化物全部被CO还原得到铁的质量_____克。(计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】炒菜时加入料酒和食醋,炒出的菜別具香味,其原因之一是料酒中的乙醇与食醋中的乙酸反应生成乙酸乙酯(C4H8O2),试计算:
(1)乙酸乙酯的相对分子质量为_________;
(2)乙酸乙酯中碳、氢元素的质量比为___________;(答最简整数比)
(3)17.6 g乙酸乙酯中所含氧元素的质量为_______g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com