
【题目】请用化学方程式表示下列反应原理
(1)向充满二氧化碳的集气瓶中加入紫色石蕊溶液,振荡后,观察到溶液变红______________。
(2)天然气用作燃料________________。
(3)铝制品耐腐蚀的原因___________________。
科目:初中化学 来源: 题型:
【题目】化学与生活息息相关,请你用化学知识回答下列问题。
(1)下列生活情景中主要利用了物质化学性质的是_____(填字母序号)。
A  食品充氮防腐 B
食品充氮防腐 B  金属制作炊具
金属制作炊具
C  氢气作火箭燃料 D
氢气作火箭燃料 D  干冰用于人工降雨
干冰用于人工降雨
(2)我国传统节日的习俗中也蕴含了许多化学知识。用墨汁书写的春联字迹长时间不变色的原因是_____,端午节挂散发特殊气味的艾草来驱虫,从微观的角度解释是因为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请用化学方程式表示或解释下列反应原理:
(1)发令枪(弹药主要成分为红磷)发令时产生大量的白烟。
_________;
(2)氨气(NH3)是一种刺激性味的气体,具有可燃性,燃烧会产生水和另外一种气体单质。写出氨气燃烧的化学方程式。
_________;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是初中化学中的四个小实验,请回答:
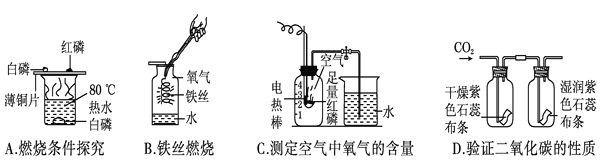
(1)A中_______________能燃烧(白磷的着火点为40 ℃,红磷的着火点为240 ℃)。
(2)B中发生反应的化学方程式是__________________,水的作用是________________。
(3)C实验在操作无误的情况下可得出的结论是_________________。
(4)D实验可得出CO2具有的化学性质是________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“对比实验”是科学探究常用的方法,根据下列所示的实验示意图回答问题。
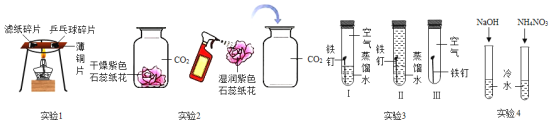
(1)实验1中,将大小相同的滤纸片和乒乓球碎片放在薄铜片的两侧,加热铜片的中部,观察现象。通过此实验,可说明燃烧的条件之一的是_______(填序号)。
A可燃物 B空气 C温度达到着火点
(2)实验2中,把干燥的紫色纸花和湿润的紫色石蕊纸花分别伸入两瓶干燥的二氧化碳气体中,下列有关说法正确的是______(填序号)。
A CO2与水发生了反应 B湿润的紫色石蕊纸花变红
C水具有酸性 D干燥的紫色石蕊纸花变红
(3)实验3是探究铁钉条件的实验,会出现明显现象的是试管_____(填序号),说明铁生锈实际上是铁与_______发生反应。
(4)实验4中____(填“左”或“右”)边试管发烫。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用“![]() ”、“
”、“![]() ”分别表示氢原子和氧原子,下图在点燃条件下,氢气与氧气反应的微观模拟图。请回答下列问题:
”分别表示氢原子和氧原子,下图在点燃条件下,氢气与氧气反应的微观模拟图。请回答下列问题:
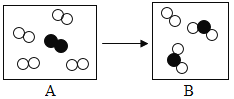
(1)氢气燃烧的化学方程式是____________________________;依据该反应的微观粒子数目之比,在B图中将相关粒子图形补充完整____________________________。
(2)由该微观模拟图,你得出的信息是____________________________;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙为初中化学常见物质,其转化关系如下图所示(“→”表示由一种物质转化成另 一种物质,反应条件、部分反应物和生成物已略去)。
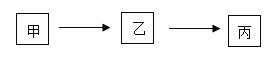
(1)若甲、乙、丙为稀硫酸、氢氧化铜、硫酸铜中的一种,写出乙到丙的化学方程式_____。
(2)若甲、乙、丙均为含有钙元素的化合物,丙中钙元素的质量分数为 40%,甲与水反应生 成乙并放出大量的热,则乙→丙的化学方程式为_____,丙的用途为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某小组同学设计并进行实验,探究影响过氧化氢分解速率的因素。(实验装置如图所示,夹持仪器已略去)
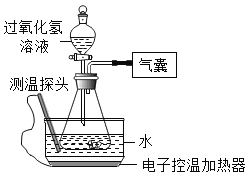
(猜想与假设)
影响过氧化氢分解速率的因素可能有温度、溶液的浓度、催化剂用量。
(实验记录)
同学们进行6组实验,实验记录如下:
实验序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
过氧化氢溶液的 浓度(%) | 30 | 30 | 15 | 30 | 30 | 30 |
过氧化氢溶液的 体积(mL) | 6 | x | 6 | 6 | 6 | 6 |
水槽中水的温度 | 20 | 90 | 70 | 70 | 20 | 20 |
锥形瓶中的物质 | 0.1g MnO2 | 0.5g MnO2 | ||||
6min内产生氧气(mL) | 0.0 | 41.0 | 4.5 | 12.1 | 2.0 | 650.0 |
(解释与结论)
(1)实验②中应加入过氧化氢溶液的体积x是________mL。
(2)实验①-⑥可以通过测定__________来比较过氧化氢的分解速率。
A 相同时间内产生氧气的体积
B 产生相同体积的氧气所需时间
C 相同时间内产生氧气的质量
(3)得出“过氧化氢溶液的浓度越大分解速率越快”结论所依据的实验是____(填序号)。
(4)通过实验①、②、④可得出的结论是_________。
(反思与评价)
(5)同学们认为实验室制氧气,应选择实验⑥而不选实验②的理由是________(答一点即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com