
| A. | Ba(NO3)2→BaSO4 | B. | H2SO4→HCl | C. | CuO→Cu(OH)2 | D. | Ba(OH)2→Fe(OH)3 |
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:初中化学 来源: 题型:选择题
| A. | Cl- | B. | NH${\;}_{4}^{+}$ | C. | Mg2+ | D. | CO${\;}_{3}^{2-}$ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 煤的气化是指将固态煤粉碎成气态煤,以使煤燃烧时能与氧气充分接触而完全燃烧 | |
| B. | 煤的焦化是使煤在隔绝空气的情况下加强热使煤分解,因此该变化是化学变化 | |
| C. | 在汽油中加入一定比例的乙醇(俗称:酒精),使燃料燃烧更充分,可减少环境污染 | |
| D. | 煤、石油、天然气是埋藏在地下的不可再生的化石燃料,要节约利用 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
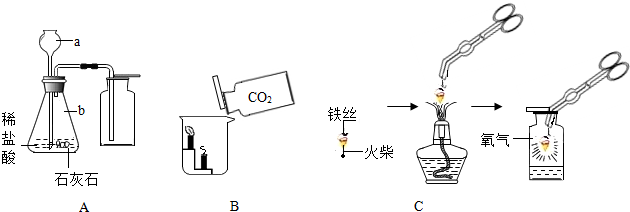
| 物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
| 燃烧时 的现象 | 剧烈燃烧,发出 耀眼白光,无火星 | 剧烈燃烧 极少火星 | 剧烈燃烧 少量火星 | 剧烈燃烧 火星四射 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
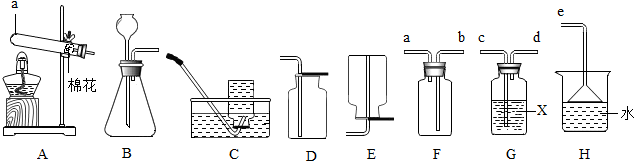
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
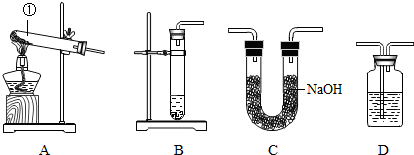
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
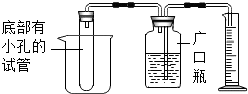 小科在学习了金属的化学性质后,想对锌、铜合金中锌的质量分数进行粗略测定.在老师的指导下,他设计了如图所示的实验装置,并选用了三种试剂:A.蒸馏水 B.锌、铜合金 C.稀硫酸.根据小科的实验思路,请你思考:
小科在学习了金属的化学性质后,想对锌、铜合金中锌的质量分数进行粗略测定.在老师的指导下,他设计了如图所示的实验装置,并选用了三种试剂:A.蒸馏水 B.锌、铜合金 C.稀硫酸.根据小科的实验思路,请你思考:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
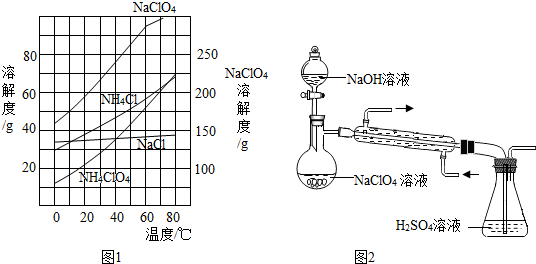
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com