
【题目】某化学探究小组用一定量AgNO3和Al(NO3)3的混合溶液进行了图6实验,已知溶液甲呈蓝色。
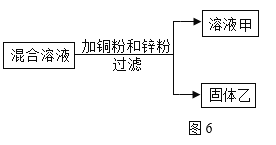
(1)“过滤”操作所需要的玻璃仪器是______________,玻璃棒的作用是__________。
(2)由以上实验可知,四种对应金属的活动性由强到弱顺序为____________。
(3)向固体乙上滴加稀盐酸时__________ (填“有”或“没有”)气泡产生。
(4)溶液甲中一定含有的溶质是___________,可能含有的溶质是_____________。
(5)请写出混合溶液中加入金属粉末后所发生反应的化学方程式_________________。
【答案】玻璃棒、烧杯、漏斗 引流 Al>Zn>Cu>Ag(或铝>锌>铜>银) 没有 Al(NO3)3、Zn(NO3)2、Cu(NO3)2(或硝酸铝、硝酸锌、硝酸铜) AgNO3(或硝酸银) Zn+2AgNO3=2Ag+Zn(NO3)2、Cu+2AgNO3=2Ag+Cu(NO3)2
【解析】
(1) “过滤”操作所需要的玻璃仪器有玻璃棒、烧杯、漏斗,故填写:玻璃棒、烧杯、漏斗;
玻璃棒在过滤中的作用是引流,故填写:引流;
(2)铜和锌都不与硝酸铝反应,说明铝的金属活动性比铜和锌强,硝酸银与铜和锌都反应,说明银的金属活动性比铜和锌弱,硝酸银先与锌反应,当锌反应完,才与硝酸铜反应,说明锌的金属活动性比铜强,故填写:Al>Zn>Cu>Ag(或铝>锌>铜>银);
(3)因为溶液甲呈蓝色,说明有硝酸铜的存在,因此就不会有比铜活动性强的锌剩余,因此过滤、洗涤后往固体乙中加入稀盐酸,没有气泡产生,故填写:没有;
(4)溶液甲中一定含有没参加反应的硝酸铝,反应产生的硝酸锌,硝酸铜,故填写:Al(NO3)3、Zn(NO3)2、Cu(NO3)2(或硝酸铝、硝酸锌、硝酸铜);
当硝酸银与铜和锌都反应完,仍有剩余,此时,溶液甲中就含有硝酸银,若硝酸银与铜和锌都反应完,没有剩余,此时,溶液甲中就不含有硝酸银,由此可得,硝酸银是否存在于溶液甲中有两种情况,因此,可能含有的溶质是硝酸银,故填写:AgNO3(或硝酸银);
(5)该实验过程中所发生反应的化学方程式有:锌与硝酸银反应生成硝酸锌和银,铜与硝酸银反应生成硝酸铜和银,反应的方程式分别为:Zn+2AgNO3=2Ag+Zn(NO3)2、Cu+2AgNO3=2Ag+Cu(NO3)2,故填写: Zn+2AgNO3=2Ag+Zn(NO3)2、Cu+2AgNO3=2Ag+Cu(NO3)2。


科目:初中化学 来源: 题型:
【题目】已知反应 A+B=C+D,若 A、C 为单质,B、D 为化合物,则该反应所属的基本反应类型是______________;若 A 的溶液呈蓝色,B 为烧碱,则该反应的化学方程式为__________;(写 出一个即可);若四种物质均为化合物,且 C 为盐,D 为水,但该反应不一定属于中和反应, 其具体例子为______________(写出一个方程式即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】暖宝宝贴(主要成分为铁粉、木炭、食盐)的热量来源与铁粉的氧化。小涛同学设计使用暖宝宝贴来测定空气中氧气的含量,实验开始前的装置如图所示,实验后从量筒中流入玻璃瓶(容积为250mL)中的水的体积为45mL(铁粉生锈消耗的水忽略不计)。下列说法错误的是( )
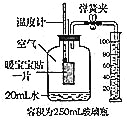
A.实验前必须检查装置的气密性
B.通过本次实验数据测得空气中氧气的体积分数为18%
C.若实验测得空气中氧气体积分数偏低,可能是暖宝宝贴的使用数量不足
D.必须等温度计的读数恢复至实验前的温度后才能记录量筒内剩余水的体积
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将稀盐酸分别滴入盛有不同物质的试管中,如图所示。
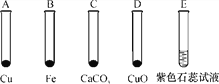
(1)不能发生反应的是________(填序号,下同)。
(2)有气泡产生的是________。
(3)溶液能变成浅绿色的是________。
(4)生成蓝色溶液的是________。
(5)溶液变成红色的是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】建立模型是学习化学的重要方法,下列化学模型中正确的是()
A. 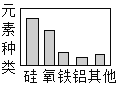 地壳中元素含量B.
地壳中元素含量B. 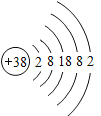 这是一种非金属元素
这是一种非金属元素
C. 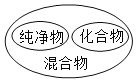 物质的分类模型D.
物质的分类模型D. 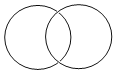 氧化反应、化合反应关系模型
氧化反应、化合反应关系模型
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某种催化剂可将汽车尾气中的一氧化碳、二氧化氮转化为两种空气中的无毒成分,反应的微观示意图如下。下列说法正确的是
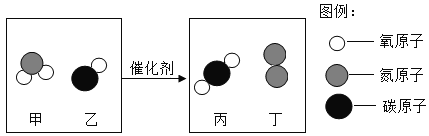
A.四种物质均属于化合物
B.物质丁由原子构成
C.参加反应的甲与生成的丁的分子个数比为2:1
D.参加反应的甲与乙的质量比为1:2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】彩漂洗衣液能够去渍、除菌,白色和彩色织物均可使用。彩漂洗衣液中含有过氧化氢。实验小组对过氧化氢的某些性质进行探究。
Ⅰ.不稳定性
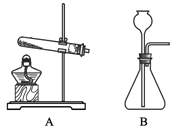
(1)过氧化氢易分解。实验室用其制取氧气时,所选用的发生装置为_____(填字母序号)。
(2)6.8g过氧化氢全部分解产生O2的质量为_____g。
Ⅱ.漂白性
(查阅资料)过氧化氢溶液可漂白一些有色物质。

(进行实验)
实验1:室温下用10%的过氧化氢溶液浸泡一块红色布条,浸泡时间与布条颜色变化如下表。
浸泡时间 | 20min | 40min | 60min |
布条颜色的变化 | 无明显变化 | 颜色稍变浅 | 颜色明显变浅 |
实验2:将红色布条分别浸泡在4种溶液中,现象如下表。
编号 | ① | ② | ③ | ④ |
实验 |
|
|
|
|
布条颜色 | 无明显变化 | 颜色稍变浅 | 颜色稍变浅 | 颜色明显变浅 |
(解释与结论)
(3)实验1的目的是_____。
(4)实验2中,欲得出“其他条件相同时,升高温度可使过氧化溶液的漂白性增强”的结论,需要对比实验_____(填编号)。
(5)实验2中,通过对比②③④,得出的结论是_____。
(6)根据上述实验,推测“使用彩漂液时水温不宜超过50℃”的原因是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是固体甲、乙的溶解度曲线图,下列说法正确的是
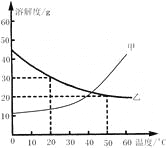
A.甲物质的溶解度大于乙物质的溶解度
B.甲、乙两物质的溶解度都随温度升高而减小
C.用冷却热饱和溶液的方法可除去混在甲中的乙物质
D.20℃时,可配制质量分数为30%的乙物质溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】提升“中国芯”的性能是我国信息产业的当务之急。“中国芯”的核心材料是高纯度的单质硅,工业上制取粗硅的化学方程式为:SiO2+2C![]() Si+2CO↑,下列说法正确的是
Si+2CO↑,下列说法正确的是
A. 硅元素在地壳中的含量比氧元素多B. 该反应的基本类型为置换反应
C. 在此反应中硅元素的化合价升高D. 该反应体现了碳的氧化性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com