
【题目】现有碳酸钙、氯化钙组成的混合物样品。小军想计算混合物中各成分的质量,进行了如下图所示的实验:

请回答。下列问题:
(1)写出发生反应的化学方程式____________________________;
(2)列出求解生成沉淀质量x的比例式______________________;
(3)混合物样品中各成分的质量比为____________________;
(4)在加入碳酸钠溶液的过程中,烧杯中溶质质量的变化情况为_____________________;
(5)若最终所得的不饱和溶液B的溶质的质量分数为5%,则加入水的质量为__________。
【答案】(1)CaCl2+Na2CO3==CaCO3↓+2NaCl
(2)106/100=10.6g/x (3 )111:50
(4)氯化钙的质量逐渐减少至消失,氯化钠的质量逐渐增多(5)32.9g
【解析】
试题分析:(1)氯化钙与碳酸钠反应生成的是碳酸钙沉淀和氯化钠:CaCl2+Na2CO3==CaCO3↓+2NaCl;
(2)利用化学方程式,根据反应的质量比即可计算出生成的碳酸钙沉淀的质量。
加入的碳酸钠溶液中溶质碳酸钠的质量=100g×10.6%=10.6g
设生成的碳酸钙的质量为x,设氯化钙的质量为y,生成的氯化钠的质量为z,
CaCl2+Na2CO3==CaCO3↓+2NaCl
111 106 100 117
y 10.6g x z
106/100=10.6g/x
X=10g
(3)106/111=10.6g/y,y=11.1g
混合物中碳酸钙的质量=16.1g-11.1g=5g,
氯化钙与碳酸钙的质量比=11.1:5=111:50;
(4)氯化钙与碳酸钠反应生成的是碳酸钙沉淀和氯化钠,故氯化钙的质量逐渐减少至消失,氯化钠的质量逐渐增多;
(5)反应后溶液中溶质的质量为氯化钠,生成的氯化钠的质量为:
106/117=10.6g/z,z=11.7g
反应后溶液的质量=16.1g+100g+100g-15g=201.1g
溶液稀释前后溶质的质量不变,设稀释后溶液的质量为a,那么:
5%a=11.7g ,a=234g
加入水的质量=234g-201.1g=32.9g


科目:初中化学 来源: 题型:
【题目】能源、环境与人类的生活和社会发展密切相关。
(1)目前,人类以化石燃料为主要能源,常见的化石燃料包括石油、天然气和 ,它们都属于 (选填“可再生”或“不可再生”)能源。
(2)为减少污染、提高煤的利用率,可将其转化为可燃性气体,此过程可认为是碳与水在高温的条件下进行的化学反应,其微观示意图如下所示,写出该反应的化学方式: 。

(3)为减少温室气体排放,人们正在积极寻找不含碳元素的燃料。经研究发现NH3燃烧的产物没有污染,且释放大量能量,有一定应用前景。
①![]() 中氮元素和氢元素的质量比为 ;
中氮元素和氢元素的质量比为 ;
②将![]() 燃烧反应的化学方程式补充完整:4NH3 + 6O2点燃6 H2O+ ;
燃烧反应的化学方程式补充完整:4NH3 + 6O2点燃6 H2O+ ;
(4)目前,人们正在利用和开发许多其他能源,如: 等(写出一种即可)。这些能源的利用,可以部分解决化石能源面临耗尽的问题,并在一定程度上减少了对环境的污染。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关水的知识中,正确的说法是( )
A.水是一种最常见的溶剂,水不能称作为自然资源。空气才是自然资源。
B.常用的硬水软化的方法,蒸馏和煮沸都是物理变化。
C.电解水时生成的氢气和氧气的质量比为2 : 1
D.水是由氧元素和氢元素组成的。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属氧化物陶瓷着色,有时测定金属氧化物中的金属含量。现将Fe2O3、CuO、Al2O3的混合物16克,与109.5克20%的稀盐酸混合后恰好完全反应,则此金属氧化物着色剂中金属元素的含量是
A.20% B.70% C.73.5% D. 80%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是a、b、c三种物质(均不含结晶水)的溶解度曲线。

①t1℃时物质的溶解度a b(填“>”或“<”或“=”);
②t2℃时将28g a物质加入到50g水中充分溶解,所得溶液的质量为 g,其中溶质与溶剂的质量比为 ;
③t1℃时,欲将c物质在m点对应的溶液变为p点的溶液,可采用的方法是 (写一种即可);
④t2℃时,将等质量的a、b、c三种物质的饱和溶液分别降温到t1℃时,所得溶液中的各项关系符合b>a>c的是 (填序号)。
Ⅰ.溶质质量 Ⅱ.溶剂质量 Ⅲ.溶液质量 Ⅳ.溶质的质量分数
⑤欲配置100g质量分数为15%的a物质的溶液,所需a物质 g,所需蒸馏水的体积为 mL,可选择的量筒规格为 mL(填50或100),溶解时玻璃棒的作用是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是实验室制取气体常见的装置,据图回答有关问题。
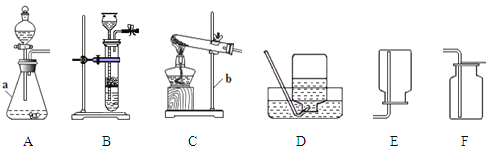
① 写出指定仪器的名称:a. ;b. ;
② 实验室制取二氧化碳气体,装置A、B都可用作发生装置,其中可以随时使反应发生或停止的装置是 (填序号,下同),可选用的收集装置是 。
③ 用装置C作为发生装置制取氧气,发生反应的化学方程式为 ;用装置D收集氧气,气体收集完毕时,应先 (填“从水中取出导气管”或“熄灭酒精灯”);氧气收集完成后,测得其纯度明显偏低,原因可能是 (填序号)
Ⅰ.氯酸钾中加入了二氧化锰 Ⅱ.收集前,集气瓶中未注满水
Ⅲ.收集后,集气瓶中仍有少量水 Ⅳ.未见气泡连续均匀冒出时就开始收集
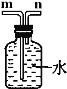
④ 实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水的速率,以免剧烈反应放热引起发生装置炸裂。你认为上图中最适合制取乙炔气体的发生装置是 ;如果用右图所示装置收集乙炔,气体应从 (填“m”或“n”)端管口通入。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学符号填空:
(1)炒菜用的盐______ _____;
(2)3个钾离子____ _____;
(3)2个硅原子______ ____;
(4)+1价氮的氧化物______ _____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com