
【题目】下图为甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
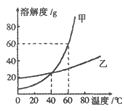
A. 20℃时,甲物质的溶解度比乙物质的溶解度大
B. 甲物质中混有少量乙物质,采用恒温蒸发溶剂的方法提纯甲物质
C. 40℃时,甲、乙两种物质的饱和溶液中溶质质量相等
D. 60℃时,,甲物质的溶解度是60g,所以将80g甲物质放入100g 水中,所得溶液中溶质质量与溶剂质量之比是:60g:100g=3:5
科目:初中化学 来源: 题型:
【题目】环境问题是人类可持续发展必须解决的一个重要问题,温室效应被列为21世纪人类面临的最大威胁之一,已引起人们的广泛关注。旨在限制发达国家温室气体排放量、抑制全球范围内气候持续变暖的《京都议定书》,已于2005年2月16日正式生效。
(1)二氧化碳是大气中的主要温室气体,我国二氧化碳的排放量位居世界第二,为减缓温室效应,我们可以采取的措施有(只填2种):________________;_____________。
(2)为减缓二氧化碳使全球变暖的趋势,有科学家提出大胆设想:将排放到空气中的二氧化碳压缩使其液化,然后将其压入到冰冷的深海中。但也有科学家担心海水中富含二氧化碳后酸度会增加,可能会杀死一些海洋生物,甚至会溶解掉部分海床,同时气候变化也可能改变海洋环流,把海底的二氧化碳又带回海面,另外把二氧化碳压入海底所消耗的能源可能会再增加二氧化碳的排放。已知温度越高、压强越小,气体在水中溶解得越少。
A、 二氧化碳气体转变为液体时将会__________能量(填“释放”或“消耗”);
B、二氧化碳使海水酸度增加的原理的反应表达式为_________ ;
C、二氧化碳在深海中比在通常状况下的水中的溶解得(填“多”或“少”)_______,原因是_____________。
(3)二氧化碳在化学家的眼里是可以利用的重要资源,只要有合适的条件,可以像发生光合作用那样将二氧化碳转变为所需要的产物。二氧化碳可以为化工合成提供足够的碳元素,既可以减少化工产业对煤和石油的消耗,又可以缓解大气中二氧化碳含量的增加。
A、二氧化碳和水通过光合作用转变为葡萄糖和氧气的反应表达式为:_______________。
B、我国科学家陈乾旺等最新研究成果表明,在一定条件下,二氧化碳和金属钠反应产生金刚石和碳酸钠,请从人类生存的角度分析,金刚石与水相比谁更宝贵______,理由是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行研究。
【查阅资料】(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成.
(2)氯化钙、氯化钡溶液均呈中性.
【提出问题】(1)酒精中是否含有碳元素?
(2)固体酒精中的氢氧化钠是否变质?
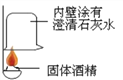
【实验探究】(1)按图实验,发现澄清石灰水变浑浊,可得出酒精中含有碳元素的结论.此结论_____________(选填“合理”或“不合理”).
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀.取沉淀与试管中加稀盐酸,有气泡产生.写出产生沉淀的化学方程式____________.分析实验并结合资料得出氢氧化钠已变质.
(3)为进一步确定氢氧化钠的变质程度,分组探究.
①甲组取烧杯上层清液于两支试管中,按下图探究.
方案 |
|
|
现象 | 溶液变红 | 产生______________ |
结论 | 清液中有氢氧化钠 | 清液中有碳酸钠 |
②乙组认为甲组实验不能证明清液中一定有氢氧化钠,理由是 ____________.他们另取烧杯中上层清液,加足量氯化钡溶液,充分反应后滴加酚酞溶液,酚酞溶液变红.
【实验结论】经讨论一致认为固体酒精中的氢氧化钠部分变质.
【反思交流】乙组实验中加足量氯化钡溶液的目的是 ____________
【拓展应用】要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的____________ .(填序号)
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验数据合理的是
A. 用 pH 试纸测得某地雨水的 pH 为 5.6
B. 用 10 mL 量筒量取了 6.53 mL 水
C. 用 20 g 氯化钠和 100 g 水配制的 120 g 食盐水,其溶质质量分数为 20%
D. 用托盘天平称得某纯碱样品的质量为 10.2g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学发现,上个月做实验用的 NaOH 溶液忘记了盖瓶盖。对于该溶液是否变质,同学们开 始实验探究。
【猜想假设】猜想 1:该溶液没有变质,为 NaOH 溶液。 猜想 2:该溶液全部变质,为Na2CO3溶液。
猜想 3:该溶液部分变质,为_______。
【设计方案】请你完善下表几组同学探讨的设计方案:
实验操作 | 可能出现的现象与结论 | 同学评价 | |
第 1 组 |
| 若溶液变红,则猜想 2 不成立 | 第 2 组同学认为:此方 案结论不正确,理由是___ |
第 2 组 |
| 若 _________________________,反 应 方 程 式:____________ , 则猜想 1 不成立 | 第 3 组同学认为:此方 案还不能确定猜想 2 还 是猜想 3 成立 |
第 3 组 | 第一步 第二步
| 若 滤 液 不 变 红 ,则 猜 想 2 成 立;若滤液变红,则猜想 3 成 立 | 第 1 组同学认为:不需 过 滤 也 能 达 到 实 验 目 的,更简单的操作方法 是:_________ |
【探究实验】综合各小组的方案后,动手实验。
【结论】NaOH 溶液易与空气中CO2反应而变质,所以 NaOH 溶液要_______保存。
【反思】实验结束后,还有同学认为,第 2 组同学的CaCl2溶液可换成Ca(OH)2溶液,同样也能完 成本实验,你是否赞成 _______(填“是”或“否”)理由是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有一份碳酸钠和硫酸钠的混合粉末,为测定其中碳酸钠和硫酸钠的质量比,小冰做了如图所示的实验:
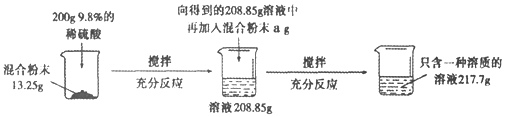
请回答下列问题:
(1)上述实验过程中发生反应的化学方程式为____________________________;
(2)向13.25g样品中加入200g稀硫酸后,生成气体的质量为_______________;
(3)根据已知条件,列出求解与13.25g样品反应的稀硫酸中溶质质量(x)的比例式________________;
(4)a的数值是_________;
(5)混合粉末中碳酸钠和硫酸钠的质量比为_________;
(6)若要使最终所得溶液溶质的质量分数变为10%,则需要向其中加入水的质量为____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】勇往直前学习小组的同学在进行酸碱的化学性质的实验活动。同学们的实验步骤如图所示:
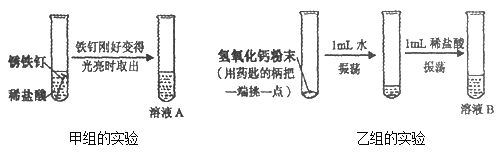
【收集证据1】(1)甲组实验中发生反应的化学方程式为①_______________________,乙组实验并不能充分证明氢氧化钙能与稀盐酸发生反应,是因为他们在加入稀盐酸前忘记了滴入②________。取用氢氧化钙时“用药匙的柄把一端挑一点”的目的是③________。
【继续实验】为妥善处理实验后所得到的废液,同学们将试管内的溶液A、B混入同一废液缸中,开始无明显现象,一段时间后出现了红褐色沉淀,过滤得到无色滤液,同学们对无色滤液中的离子组成产生了兴趣,进行继续探究:
【提出问题】除Cl_外,废液缸中还含有哪几种离子?
【猜想与假设】小冰:H+、Ca2+、Fe3+ 小城:Ca2+、OH_ 小美:(2)________________
上述猜想中,小冰的猜想一定是错误的,不需验证,理由是(3)______________。
【设计实验】为得出结论,同学们设计了下图实验,根据实验现象可以得出(4)________的猜想是正确的,从而得出结论。
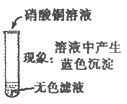
【总结与归纳】回顾整个实验过程,可以归纳出氢氧化钙的化学性质是与(5)_______(填物质类别)反应,同时还可归纳出:分析反应后溶液的离子组成时,除了有时可以依据溶液的颜色外,更多时候是根据两种废液混合后产生的(6)______________来推知某些离子的有无。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下表信息,相关说法正确的是( )

A.20℃时,NaCl 的溶液度为 36.0
B.40℃时,KCl 饱和溶液的溶质质量分数为 40%
C.40℃时,向 100g 水中加入 50gNH4Cl 充分溶解,溶液质量为 145.8g
D.60℃时降温到 20℃时,KNO3 和 KCl 的饱和溶液析出晶体较多的是 KNO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用数轴表示某些化学知识直观、简明、易记。下列数轴表示错误的是
A. 硫及其化合物与化合价的关系:![]()
B. 银、铜、铁的金属活动性强弱: ![]()
C. 物质形成溶液的pH:![]()
D. 形成溶液时的温度:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com