
| A. | 5g | B. | 10g | C. | 15g | D. | 20g |
科目:初中化学 来源: 题型:选择题
| A. | 农业和园林灌溉,改大水浸灌为喷灌、滴灌 | |
| B. | 改进汽车发动机的燃烧方式,使汽油充分燃烧 | |
| C. | 回收利用废旧金属、废旧书籍及废旧塑料 | |
| D. | 为提高粮食产量,大量使用各种化肥、农药 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
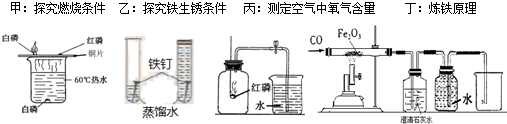
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 保存方法 | 原 因 |
| A | 生石灰应密封保存 | 生石灰易与空气中的氧气反应 |
| B | 浓盐酸应密封保存 | 浓盐酸在空气中易分解 |
| C | 烧碱应密封保存 | 烧碱易潮解且与空气中二氧化碳反应 |
| D | 白磷应保存在水中 | 白磷有剧毒 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
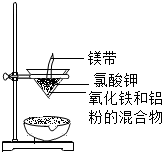 铝和氧化铁的反应:2Al+Fe2O3$\frac{\underline{\;900℃-1550℃\;}}{\;}$Al2O3+2Fe称为“铝热反应”(如图所示),引燃镁条,漏斗内的物质熔化,镁条燃尽,漏斗下端仍持续产生大量熔融物落入沙中,该熔融物可用于焊接铁轨
铝和氧化铁的反应:2Al+Fe2O3$\frac{\underline{\;900℃-1550℃\;}}{\;}$Al2O3+2Fe称为“铝热反应”(如图所示),引燃镁条,漏斗内的物质熔化,镁条燃尽,漏斗下端仍持续产生大量熔融物落入沙中,该熔融物可用于焊接铁轨| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1565 | 1462 |
| 沸点/℃ | 246 | 2980 | 2750 | -- |
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量冷却后的熔融物于试管中,加入 氢氧化钠溶液 | 有气泡产生 | 熔融物重含有铅 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
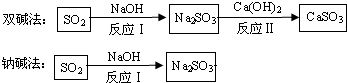
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com