
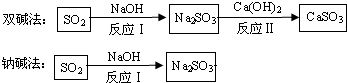
分析 (1)根据反应Ⅰ是氢氧化钠与二氧化硫的反应,写化学方程式;
(2)根据反应Ⅱ是亚硫酸钠与氢氧化钙的反应,判断反应类型;并计算CaSO3中Ca、S、O元素的质量比;
(3)通过数据和流程得出双碱法所需的原料成本更低的原因.
解答 解:(1)反应Ⅰ是氢氧化钠与二氧化硫的反应,化学方程式为SO2+2NaOH=Na2SO3+H2O;
(2)反应Ⅱ是亚硫酸钠与氢氧化钙的反应,发生的方程式为:Na2SO3+Ca(OH)2=CaSO3+2NaOH;属于复分解反应;CaSO3中Ca、S、O元素的质量比40:32:48=5:4:6;
(3)两种工艺中,处理相同量的SO2,双碱法所需的原料成本更低,原因是通过反应II实现了NaOH的循环利用,减少了NaOH的用量,所以成本降低.
故答案为:
(1)SO2+2NaOH=Na2SO3+H2O;
(2)Na2SO3+Ca(OH)2=CaSO3+2NaOH;复分解反应;5:4:6;
(3)通过反应II实现了NaOH的循环利用,减少了NaOH的用量,所以成本降低.
点评 本题联系生活考查了环境污染和资源综合利用方面的知识,同学们需要在平常生活中提高“节能、环保”的意识.


科目:初中化学 来源: 题型:选择题
| A. | 5g | B. | 10g | C. | 15g | D. | 20g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 已知A 与B、甲与乙均为初中化学常见的物质,且下列三种情况中的A 为甲烷、稀硫酸、硝酸银中的一种,其转化关系如图所示.
已知A 与B、甲与乙均为初中化学常见的物质,且下列三种情况中的A 为甲烷、稀硫酸、硝酸银中的一种,其转化关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 给烧瓶、烧杯里的固体物质加热时,一定要垫上石棉网,防止受热不均而炸裂 | |
| B. | CO还原CuO实验结束时,先熄灭酒精灯,冷却后再停止通CO,防止红热的铜被氧化 | |
| C. | 稀释浓硫酸时,要将水沿烧杯内壁缓慢注入浓硫酸中,并用玻璃棒不断搅拌 | |
| D. | 测溶液的PH时,用玻璃棒蘸取待检液涂在湿润后的PH试纸上,再与比色卡对比读数 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 石油分馏出汽油、柴油等 | B. | 利用渗透膜从海水中获得淡水 | ||
| C. | 铁矿石冶炼成铁 | D. | 工业上从空气中分离出氧气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com