
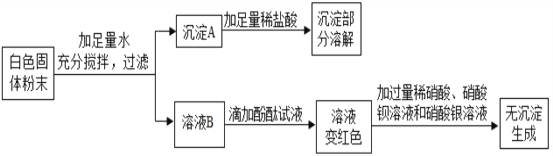
【题目】一包白色固体可能含有 Ba(NO3)2、NaCl、NaOH、Na2SO4、CuSO4 中的一种或几种。为确定其组成,某同学设计了如下实验方案:
下列判断正确的是
A. 原固体中一定有Ba(NO3)2、NaOH、CuSO4 和Na2SO4
B. 沉淀 A 中一定有Cu(OH)2 和BaSO4
C. 溶液 B 中一定有NaOH 和 Na2SO4,一定没有CuSO4
D. 原固体中一定没有 NaCl和Na2SO4
【答案】B
【解析】硫酸铜和氢氧化钠反应生成蓝色的氢氧化铜沉淀,氢氧化铜沉淀溶于酸,硝酸钡和硫酸钠反应生成不溶于酸的硫酸钡沉淀,碱溶液能使酚酞变红色,硫酸根离子和钡离子反应硫酸钡沉淀,氯离子和银离子反应会生成氯化银沉淀。白色固体粉末加入足量的水水后,得到沉淀A和溶液B,沉淀A中加入稀盐酸,部分溶解,所以沉淀A中一定含有氢氧化铜沉淀和硫酸钡沉淀,白色固体粉末中一定含有硝酸钡、氢氧化钠、硫酸铜,可能含有硫酸钠,溶液B中加入酚酞,溶液变红色,所以B中一定含有氢氧化钠,加入足量的硝酸、硝酸钡、硝酸银,无沉淀生成,所以白色固体粉末中一定不含氯化钠,因此:
A、原固体中一定有 Ba(NO3)2、NaOH、CuSO4,可能含有Na2SO4,错误;
B、沉淀A中一定有 Cu(OH) 2 和 BaSO4,正确;
C、溶液B中一定有 NaOH,一定没有Na2SO4和CuSO4,错误;
D、原固体中一定没有NaCl,可能含有Na2SO4,错误。故选B。


科目:初中化学 来源: 题型:
【题目】A、B、C为初中化学常见的物质,且都含有同一种元素,它们之间的反应关系如下(→表示一步反应的转化):
![]()
(1)若A、B组成元素相同,B含量过多导致温室效应加剧,写出一个符合B→C的化学方程式:_____。
(2)若B位密度最小的气体,A、C的化学式可以是_______(填序号)
①HCl、H2O ②H2SO4、NaOH ③H2O2、H2CO3
(3)若A、B、C是不同类型的化合物,B是改良酸性土壤的碱,B→C发生中和反应,则A可以是____,写出B→C的化学方程式:_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是A、B、C三种固体物质的溶解度曲线.下列分析不正确的是( )
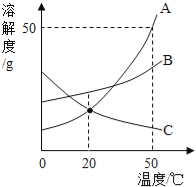
A. 50℃时,三种物质的溶解度由大到小的顺序是A>B>C
B. 50℃时,把50gA放入50g水中能形成75gA的饱和溶液
C. 将C的饱和溶液变为不饱和溶液,可采用降温的方法
D. 分别将三种物质的饱和溶液从50℃将至20℃时,所得溶液溶质质量分数大小关系是B>C=A
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学晚会上,某同学表演了一个化学小魔术“空瓶生烟”,两瓶分别盛有氯化氢气体和氨气,当两种气体相结合,会看到瓶中充满浓浓的白烟。下图为该反应的微观模拟示意图,下列说法中,正确的是 ( )

A. 该反应的生成物是一种氮肥
B. 参加反应的两种物质的分子个数比为1:2
C. 该反应属于复分解反应
D. 化学反应前后,分子和原子的种类都没有改变
查看答案和解析>>
科目:初中化学 来源: 题型:
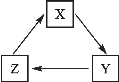
【题目】下列各组物质间通过一步反应就能实现如图转化的是
X | Y | Z | |
A | Fe | FeCl2 | Fe2O3 |
B | Ca(OH)2 | NaOH | NaCl |
C | AgNO3 | Ba(NO3)2 | BaSO4 |
D | H2O | O2 | CO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碱式碳酸镁是白色粉末,不溶于水,可用于镁盐制备、制药工业等,其组成一般以xMgCO3yMg(OH)2zH2O 表示。某化学兴趣小组同学在老师带领下参观了碱式碳酸镁的生产流程,并设计实验确定碱式碳酸镁的组成。
Ⅰ 碱式碳酸镁的制备
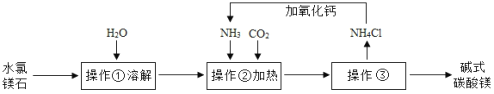
(1)操作③的名称是__________。
(2)上述流程中NH3被循环使用,流程中生成NH3的化学方程式为:①CaO+H2O═Ca(OH)2;②_______。
(3)判断碱式碳酸镁是否洗涤干净,可向最后的洗出液中滴加_______(填字母),观察现象判断。
A.盐酸和氯化钡的混合液 B.硝酸和硝酸银的混合液 C.碳酸钠溶液 D.稀盐酸
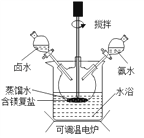
(4)实验室可用复盐 MgCO3 (NH4)2CO3H2O 作原料制备碱式碳酸镁。取一定量原料放入三颈烧瓶中,并将三颈烧瓶放在恒温水浴锅中加热(如下图所示),加入一定量蒸馏水,开启搅拌器同时加入预定的氨水,待温度达40℃时滴加卤水并继续滴入氨水,一段时间后通过系列实验操作得到碱式碳酸镁产品。实验中搅拌的目的是_________,水浴加热的优点是 ________ 。
Ⅱ 测定碱式碳酸镁的组成
【查阅资料】
①MgCO3![]() MgO+CO2↑。② Mg(OH)2
MgO+CO2↑。② Mg(OH)2![]() MgO+H2O。
MgO+H2O。
【实验设计】
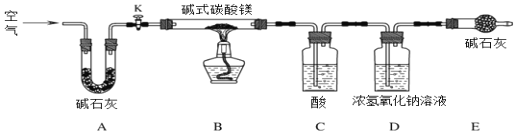
⑸ C中的物质是_________(填名称)。实验过程中,当关闭K后,加热B装置,判断碱式碳酸镁完全分解的方法是:当观察到C中_________,则其已完全分解。D处常用浓氢氧化钠溶液而不用饱和石灰水的原因是____________。
【数据分析】
(6)取碱式碳酸镁[xMgCO3yMg(OH)2zH2O]4.66g,高温煅烧至恒重,得到固体2.00g, CO21.76g,试通过计算确定该碱式碳酸镁中 x:y 的最简整数比________(请写出计算过程)。
(7)若没有 A 装置,则测定得到的z值__________ (填“偏大”、“偏小”、“无影响”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有指定化合价的几种元素; ![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,请选择元素,写出符合要求的化合物的化学式:
,请选择元素,写出符合要求的化合物的化学式:
(1)一种难溶于水的碱________; (2)一种酸________;
(3)一种复合肥料________; (4)原子个数比为1:1的氧化物________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如下图所示是甲、乙、丙三种固体物质的溶解度曲线.下列说法正
确的是()

A. t2℃时,甲、乙两物质的饱和溶液中含溶质的质量相等
B. t1℃时把30g丙放入50g水中能得到80g丙的饱和溶液
C. 将丙的不饱和溶液变为饱和溶液,可以采用降温方法
D. t3℃时,用等质量的甲、乙、丙分别配制成三种物质的饱和溶液,所需溶剂的质量为甲<乙<丙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】定量研究是科学研究的重要方法之一,利用它可以解决许多生产生活中的实际问题。
⑴将20g质量分数为4%的氢氧化钠溶液与7.3g稀盐酸混合,恰好完全反应,所得溶液的PH为7,试计算所用稀盐酸的溶质质量分数。
⑵实验室浓盐酸(分析纯)的溶质质量分数在36%-38%之间为合格药品。(1)题中的稀盐酸是用一定体积(折算成质量为2g)的浓盐酸(分析纯)加水配制而成的。通过计算判断该浓盐酸是否为合格药品。(只写结果,不写计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com