
【题目】如表是硝酸钾、氯化钠在不同温度下的溶解度。

(1)从表中数据分析,溶解度受温度影响较大的物质是_____,硝酸钾和氯化钠溶解度曲线的交点在_____(填字母序号)之间。
A 20℃~30℃ B 30 ℃~40℃ C 40℃~50℃
(2)20 ℃,将50 g硝酸钾与100 g水混合,充分搅拌后静置,得到的溶液是硝酸钾的_____(“饱和”或“不饱和”)溶液,若将温度升高到40 ℃,该溶解溶质的质量分数为_____(精确到0.1%)。
(3)保持温度为20 ℃,将氯化钠的不饱和溶液变成饱和溶液,写出一种可行的方法_____。
【答案】KNO3 A 饱和 33.3% 加溶质(或恒温蒸发溶剂)
【解析】
硝酸钾的解度曲线随温度是升高而增大,氯化钠溶解度随温度的升高增长较缓慢。
(1)根据氯化钠、硝酸钾在不同温度下的溶解度可以看出溶解度受温度影响较大的物质是硝酸钾,硝酸钾和氯化钠的溶解度曲线可能在20 ℃~30 ℃之间出现交点。
(2)在20 ℃时,硝酸钾的溶解度是31.6 g,100 g水中最多溶解31.6 g的硝酸钾,所以20 ℃时,将50 g硝酸钾固体投入100 g水中,充分溶解后可得到硝酸钾的饱和溶液,硝酸钾在40 ℃时,溶解度是63.9 g,所以将温度升到40 ℃,100 g水中能溶解硝酸钾63.9 g,所以得到不饱和溶液,溶质质量分数为![]() 。
。
(3)在20 ℃时,将氯化钠的不饱和溶液含有溶剂较多,故变成饱和溶液可以加溶质、恒温蒸发溶剂等。


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案科目:初中化学 来源: 题型:
【题目】小南发现了许多有趣的化学问题,请你帮助她解决这些问题。
(1)现将300g 25%的NaCl溶液稀释为10%的NaCl溶液,需要加水的质量为_____g;配制的主要步骤有:计算、称量、溶解、装瓶并贴上标签;实验中用到的玻璃仪器有胶头滴管、烧杯、_____、玻璃棒和试剂瓶。
(2)甲、乙、丙三种物质的溶解度曲线如图所示,据图回答:
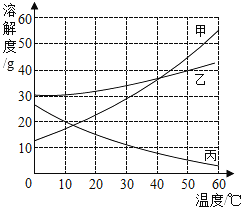
①30℃时,三种物质的溶解度由大到小的顺序为_____;
②要使接近饱和的丙物质溶液变为饱和,可采取的一种措施是_____;
③50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃时,析出晶体最多的是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是CO与CuO反应的实验装置,下列关于该实验说法正确的是( )
①玻璃管中黑色固体变成了红色
②CO被还原为CO2
③玻璃管中发生的反应为置换反应
④既有效地防止了CO对空气的污染,又充分利用了能源
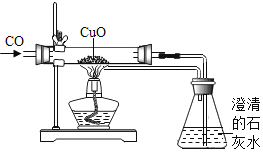
A. ①②B. ①④C. ②④D. ③④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是电解水的实验装置图,试回答下列问题.
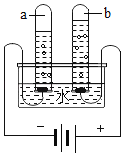
(1)据图可知:a试管内收集到的气体是_____,检验b试管中气体的方法是_____,
(2)在该实验中,a、b两试管中收集的气体体积比约为_____,通过实验可得出有关水的组成的结论是_____.
(3)如图是电解水实验装置.请写出水在通电条件下反应的化学方程式_____.
(4)地球上的总储水量虽然很大,但淡水很少,爱护水资源是每个公民的责任和义务.下列行为属于节约用水的是_____(填序号)
A 公共场所不用随手关水龙头 B 洗完菜的水用来浇花 C 不间断放水刷牙.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一支试管中放入一小段镁条(已擦去氧化膜),再向试管中加入一定量的盐酸,镁条表面有________产生,反应的化学方程式是________________________________________________________。
[发现问题]为了再次观察上述反应现象,小林同学用较长的镁条重做上述实验,但发现了异常现象,试管中出现了白色沉淀。
[实验验证1]小林同学针对两次实验的不同,设计对比实验方案,探究出现异常现象的原因。
试管(盛有同体积同浓度的盐酸) | ① | ② | ③ | ④ |
镁条长度 | 1cm | 2cm | 3cm | 4cm |
相同的实验现象(省略题干现象) | 快速反应,试管发热,镁条全部消失 | |||
沉淀量差异(恢复至20℃) | 无 | 少量 | 较多 | 很多 |
[得出结论]镁条与盐酸反应产生白色沉淀与________有关。
[追问]白色沉淀是什么物质?
[查阅资料]①20 ℃时,100 g水中最多能溶解氯化镁54.8 g;
②镁能与热水反应产生一种碱和氢气;
③氯化银既不溶于水也不溶于稀硝酸。
[做出猜想]猜想一:镁;猜想二:氯化镁;猜想三:氢氧化镁,猜想的依据是____________________(用化学方程式表示)。
[实验验证2]将白色沉淀洗涤干净,分别取少量沉淀于A、B、C试管中,进行如表实验:
试管 | 操作 | 现象 | 结论 |
A | 加入足量盐酸 | ________,白色沉淀________ | 猜想一不正确,但这种白色沉淀能溶于盐酸 |
B | 加入足量水 | 白色沉淀________ | 猜想二不正确 |
C | 加入适量稀硝酸 | 白色沉淀消失 | 原白色沉淀中含有的离子是: |
继续滴加几滴硝酸银溶液 | 出现大量白色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校研究性学习小组对福州某段内河水质的状况进行相关的调查研究。
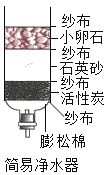
(1)如图所示的自制净水器中的_____物质,可除去水中的异味和色素。
(2)硬水会给生活和生产带来许多麻烦,长期饮用硬水可能会引起体内结石;如用硬水洗涤衣物,既浪费肥皂又洗不干净,时间长了还会使衣物变硬。通过化学学习,我们知道可用_____来区分该内河的水属于硬水还是软水;生活中要降低水的硬度,可采用的方法是________
(3)你认为下列行为会造成内河水质下降的是_____。(填标号)
A 在河边种植花草树木
B 居民将生活污水直接排入内河
C 将垃圾倒入内河中
D 定时定期进行水质监测
(4)请针对现阶段的水污染提2条建议:_____;_____;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】结合以下实验室制取气体的常用装置回答问题:
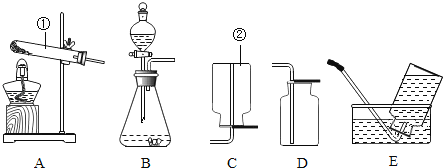
(1)写出标号仪器的名称:①_____②_____。
(2)实验室采用过氧化氢溶液制取氧气时,应选择的发生装置是_____(填序号,下同),锥形瓶中应先放入的药品是_____,它与采用装置A制取氧气时比较,主要优点是_____(任答一条)。如何检查该装置的气密性_____。
(3)实验室制取二氧化碳时,应选用的发生装置是_____(填序号,下同),收集装置是_____。如何检验其是否收集满_____反应的文字表达式为_____。
(4)如果用高锰酸钾制氧气,主要操作步骤有①从水槽中取出导管②检查装置的气密性③停止加热④收集气体⑤加热⑥加入药品,请写出正确的操作顺序___(填序号)。应选用的发生装置是__(填序号),反应的文字表达式为__,所选发生装置中还缺少___。
(5)乙炔又称电石气,是一种无色、无味、密度比空气略小,不溶于水的气体;工业上常用它燃烧产生的高温来切割和焊接金属;实验室用电石(固体)与水反应制取乙炔。你认为制取乙炔应选择的发生装置是_____(填序号,下同);要想收集更纯净的乙炔气体,最好选用的收集装置是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向一定量的NaOH溶液中慢慢通入CO2气体,看不到明显现象。某实验小组的同学对所得溶液成分进行了如下探究。请你参与他们的探究活动,并完成以下问题:
(提出问题)所得溶液中溶质的成分是什么?
(査阅资料)资料一:将CO2气体慢慢地通入一定量的NaOH溶液中,可能发生以下两个化学反应:
先发生反应:2NaOH+CO2═Na2CO3+H2O
当NaOH反应完全后,继续发生反应:Na2CO3+CO2+H2O═2NaHCO3
資料二;Ca(HCO3)2易溶于水;CaCl2溶液与NaCl溶液均呈中性; NaHCO3溶液呈碱性,可使酚酞溶液变红色。
(猜想与假设)小组同学通过讨论,提出了以下四种猜想
猜想一:溶质为NaOH和Na2CO3
猜想二:溶质全为Na2CO3
(1)你认为猜想三:溶质为_____
猜想四:溶质全为 NaHCO3
(实验探究)小组同学设计并完成了如下实验:
实验步骤 | 实验过程 | 实验现象 | 实验结论 |
① | 取适量反应后的溶液置于试管 中,加入过量CaCl2溶液 | 有白色沉淀生成 | (2)猜想_____不成立 |
② | 取适量步骤①反应后的上层清 液,滴加几滴酚酞溶液 | (3)现象为_____ | 猜想二不成立 |
③ | 取适量步骤①反应后的上层清 液,加入适量稀HCl | 有气泡产生 | (4)猜想_____成立 |
(实验总结)针对上述实验,实验小组的同学总结并写出了上述探究过程中的各步反应方程式。
(5)你认为步骤①发生反应的化学方程式是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为氢氧化钠溶液和稀硫酸恰好反应的微观模拟图,请回答下列问题:
(1)将A、B图的粒子图示补充完整_______
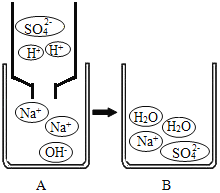
(2)该反应前后没有发生变化的离子的符号是_____
(3)该反应的微观实质是_____。
(4)若将质量相同、溶质质量分数也相同的氢氧化钠溶液和稀硫酸混合后,滴加几滴紫色石蕊溶液后,能观察到紫色石蕊溶液变成___色。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com