
| ʱ��/min | 1 | 2 | 3 | 4 | 5 |
| ����CO2������/g | 6 | 12 | 18 | 22 | 22 |


 ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
| ��������������Һ��������/g | 20 | 40 | 60 | 80 | 140 | 160 |
| ���ɳ���������/g | 0 | 0 | 1.07 | 2.14 | 5.35 | 5.35 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
| ʱ��/min | 0 | 3 | 6 | 9 |
| ��п����Һ������/g | 150.4 | 150.2 | 150.0 | 150.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
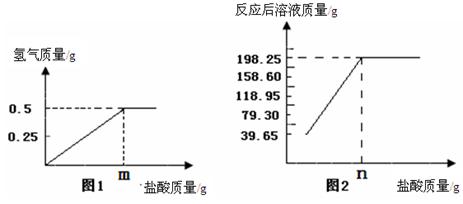

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
| | �� | �� | �� |
| ����NaOH��Һ��������g�� | 35.0 | 40.0 | 45.0 |
| ��Ӧ�õ�������������g�� | 2.5 | 2.9 | 2.9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
| ���� | 1 | 2 | 3 | 4 |
| ����Ca(OH)2��Һ������/�� | 100 | 100 | 100 | 100 |
| �ձ������ɳ���������/�� | 1 | m | 3 | 3 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com