
| A. | 电解水制取氢气 | B. | 用锌粒和盐酸制取氢气 | ||
| C. | 2M+N→2P+Q 2P+M→Q | D. | 用硫酸铜和氢氧化钠制取氢氧化铜 |
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧气化学性质比较活泼,能燃烧 | |
| B. | 氮气的化学性质不活泼,可在食品包装时充入防腐 | |
| C. | 稀有气体不与其他物质发生反应 | |
| D. | 二氧化碳是一种气体污染物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
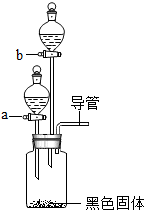 不少家庭养观赏鱼,有时会在鱼缸里放点“鱼浮灵”,可使水中的含氧量迅速增加.请你和小欣同学一起完成这项探究活动.
不少家庭养观赏鱼,有时会在鱼缸里放点“鱼浮灵”,可使水中的含氧量迅速增加.请你和小欣同学一起完成这项探究活动.| 实验 | 主要操作步骤 | 主要实验现象 | 结论 |
| ① | 在集气瓶中加入少量二氧化锰(黑色固体),在仪器a中加入新配制的“鱼浮灵”的饱和水溶液;打开仪器a的活塞,放出适量溶液后,在导管口放一根带火星的木条 | 有气泡逸出,能使带火星木条复燃 | “鱼浮灵”溶于水生成过氧化氢 |
| ② | 关闭仪器a,在仪器b中加入稀盐酸,打开活塞,放出适量溶液后,在导管口放一燃着的木条 | 生成大量无色气泡,木条熄灭 | “鱼浮灵”溶于水生成碳酸钠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com