
著名的科学家诺贝尔经过长期的试验,研制出安全炸药。炸药三硝酸甘油酯(C3H5N3O9)发生爆炸的化学方程式:4C3H5N3O9  12CO2↑+ 10H2O↑+ 6X↑+ O2↑
12CO2↑+ 10H2O↑+ 6X↑+ O2↑
(1)推断X的化学式为____。
(2)若生成13.2 g二氧化碳,则同时生成氧气和水的质量分别是多少?
(1) N2 (2) 0.8g 4.5g
解析试题分析:(1)质量守恒定律微观解释:在化学反应前后,各原子的种类、数目、质量均保持不变(原子的“三不变”),即化学反应前后C、H、N、O的原子个数不变,可推出X的化学式为:N2
(2)化学方程式表示各物质间的质量比(质量比=各物质的相对分子质量×各化学式前面的系数的积的比),即根据化学方程式中二氧化碳、氧气、水之间的质量关系,再根据二氧化碳的质量,可算出氧气和水的质量
解:设生成氧气质量为x,水的质量为y
4C3H5N3O9  12CO2↑+ 10H2O↑+ 6 N2↑+ O2↑
12CO2↑+ 10H2O↑+ 6 N2↑+ O2↑
528 180 32
13.2g y x
528:180=13.2g:y y=4.5g
528:32=13.2g:x x=0.8g
答:生成氧气质量为0.8g,生成水的质量为4.5g
考点:质量守恒定律微观解释,根据化学方程式的计算


科目:初中化学 来源: 题型:计算题
为了测定碳酸钠样品(内含有氯化钠)的纯度,现将10克样品加入重为5克的烧杯中,再往烧杯中加入40克水搅拌至固体完全溶解,再向烧杯中加入50克稀盐酸,恰好不再产生气泡,称得烧杯总质量为102.8克。
请完成下列计算:
(1)反应产生的气体的质量是多少?
(2)碳酸钠样品中碳酸钠的质量分数是多少?
(3)盐酸溶液中溶质的质量分数是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
为检查某石灰石样品中碳酸钙的纯度,取该样品24g放入烧杯中,再向烧杯中加入70g稀盐酸,恰好完全反应(杂质不参加反应),反应后烧杯中剩余固体物质共85.2g,
(1)反应生成CO2的质量为 g;
(2)石灰石样品中碳酸钙的质量。
(3)石灰石样品中碳酸钙的质量分数
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
取氯酸钾和二氧化锰的混合物12克制取氧气,加热一段时间后,测得50%的氯酸钾分解,将剩余的固体冷却后称量,其质量为10.08克,求原混合物中氯酸钾和二氧化锰各多少克?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
乙炔(C2H2)是一种重要的化工原料,实验室常用碳化钙(CaC2)与水反应制取乙炔,该反应方程式为:CaC2 + 2H2O =Ca(OH)2 + C2H2↑。计算:要制取52g乙炔气体,需要碳化钙的质量。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
请根据下图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),回答下列问题: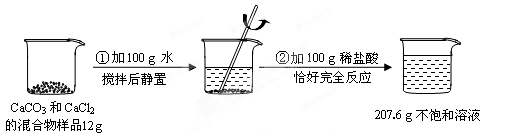
(1)实验过程中产生的CO2气体的质量为 g
(2)计算实验所用稀盐酸的溶质的质量分数(写出计算过程)。
(3)计算配制的CaCl2不饱和溶液中溶质的质量分数(写出计算过程,结果保留一位小数)。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
我国是世界钢铁产量最大的国家,炼铁的主要原料是铁矿石。
(1)用赤铁矿石(主要成分为Fe2O3)炼铁的反应原理为:
(2)Fe2O3中铁元素的质量分数为:
(3)根据化学方程式计算:用含Fe2O360%的赤铁矿石800 t,理论上可炼出纯铁多少吨?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
将铜和氧化铜固体混合物粉末11.2g放入烧杯中,当加入稀硫酸100 g时,氧化铜与硫酸恰好完全反应.过滤后所得溶液的质量为108g,(不考虑过滤过程中溶液的质量损失).
(1)混合物中铜元素的质量分数为 (计算结果保留到0.1%)
(2)求稀硫酸中H2SO4的质量分数.(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某同学将15.0g碳酸钙粉末置于250mL、87.0g的烧杯中,向其中加入105.4g某浓度的稀盐酸,充分反应后,称得烧杯及其剩余物的总质量为203.0g。则:
(1)反应生成的二氧化碳的质量为________________g;(1分)
(2)烧杯内各物质的名称分别为_________ __________;(2分)
(3)列式计算所得溶液的溶质质量分数。(3分)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com