
 向100mL稀盐酸中加入混合均匀的NaHCO3和KHCO3固体粉末.充分反应后使气体完全放出.如图是加入粉末的质量与产生的二氧化碳的关系图
向100mL稀盐酸中加入混合均匀的NaHCO3和KHCO3固体粉末.充分反应后使气体完全放出.如图是加入粉末的质量与产生的二氧化碳的关系图分析 (1)由图示可知,生成气体的质量为22g,然后根据HCl的相对分子质量与二氧化碳的相对分子质量和生成的二氧化碳的质量,列出比例式,即可计算出该盐酸中HCl的质量;
(2)由图示可知,完全反应时加入粉末的质量为45g,根据(1)中生成气体的质量即可设计出此时产生CO2的质量;
(3)根据图示盐酸体积与(3)中盐酸体积的比,得出粉末的取值范围,即可得出粉末质量x(g)与产生CO2质量y(g)之间的关系.
解答 解:(1)由图示可知,m(CO2)=22g;根据NaHCO3和KHCO3与盐酸反应的方程式可知,盐酸与二氧化碳的关系式为HCl~CO2
设盐酸中HCl的质量为x.
HCl~CO2
36.5 44
x 22g
∴$\frac{36.5}{x}=\frac{44}{22g}$
解之得:x=18.25g;
(2)∵$\frac{120mL}{100mL}$<$\frac{58.5g}{45g}$,
∴m(CO2)=22g×1.2=26.4g,
或者这样理解,100mL恰好与45g固体粉末反应,那么120mL只能与$\frac{120×45g}{100}$=54g固体粉末反应,
故58.5g粉末过量,120mL盐酸完全反应,即m(CO2)=22g×1.2=26.4g,
(3)恰好反应时混合物的质量:m(粉末)=45g×1.4=63g,(因为盐酸是原来的1.4倍)
若x≤63 g,由于是反应物的物质的量与生成的气体的物质的量,(混合物的平均相对分子质量根据上一问可知是90,而此时盐酸有剩余,所以按照固体物质的物质的量求算)则y=$\frac{x}{90}$,
若x>63 g,(此时盐酸完全反应,不能继续生成气体,也可以说继续加入的物质的质量无关).则y=22g×1.4=30.8g,
故答案为:(1)该盐酸中HCl的质量为18.25 g.(2)产生CO2的体积为26.4g.
(3)若x≤63 g,y=$\frac{x}{90}$;若x>63 g,y=30.8g.
点评 本题主要考查学生运用化学方程式和已知数据进行推断的能力,解答本题要注意分析物质之间是否恰好完全反应,如果不是恰好完全反应,要以不过量的物质为基础进行计算.


科目:初中化学 来源: 题型:解答题
 人类的生产生活离不开金属材料,随着科技水平的不断提高,金属及其合金在日常生活中扮演着越来越重要的角色.
人类的生产生活离不开金属材料,随着科技水平的不断提高,金属及其合金在日常生活中扮演着越来越重要的角色.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO | 只有CO2 | 含有CO和CO2 |
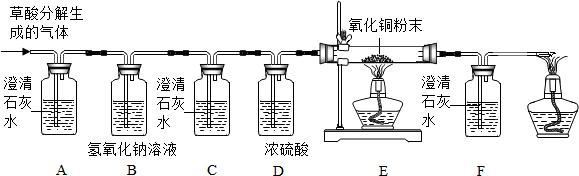
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某厂排放的废水含有碳酸钠和氢氧化钠.技术员为该厂设计处理和利用方案,进行了如下实验:取过滤后的废水样品200g于烧杯中逐滴加入溶质质量分数为7.3%的稀盐酸,不断搅拌至好恰好不再产生气泡为止.测得反应产生的气体与加入稀盐酸质量关系曲线如图所示(反应生成的气体全部逸出).请回答下列问题:
某厂排放的废水含有碳酸钠和氢氧化钠.技术员为该厂设计处理和利用方案,进行了如下实验:取过滤后的废水样品200g于烧杯中逐滴加入溶质质量分数为7.3%的稀盐酸,不断搅拌至好恰好不再产生气泡为止.测得反应产生的气体与加入稀盐酸质量关系曲线如图所示(反应生成的气体全部逸出).请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 过滤能除去天然水中所有的杂质 | |
| B. | 水是由氢气和氧气组成的混合物 | |
| C. | 自来水厂净水过程中所采用的方法包括:沉降、过滤、吸附、消毒 | |
| D. | 长期饮用纯净水有益身体健康 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.
如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| 把钯浸入硝酸银溶液中 | 无明显现象 | 钯的活动性比银弱 |
| 把铂浸入氯化钯溶液中 | 无明显现象 | 钯的活动性比铂强 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 煤、石油、乙醇是三种重要的化石燃料 | |
| B. | 全力开采化石燃料用于居民供暖 | |
| C. | 图书档案着火宜用水基型灭火器扑灭 | |
| D. | 室内着火时不要急于打开门窗 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com