
| 106 |
| x |
| 117 |
| y |
| 44 |
| 8.8g |
| 21.2g |
| 23.2g |
| 25.4g |
| 100.0g |


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:初中化学 来源: 题型:
| A、它们属于不同种元素 |
| B、三种原子的质量相等 |
| C、它们的核外电子数不同 |
| D、不管含碳物质中到底含哪种碳原子,它们统称为碳元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、蜡烛是无色、无味、透明的固体,不溶于水 |
| B、蜡烛浮于水面,说明它的密度比水小 |
| C、蜡烛在空气中燃烧有明亮的火焰,稍有黑烟,放出热量 |
| D、用指甲在蜡烛的表面轻轻一划,能出现纹迹,说明蜡烛的硬度较小 |
查看答案和解析>>
科目:初中化学 来源: 题型:
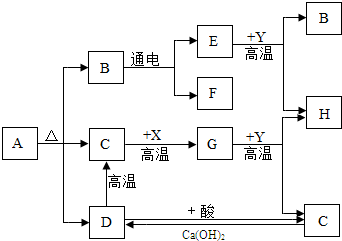 图中A、B、C、D、E、F、G、H分别代表相关反应的一种物质.已知:X、H为黑色固体单质,D是大理石的主要成分,Y为红棕色粉末.常温下C、E、F、G均为无色气体,图中有部分生成物未标出.请填写以下空白:
图中A、B、C、D、E、F、G、H分别代表相关反应的一种物质.已知:X、H为黑色固体单质,D是大理石的主要成分,Y为红棕色粉末.常温下C、E、F、G均为无色气体,图中有部分生成物未标出.请填写以下空白:| 高温 |
| Ca(OH)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验 | 1 | 2 | 3 | 4 |
| 加入样品的质量/g | 10 | 20 | 30 | 40 |
| 生成氢气的质量/g | 0.1 | 0.2 | 0.25 | m |
查看答案和解析>>
科目:初中化学 来源: 题型:
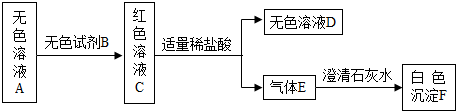
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验序号 | ① | ② | ③ | ④ | ⑤ |
| 所用酒精的体积分数 | 95% | 65% | 55% | 15% | 5% |
| 实验现象 | 酒精烧完,棉布烧坏 | 酒精烧完,棉布无损 | 酒精烧完,棉布无损 | 不燃烧 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com