
【题目】白钨矿的主要成分是CaWO4,工业生产钨流程如下: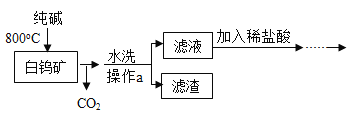
(1)水洗后,进行分离操作的名称是______,其中玻璃棒作用是______。
(2)白钨矿反应前需要进行粉碎,其目的是______。
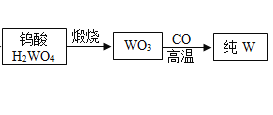
(3)写出生成纯钨的化学方程式是______,写出金属钨的一种用途______。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
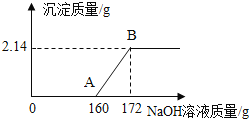
【题目】某NaCl样品中混有杂质MgCl2,为了测定样品中MgCl2的质量分数。取固体样品50.0g完全溶解于水中,并向其中逐渐加入NaOH溶液,实验过程中生成沉淀的质量与加入NaOH溶液的质量的关系如下图所示:
注:发生反应的化学方程式为MgCl2+2NaOH==Mg(OH)2↓+2NaCl
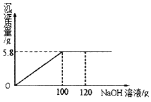
请根据相关信息完成下列计算:
(1)反应完全时生成氢氧化镁的质量_______g。
(2)样品中氯化镁的质量分数。_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学活动小组探究金属的反应规律。
(探究一)在室温条件下进行如图所示实验。
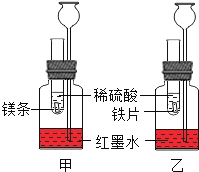
(1)已知:试管内的镁条和铁片表面均被打磨洁净,且形状、大小相同;同时加入等质量和等质量分数的稀硫酸,甲中反应方程式为___.
(2)若比较镁和铁的金属活动性,观察到的现象是___.
(3)若比较相同时间内镁、铁与稀硫酸反应放出热量的多少,长颈漏斗中的现象是___.
(4)若实验所用的金属均过量,则甲装置中产生的H2的质量___(填“大于”、“小于”或“等于”)乙装置中产生的H2质量。
(5)(探究二)在硫酸铜和硫酸亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,没有气泡产生。下列判断正确的是___.
A 滤出的固体中一定含有铜
B 滤出的固体可能含有铁和镁
C 滤液中可能含有硫酸铜
D 滤液中一定含有硫酸镁和硫酸亚铁。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】中国芯彰显中国“智”造,芯片的基材主要是高纯硅(Si),下图是某种制备高纯硅的工艺流程图:
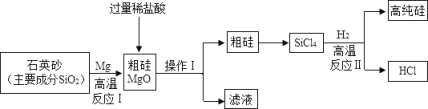
(1)地壳中硅元素的含量比铝_____(填“高”或“低”),二氧化硅中硅元素化合价为_____。
(2)反应Ⅱ的化学方程式为____,该反应要在无氧环境中进行,原因是______(答出一种即可)。
(3)操作Ⅰ的名称是_____,所得粗硅应充分洗涤,以除去表面可能含有的盐酸、_____(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学反应的微观示意图如图,根据该图得出的结论,正确的是______

A 该反应属于置换反应
B 乙中元素的化合价反应前后不变
C 化学反应前后,原子种类、数目保持不变
D 生成的丙和丁的分子个数比为______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业盐酸中通常溶有少量的FeCl3而呈黄色,小红为测定某工业盐酸中HCl的含量进行如下实验:取某工业盐酸100g,滴加一定溶质质量分数的NaOH溶液,测得加入NaOH溶液的质量与反应生成的沉淀质量关系如图所示,FeCl3与NaOH反应的化学方程式为FeCl3+3NaOH═Fe(OH)3↓+3NaCl.请回答下列问题。
(1)A点时,溶液中的溶质是______。
(2)该工业盐酸中HCl的质量分数是多少?_____(写出计算过程)
(3)取100g该工业盐酸稀释成溶质质量分数为10%的稀盐酸,需加水______g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】正常雨水因溶解了少量二氧化碳,pH为5.6,化石燃料燃烧可能产生![]() ,最终导致降雨的酸性增强,下图是形成酸雨的其中一条途径:
,最终导致降雨的酸性增强,下图是形成酸雨的其中一条途径:

(1)我们把pH_____5.6(填“>”“<”或“=”)的降雨称为酸雨。
(2)以上途径的各物质中,硫元素的化合价有_______种。
(3)为减少酸雨危害,下列措施合理的有_________(填序号)
①减少汽车尾气排放 ②禁止使用化石燃料
③将燃煤锅炉烟囱加高 ④开发风能、太阳能等新能源
(4)可用氢氧化钠溶液吸收二氧化硫,其化学方程式为______________________。
(5)![]() 通入碘水(
通入碘水(![]() 的水溶液)会生成硫酸和氢碘酸(HI),我们可利用此原理来测定空气中
的水溶液)会生成硫酸和氢碘酸(HI),我们可利用此原理来测定空气中![]() 的含量,该原理的化学方程式为___________________。
的含量,该原理的化学方程式为___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了除去铜粉样品中混有的铁粉,并用提纯的铜粉制取胆矾(CuSO4.5H2O 相对分子质量250)同时制取FeCl3溶液来制作印刷线路板。某校初三学霸小组的同学按如下流程进行实验:(反应中部分生成物已略去)
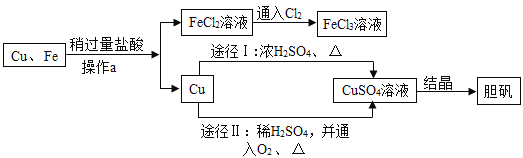
已知: ![]() 回答下列有关问题:
回答下列有关问题:
(1)操作a的名称是_____。
(2)从环保、节约的角度来看由Cu制CuSO4溶液的途径中_____(填“ I”与“II”)更优秀。
(3) FeCl3溶液可腐蚀铜以制作印刷线路板,反应只生成两种常见的盐,则该反应的化学方程式为_____。(已知:产物中金属元素均显正二价)
(4)学霸小组称取了10g样品进行实验,最终得到胆矾25g,请计算原样品中铜粉的质量分数为_____。(忽略实验过程中的消耗)。
(5)总结反思:直接比较铜和铁的活动性强弱实验时,应选择的药品为适量的_____(填序号)。
①铜、铁和稀盐酸
②铜和氯化铁
③铜和氯化亚铁
④铁和硫酸铜
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙是初中化学常见的三种物质,其相互转化关系如图,通常甲为固态单质,乙、丙为两种气体,且所含元素种类相同,乙易与血液中的血红蛋白结合。下列说法错误的是( )

A.丙能产生温室效应
B.③的转化只能通过和氧气反应来实现
C.乙和丙化学性质不同是由于其分子构成不同
D.①②④三个转化的反应中有一种相同的反应物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com