
(7分)某同学做了如下实验: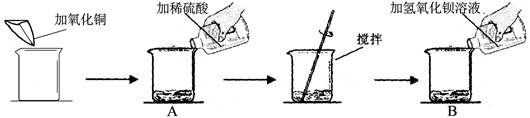
实验数据及部分实验现象如下表:
| | 第一次[来源:学.科.网Z.X.X.K] | 第二次 |
| 加氧化铜的质量(g) | m | m |
| 加稀硫酸的质量(g) | 50 | 100 |
| 加氢氧化钡溶液的质量(g) | 100 | 100 |
| B中主要现象 | 淡蓝色沉淀 | ? |
(1) CuO + H2SO4 = CuSO4 + H2O Ba(OH)2 +CuSO4 =Cu(OH)2↓ + BaSO4↓
(2)产生白色沉淀(蓝色溶液变浅) (3) 4
(4) 171/233=8.55g/X (5)5% (6)135g
解析试题分析:(1)第一次试验是在氧化铜中加入稀硫酸,发生反应生成硫酸铜蓝色溶液,化学反应方程式为 :CuO + H2SO4 = CuSO4 + H2O,生成的硫酸铜溶液继续与氢氧化钡溶液反应,化学反应方程式为 :Ba(OH)2 +CuSO4 =Cu(OH)2↓ + BaSO4↓
(2)由于第一次试验每一步均恰好完全反应,所以第二次实验加入 100g稀硫酸,说明过量,所以第二次实验B中的主要现象是产生白色沉淀(蓝色溶液变浅)
(3)根据化学反应:CuO + H2SO4 = CuSO4 + H2O和Ba(OH)2 +CuSO4 =Cu(OH)2↓ + BaSO4↓,可以看出CuO与Ba(OH)2的质量关系80:171,而氢氧化钡的质量=100g×8.55%=8.55g,所以不难算出CuO的质量m=4g
(4)第二次反应发生的方程式为:Ba(OH)2+H2SO4==BaSO4↓+2H2O根据Ba(OH)2与BaSO4的质量关系为171:233,而Ba(OH)2的质量为100g×8.55%=8.55g,所以可设BaSO4的质量为x,故可列式为:171/233=8.55g/X
(5)第二次反应后的滤液是加入了100g稀硫酸反应得到的溶液 ,根据第一次反应的质量关系,CuO + H2SO4 = CuSO4 + H2O,可计算出溶质CuSO4的质量为 8g,而根据方程式:Ba(OH)2+H2SO4==BaSO4↓+2H2O,可算出BaSO4的质量=11.65g,故溶液质量=4g+100g+100g-11.65g=192.35g,,所以将第二次反应后的滤液蒸发32.35克水,此时溶液的质量变为=192.35-32.35g=160g,则所得不饱和溶液中溶质的质量分数=8g/160g×100%=5%
(6)根据反应CuO + H2SO4 = CuSO4 + H2O中CuO与H2SO4的质量关系为80:98,CuO的质量m=4g,所以H2SO4的质量=4.9g,所以H2SO4的质量分数=4.9g/50g×100%=9.8%,所消耗的稀硫酸总质量为150g,所以根据稀释前后的溶质质量不变,可设98%的浓硫酸质量为 x,可列式为 :98%×x=150g×9.8%,所以x=15g,故水的质量=150g-15g=135g
考点:化学反应方程式的书写,根据化学反应方程式计算,溶液的稀释


科目:初中化学 来源: 题型:单选题
实验室存有一定量的溶质质量分数为5%的氢氧化钠溶液,加热蒸发掉108g水后,所得溶液的溶质质量分数变为20%。
求:(1)原氢氧化钠溶液的质量是多少克?
(2)原氢氧化钠溶液中含有溶质多少克?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(11分)煤、石油和天然气等化石燃料是目前人类使用的最主要燃料,也是重要的化工原料。
(1)石油中主要含有 两种元素(填写元素符号);天然气的主要成分是 (填写化学式)。
(2)化石燃料属于 (选填“可再生”或“不可再生”)能源,其燃烧排放的大量二氧化碳会引起全球气候变暖。一种新的处理方法是将二氧化碳气体通入含有长石(地壳中最常见的矿石,含量高达60%)成分的水溶液里,其中一种反应的化学方程式: KAlSi3O8+CO2+2H2O==KHCO3+X+3SiO2↓,则X的化学式为 。
(3)工业上,煤炭燃烧前进行粉碎的目的是 。煤隔绝空气加强热得到的焦炭,是冶铁的重要原料。为了测定某赤铁矿中氧化铁的质量分数,化学兴趣小组的同学设计了两种实验方案(假设该赤铁矿中的杂质既不溶于水,也不发生反应)。
方案I 取8.00g赤铁矿粉,加入足量稀硫酸,完全反应后过滤,得到1.60g滤渣。则赤铁矿粉中氧化铁的质量分数为 。
方案Ⅱ 如图所示,取8.00g赤铁矿粉与过量的焦炭粉混合后加强热,充分反应。测得氢氧化钠溶液反应前后质量增加了1.32g。如果产生的二氧化碳被氢氧化钠溶液完全吸收,根据所学反应3C+2Fe2O3△4Fe+3CO2↑计算,赤铁矿粉中氧化铁的质量分数为 。
[实验反思]方案Ⅱ中硬质玻璃管内原有的空气对实验结果有影响,这会导致测出的氧化铁的质量分数 (选填“偏大”、“偏小”或“不变”)。
[实验分析]方案I测出的氧化铁的质量分数明显大于方案Ⅱ测出的结果,可能的原因是 (写出一种即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某品牌纯碱中含有杂质NaCl,化学兴趣小组的同学进行了如下实验探究:称取12g样品放入烧杯中,加入稀盐酸至不再产生气泡为止,并绘制出加入稀盐酸的质量与放出气体质量的关系如图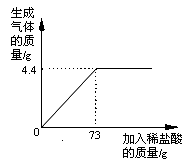
(1)纯碱恰好完全反应时,生成CO2的质量为 g
(2)计算该样品中含杂质的质量分数是多少?(计算结果保留一位小数,下同)
(3)计算当盐酸与纯碱恰好完全反应时,所得溶液的溶质质量分数是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(12分)某氢氧化钙中含有碳酸钙杂质,称取研细的该样品12.4g放入锥形瓶中,加入32.6g水,充分振荡形成悬浊液,再向锥形瓶中逐滴滴加盐酸使其充分反应至无气泡产生,测得加入盐酸的质量与锥形瓶中物质的质量关系如下表所示.
| 加入盐酸的质量/g | 0 | 25 | 37.5 |
| 锥形瓶中物质的质量/g | 45 | 70 | 80.3 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(6分)称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题: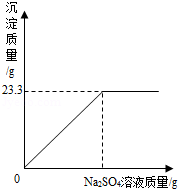
(1)完全反应后生成BaSO4沉淀 g.
(2)恰好完全反应时消耗Na2SO4溶液的质量是多少克?
(3)恰好完全反应时所得溶液中溶质的质量分数是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(7分)在一烧杯中盛有60.2gBaCO3和BaCl2的粉末状混合物,向其中加入188.8g水使混合物中可溶物完全溶解,然后向其中逐滴加入溶质质量分数为10%的稀盐酸至146g时恰好反应完全,请根据题意回答问题:
(1)在滴加盐酸过程中观察到的明显实验现象是 。
(2)当盐酸滴加至140g时,烧杯中溶液里含有溶质的是 。(写化学式)
(3)计算恰好反应完全时烧杯中所得不饱和溶液的质量。(结果精确到0.1g)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(3分)硫代硫酸钠(Na2S2O3)是一种用途广泛的物质。某硫代硫酸钠样品中含有少量的硫酸钠。现取16 g该样品放入烧杯中,加入113.6 g一定溶质质量分数的稀硫酸恰好完全反应,得到120 g硫酸钠不饱和溶液。
发生反应的化学方程式为:Na2S2O3 + H2SO4=== Na2SO4 + H2O + S↓+ SO2↑
请计算:
(1)样品中硫代硫酸钠(Na2S2O3)与硫酸钠的质量比。
(2)所得溶液中溶质质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com