
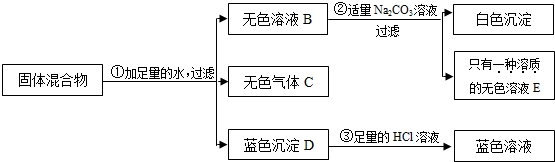
分析 根据题中所给的五种物质两两之间反应会生成气体的,只能是氧化钙和水反应生成氢氧化钙,氢氧化钙和氯化铵反应生成氨气,则白色固体A中一定存在氧化钙和氯化铵,氢氧化钙和氯化铵反应生成氯化钙、水和氨气,所以C是氨气,氨气的水溶液显碱性,无色溶液B中含有氯化钙,C和碳酸钠反应除了生成白色沉淀,生成的无色溶液只有一种溶质,所以固体A中没有硝酸铜,有没有氯化钙对实验现象不会造成影响;蓝色沉淀D和足量稀盐酸反应生成蓝色溶液,所以D是氢氧化铜沉淀,因此固体A中也一定含有二价铜的化合物,但是然后将推出的混合物中的各种物质代入题中进行检验即可.
解答 解:题中所给的五种物质两两之间反应会生成气体的,只能是氧化钙和水反应生成氢氧化钙,氢氧化钙和氯化铵反应生成氨气,则白色固体A中一定存在氧化钙和氯化铵,氢氧化钙和氯化铵反应生成氯化钙、水和氨气,所以C是氨气,氨气的水溶液显碱性,无色溶液B中含有氯化钙,C和碳酸钠反应除了生成白色沉淀,生成的无色溶液只有一种溶质,所以固体A中没有硝酸铜,有没有氯化钙对实验现象不会造成影响;蓝色沉淀D和足量稀盐酸反应生成蓝色溶液,所以D是氢氧化铜沉淀,因此固体A中也一定含有二价铜的化合物,即一定含有氯化铜,带入验证符合转化关系,因此:
(1)依据上面的推导可知氨气的水溶液显碱性,所以氨气能使湿润的红色石蕊试纸变蓝色,所以现象是:试纸变蓝;故填:蓝;
(2)滤渣D是蓝色的氢氧化铜沉淀,故填:Cu(OH)2;
(3)根据推断可知一定含有氯化铵、氯化铜和氧化钙,可能含有氯化钙,一定没有硝酸铜;故填:NH4C1、CuCl2、CaO;
(4)氯化铵和氢氧化钙反应生成了氯化钙、水和氨气,所以滤液B一定大量存在的酸根离子是:Cl-;故填:Cl-;
(5)盐酸与氢氧化铜反应生成氯化铜和水,反应的化学方程式为:Cu(OH)2+2HCl═CuCl2+2H2O;故填:Cu(OH)2+2HCl═CuCl2+2H2O;
(6)固体混合物A中可能存在的物质为氯化钙;氢氧化钙和氯化铵会生成氯化钙,所以固体A中有没有氯化钙,不会影响无色溶液C和碳酸钠的反应现象,所以固体A中可能存在的物质是:CaCl2,原因是:因为NH4Cl与CaO一定存在,CaO与H2O反应生成Ca(OH)2,Ca(OH)2与NH4Cl反应,在滤液C中一定能产生CaCl2,故原混合物是否含有CaCl2无法确定;故填:CaCl2,因为NH4Cl与CaO一定存在,CaO与H2O反应生成Ca(OH)2,Ca(OH)2与NH4Cl反应,在滤液C中一定能产生CaCl2,故原混合物是否含有CaCl2无法确定.
点评 在接此类题时,首先分析题中所给物质的性质以及两两之间的反应,然后结合题中的现象确定各物质的存在性,最后将各物质代入转化关系中验证即可.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | (m-n) g | B. | (m+2-n) g | C. | (m+2+n) g | D. | (n-2)g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
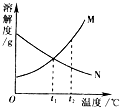 如图表示M、N两种不含结晶水的固体物质的溶解度曲线.根据图示判断,下列说法中,正确的是②
如图表示M、N两种不含结晶水的固体物质的溶解度曲线.根据图示判断,下列说法中,正确的是②查看答案和解析>>
科目:初中化学 来源: 题型:解答题
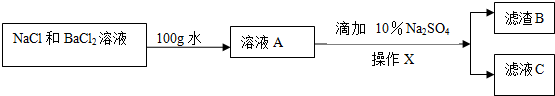
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 40g | B. | 70g | C. | 80g | D. | 140g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 试管朝向 |  |  |  |  |
| 实验项目 | A.加热高锰酸钾制氧气 | B.向试管中加入粉末状药品的初始阶段 | C.排空气法收集氧气 | D.给液体加热 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com