
【题目】中国是全球抗生素滥用最严重的国家之一,需引起我们重视。 环丙沙星是常用的一种抗生素,其说明书中部分内容如图。

(1)环丙沙星属于____(填“有机”或“无机”)化合物。
(2)环丙沙星分子中碳、氢、氧的原子个数比为____。
(3)环丙沙星中氟元素的质量分数为____(结果精确到 0.1%)。
(4)患者一个疗程共服用了____片环丙沙星片。
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】如图所示,将滴有酚酞试液的滤纸条放在试管中,试管口塞上一团脱脂棉。
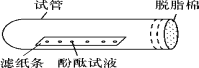
(1)用仪器A吸取浓氨水,滴在脱脂棉上(10~15滴)。A的名称是:_____
(2)实验中,观察到的现象是_____,这说明了_____
(3)实验中,往往在试管下放一张白纸,白纸的作用是_____。
(4)某同学做此实验时,发现滤纸条上没有变色,而试管中所塞的脱脂棉却变成了红色。导致这种现象产生的错误操作可能是_____,这一实验还说明,两种试剂中_____具有挥发性。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属钛被用于航空航天工业、化工、医疗等领域。用钛铁矿(主要成份FeTiO3)制取钛并获得副产品A的主要工艺流程如下:(反应①②均为分解反应)
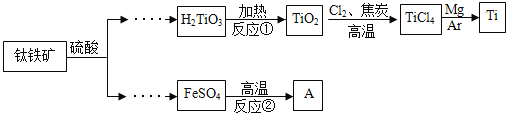
(1)反应①生成了两种氧化物,化学方程式为________。
(2)TiO2与焦炭和Cl2在高温下反应,该反应中C和Cl2按质量比为12: 71的比例参加反应,相应的化学方程式为__________。
(3)反应②产物除红色固体A外,还有两种组成元素相同且相对分子质量相差16的气体,化学方程式为__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用下图所示装置进行实验,研究燃烧的条件。已知:白磷的着火点为40℃,红磷的着火点为240℃。
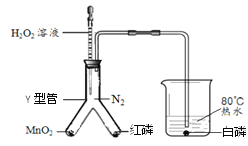
(1)当H2O2溶液与MnO2接触时,发生反应的化学方程式为________。
(2)检查上述装置气密性的实验方案是________。
(3)向Y型管中挤入H2O2溶液后,观察到导管口开始产生气泡时,烧杯中白磷不燃烧;一段时间后,白磷燃烧,此现象能够证明的可燃物燃烧的条件是________;若证明可燃物燃烧的另一个条件,依据的现象是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有 H2SO4 与 CuSO4 的混合溶液,为了分析混合溶液中 H2SO4与 CuSO4 的质量分数,设计了如图 1 实验方案:
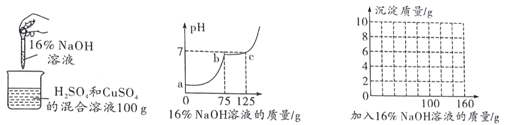
图1 图2
(1)根据图 1 坐标,推测 CuSO4 溶液呈________(填“酸”、“碱”、“中”) 性;C 点溶液中的溶质为_______(写化学式)。
(2)请计算该混合溶液中的CuSO4 的溶质质量分数_________。
(3)若在100g 混合溶液中不断加入上述氢氧化钠溶液,请你在图 2 中画出加入氢氧化钠溶液的质量与产生沉淀的质量的关系图________。
(4)根据该方案的实验现象就能证明硫酸和氢氧化钠发生了中和反应的原因是____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学学科实践活动课上,老师拿来一包粉末。它是由长期放置在空气中的铁粉和久置的碱石灰干燥剂混合而成,让同学们设计实验进行探究。
(提出问题)固体样品的成分是什么?
(查阅资料)(1)碱石灰干燥剂是CaO和NaOH的混合物。(2)CaCl2溶液显中性。
(猜想与假设)固体样品中可能含有 Fe、Fe2O3、CaO、NaOH、Ca(OH)2、Na2CO3和_____等七种物质。
(进行实验)
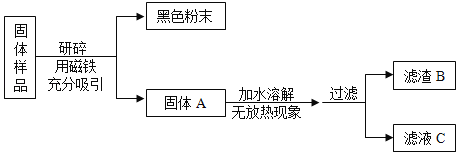
甲组同学对滤渣B的成分进行探究,记录如下:
实验操作 | 实验现象 | 实验结论及化学方程式 |
取少量滤渣B于试管中,加入足量稀盐酸,将生成的气体通入澄清的石灰水中 | ①_______________ ②_______________ | 结论:滤渣B中有 Fe2O3,CaCO3。 实验操作中Fe2O3与稀盐酸反应的化学方程式为:____________________ |
乙组同学对滤液C的成分进行探究,记录如下:
实验操作 | 实验现象 | 实验结论及化学方程式 |
取少量滤液C于试管中,加入过量CaCl2溶液,静置,向上层清液中滴加无色酚酞试液,振荡 | ①有白色沉淀生成 ②酚酞试液由无色变成红色 | 滤液C中有__________; 滤液C中的物质与CaCl2反应的化学方程式是_________________ |
(解释与结论)(1)乙组同学实验中加入过量CaCl2溶液的目的是________________________
(2)通过以上实验探究,该固体样品中能确定一定含有的成分是___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某市一家大型化工厂处理回收含铜废料的生产流程如图:
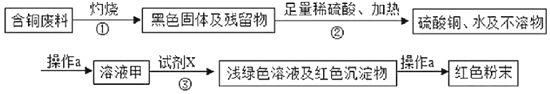
(资料)过程①得到的残留物不溶于水和不溶于酸;亚铁离子在空气中易被氧化为铁离子。
回答下列问题:
(1)写出流程①中与铜有关的化学方程式:_____。
(2)操作a的名称是_____,溶液甲呈_____色。
(3)为达到回收铜的目的,流程③中加入的试剂X为_____。
(4)浅绿色溶液放在空气中一段时间后会发生变化,请你对变化产生的现象提出猜想并说明依据:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】肼(N2H4)是一种火箭和喷气发动机的燃料(在空气中燃烧产物只有水和一种气体单质),在空气中易吸收水分形水合肼N2H4H2O,回答下列问题:
(1)肼也称为联氨,若氨的分子结构可表示为![]() ,则肼的分子结构可表示为_____;水合肼中各元素质量比为N:H:O=_____。
,则肼的分子结构可表示为_____;水合肼中各元素质量比为N:H:O=_____。
(2)肼常贮存于带有干燥剂的密封装置中,原因是防止_____;肼作燃料的优点有_____。
A 自然界蕴藏有丰富的肼,容易得到 B 燃烧时发热量高
C 有毒性和腐蚀性 D 燃烧产物无污染
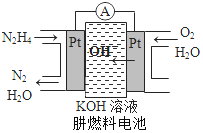
(3)如图是肼燃料电池示意图,电池总反应和肼燃烧一致,则电池总反应方程式为_____,电池工作时将化学能转化为_____能,电池工作时的两个电极反应分别为:A极(O2+2H2O+4e﹣=4OH﹣);B极(N2H4+4OH﹣+4e﹣=4H2O+N2↑),电化学上把反应后物质中元素化合价升高的电极称为负极,反之称为正极,则该电池的正极为_____(A或B)极。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com