
小明在老师的指导下测一瓶稀盐酸的溶质质量分数,具体步骤如下:
步骤一:配制溶质质量分数为1%的氮氧化钠溶液.
步骤二:向20 克待测稀盐酸中逐滴滴入上述氢氧化钠溶液,并使用pH计记录溶液的pH变化情况,绘制图象如图.
(1)在步骤一中需要用到的玻璃仪器有 (写出两种).
(2)已知发生反应的化学方程式为:NaOH 十HCl=NaCl+H2O,请结合图,计算该稀盐酸的溶质质量分数.(结果精确到0.01% )
(3)在往稀盐酸中逐渐滴入氢氧化钠溶液的过程中,当溶液的pH达到2时,溶液中的溶质有 .(用化学式表示)
(1)器玻璃棒、烧杯
(2)0.37%
(3)NaCl、HCl
解析试题分析:(1)溶液配制的步骤:计算、称量和量取、溶解;所以需要的仪器玻璃棒、烧杯、量筒、胶头滴管;故填:器玻璃棒、烧杯;
(2)溶液的pH等于7时恰好完全反应消耗氢氧化钠溶液的质量为8g,
设该稀盐酸的溶质质量分数为x,
NaOH+HCl=NaCl+H2O
40 36.5
8g×1% x×20g
x=0.37%
答:该稀盐酸的溶质质量分数为0.37%;
(3)当溶液的pH达到2时,说明溶液显酸性,盐酸有剩余,所以溶液中的溶质有NaCl、HCl.故填:NaCl、HCl.
考点:根据化学反应方程式的计算;一定溶质质量分数的溶液的配制;有关溶质质量分数的简单计算.
点评:本题是结合题中信息的计算题,考查了根据NaOH+HCl=NaCl+H2O化学方程式的计算题,注意做题时要细心求对相分子质量.


科目:初中化学 来源: 题型:计算题
以下是某研究小组探究影响反应速率部分因素的相关实验数据.
| 实验序号 | 过氧化氢溶液浓度、% | 过氧化氢溶液体积/ml | 温度/C | 二氧化锰的用量/g | 收集氧气的体积/ml | 反应所需的时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 15.05 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 3.03 |
| ③ | 30 | 5 | 35 | | 2 | 48.21 |
| ④ | 30 | 5 | 55 | | 2 | 10.95 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
校化学兴趣小组的同学取60g氯化钙溶液,向其中加入适量碳酸钠溶液,反应完毕后过滤,所得固体用作制取牙膏摩擦剂的主要原料,同时所得滤液用来进行小麦选种(选种液要求氯化钠是质量分数在10%~20%之间)。实验过程中所加碳酸钠溶液的质量与生成碳酸钙沉淀的质量关系如下图所示。通过下图可知,当氯化钙恰好反应完时: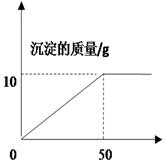
(1)消耗碳酸钠溶液的质量为 g;
(2)请通过计算回答,此时所得氯化钠溶液能否作为小麦选种液?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应制备:Al2O3+N2+3C 2AlN+3CO,若要得到41Kg的氮化铝,则至少需要参加反应的氧化铝(Al2O3)的质量为多少千克?
2AlN+3CO,若要得到41Kg的氮化铝,则至少需要参加反应的氧化铝(Al2O3)的质量为多少千克?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
乙醇是一种清洁的绿色能源,可再生,俗称酒精,其化学式为C2H5OH,其在空气中完全燃烧的化学方程式为:C2H5OH+3O2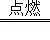 2CO2+3H2O,现有100g质量分数为92%的乙醇溶液在空气中完全燃烧产生二氧化碳的质量为多少克?
2CO2+3H2O,现有100g质量分数为92%的乙醇溶液在空气中完全燃烧产生二氧化碳的质量为多少克?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
湿法冶金是我国古代劳动人民智慧的结晶.若向ag含杂质的铁粉中(假设杂质不溶于水,也不与其他物质反应)加入l60g溶质的质量分数为l0%的硫酸铜溶液,恰好完全反应后,过滤得到6.8g干燥固体,同时得到一种不饱和溶液(滤液损失忽略不计).
请回答下列问题:
(1)写出上述反应的化学方程式 ;
(2)根据硫酸铜质量列出求解样品中铁的质量(x)的比例式 ;
(3)a的数值为 ;
(4)若向反应后的滤液中加入40.8g水,则所得溶液中溶质的质量分数为 ;
(5)工业上若要得到120t上述铁粉,需要含杂质(杂质不含铁元素)20%的赤铁矿的质量是 .
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某同学称取一定质量的铁粉样品(含有少量不与稀硫酸反应的杂质),放入烧杯中,加入98g稀硫酸,恰好完全反应,生成气体的质量与反应时间的关系如图所示,试回答下列问题: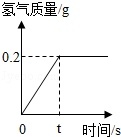
(1)根据图象,恰好完全反应时生成氢气的质量是 g;
(2)样品中铁的质量是多少?稀硫酸的溶质质量分数是多少?(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
化学家TimRichard将分子结构简式像小狗的某有机物(如图所示),取名为“小狗烯”(化学式为C26H26).请计算: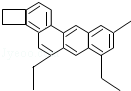
(1)“小狗烯”中碳原子和氢原子的原子个数比 (填最简整数比).
(2)“小狗烯”中碳元素和氢元素的质量比 (填最简整数比)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
为测定锌铜合金中锌的含量,取该合金放入如图 14 盛有稀硫酸的锥形瓶中,发生反应: Zn+H2SO4=ZnSO4+H2↑ 。多次实验后,取平均值所得数据如下表:
| 反应前 | 充分反应后装置及反应剩余物质质量 | |
| 装置和足量的稀硫酸质量 | 锌铜合金质量 | |
| 342.10g | 16.00g | 357.70g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com