
вдЯТЪЧФГбаОПаЁзщЬНОПгАЯьЗДгІЫйТЪВПЗжвђЫиЕФЯрЙиЪЕбщЪ§ОнЃЎ
| ЪЕбщађКХ | Й§бѕЛЏЧтШмвКХЈЖШЁЂ% | Й§бѕЛЏЧтШмвКЬхЛ§/ml | ЮТЖШ/C | ЖўбѕЛЏУЬЕФгУСП/g | ЪеМЏбѕЦјЕФЬхЛ§/ml | ЗДгІЫљашЕФЪБМф/s |
| Ђй | 5 | 1 | 20 | 0.1 | 4 | 15.05 |
| Ђк | 15 | 1 | 20 | 0.1 | 4 | 3.03 |
| Ђл | 30 | 5 | 35 | | 2 | 48.21 |
| Ђм | 30 | 5 | 55 | | 2 | 10.95 |
ЃЈ1ЃЉЙ§бѕЛЏЧтЕФХЈЖШ
ЃЈ2ЃЉЂм ЮТЖШдНИпЗДгІЫйЖШдНПьЃЌЮТЖШдНЕЭЗДгІЫйЖШдНТ§ЃЈ2ЗжЃЉ
ЃЈ3ЃЉ20ЁцЪБ5%Й§бѕЛЏЧтШмвКжаМгШыЩйСПЖўбѕЛЏУЬ
НтЮіЪдЬтЗжЮіЃКЃЈ1ЃЉДгБэжаЗжЮіПЩжЊЃКЂйКЭЂкЪЧЙ§бѕЛЏЧтХЈЖШВЛЭЌЖјЦфЫћЕФЗДгІЪБИїжжСПОљЯрЭЌЃЌПЩжЊетвЛЙ§ГЬЪЧПМВщЗДгІЮяЕФХЈЖШгыЗДгІЫйЖШЕФЙиЯЕЃЌЗДгІЮяХЈЖШдНДѓЃЌЗДгІЫйТЪдНПьЃЛ
ЃЈ2ЃЉЂлКЭЂмдђЪЧЮТЖШВЛЭЌЦфЫћЬѕМўЯрЭЌЃЌУїЯдЪЧЖдЮТЖШгАЯьЛЏбЇЗДгІЫйЖШЕФЬНОПЃЛДгНсЙћПДЮТЖШИпЪБЗДгІЫљгУЕФЪБМфНЯЖЬЃЌМШЗДгІЕФЫйЖШНЯПьЃЌЮТЖШЕЭЪБЗДгІЕФЫйЖШТ§ЃЛ
ЃЈ3ЃЉЪЕбщЪвгУЙ§бѕЛЏЧтжЦШЁбѕЦјвЊЧѓЗДгІМђБувзВйзїЃЌЫљвдВЩгУВЛМгШШЖјМгДпЛЏМСЕФЗНЗЈНјааНЯКЯЪЪЃЌДгвзгкЪеМЏЕФНЧЖШжЊЃЌЗДгІЕФЫйЖШВЛФмЬЋПьвВВЛФмЬЋТ§ЃЌЫљвдзюКЯЪЪЕФЬѕМўЪЧЙ§бѕЛЏЧтШмвКжаМгШыЩйСПЖўбѕЛЏУЬЃЛ
ПМЕуЃКЬНОПЭтНчЬѕМўЖдЛЏбЇЗДгІЫйТЪЕФгАЯь



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃКМЦЫуЬт
ЮЊВтЖЈЪЕбщЪвжаФГЙ§бѕЛЏЧтШмвКЕФШмжЪжЪСПЗжЪ§ЃЌаЁУїШЁ25.0gЙ§бѕЛЏЧтШмвКЗХШыЩеБжаЃЌШЛКѓНјааШчЭМЫљЪОЕФЪЕбщЃЎЧыМЦЫуЃК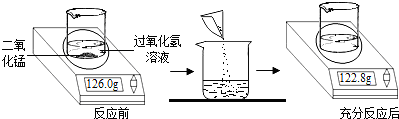
ЃЈ1ЃЉЗДгІКѓВњЩњЦјЬхЕФжЪСПЮЊЁЁ_________ЁЁgЃЎ
ЃЈ2ЃЉДЫЙ§бѕЛЏЧтШмвКЕФШмжЪжЪСПЗжЪ§ЃЎ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃКМЦЫуЬт
дьжНЪЧЮвЙњЙХДњЫФДѓЗЂУїжЎвЛЃЌЫќгааЇЕиЭЦЖЏСЫШЫРрЮФУїЕФЗЂеЙЃЎ
ЃЈ1ЃЉЛиЪеХЉЬяВњЩњЕФНеИбзїЮЊдьжНдСЯЃЌПЩвдМѕЩйЗйЩеНеИбДјРДЕФЛЗОГЮлШОЃЎНеИбЕФжївЊГЩЗжЪЧЯЫЮЌЫи[ЃЈC6H1005ЃЉn]ЃЌЯЫЮЌЫижаCЁЂHЁЂOШ§жждЊЫиЕФжЪСПБШЮЊЁЁ ЁЁЃЈгУзюМђећЪ§БШБэЪОЃЉЃЎ
ЃЈ2ЃЉдьжНЛсВњЩњДѓСПКЌNaOHЕФМюадЗЯЫЎЃЌашОДІРэГЪжаадКѓХХЗХЃЎШєФГдьжНГЇЗЯЫЎжаNaOHЕФжЪСПЗжЪ§ЮЊlЃЎ6%ЃЌЯжгаЗЯСђЫс9.8tЃЈH2SO4ЕФжЪСПЗжЪ§ЮЊ20%ЃЉЃЌПЩвдДІРэЕФЗЯЫЎжЪСПЪЧЖрЩйЃП
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃКМЦЫуЬт
ЁАЙ§ЬМЫсФЦЁБЃЈЛЏбЇЪНПЩБэЪОЮЊ2Na2CO3?3H2O2ЃЉЫзГЦЙЬЬхЫЋбѕЫЎЃЌМЋвзЗжНтЃЌЫќМШгаЬМЫсбЮЕФаджЪЃЌгжгаЫЋбѕЫЎЕФВЛЮШЖЈадКЭбѕЛЏадЃЌЪЧКмКУЕФЯћЖОМСКЭЙЉбѕМСЃЌЙуЗКгІгУгкЯДЕгЁЂгЁШОКЭвНвЉЕШСьгђЃЎЯжНЋвЛЖЈжЪСПЕФЙ§ЬМЫсФЦЗлФЉШмгкmПЫЫЎжаХфГЩЯЁШмвКЃЌдйЯђЦфжаМгШыЪЪСПЖўбѕЛЏУЬЗлФЉЃЌГфЗжЗДгІКѓЩњГЩ4.8gЦјЬхЃЎНЋЗДгІКѓЕФЛьКЯЮяЙ§ТЫЃЌВтЕУТЫвКЕФШмжЪжЪСПЗжЪ§ЮЊ10.6%ЃЌЧѓmЃЎЃЈВЛПМТЧЫ№КФЃЉ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃКМЦЫуЬт
ФГПЮЭтЛюЖЏаЁзщЮЊВтЖЈЕБЕиЪЏЛвЪЏжаКЌЬМЫсИЦЕФжЪСПЗжЪ§ЃЌШЁРДСЫвЛаЉПѓЪЏбљЦЗЃЌВЂШЁЯЁбЮЫс200gЃЌЦНОљЗжГЩ4ЗнЃЌНЋЫФЗнВЛЭЌжЪСПЕФбљЦЗМгШыЕНЫФЗнЯЁбЮЫсжаЃЌНјааЪЕбщЃЌНсЙћШчЯТЃК
| ЪЕбщ | 1 | 2 | 3 | 4 |
| МгШыбљЦЗЕФжЪСП/g | 5 | 10 | 15 | 20 |
| ЩњГЩCO2ЕФжЪСП/g | 1ЃЎ54 | 3ЃЎ08 | 4ЃЎ4 | m |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃКМЦЫуЬт
ЧыИљОнЯТЭМЫљЪОЕФЪЕбщЙ§ГЬКЭЬсЙЉЕФЪ§ОнЃЈВНжшЂкВњЩњЕФЦјЬхШЋВПвнГіЃЉЃЌЛиД№ЯТСаЮЪЬтЃКЃЈCaCl2ШмгкЫЎЃЌЕЋВЛгыЯЁбЮЫсЗДгІЃЉ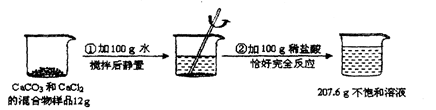
МЦЫудЛьКЯЮябљЦЗжаCaCl2ЕФжЪСПЃЈаДГіМЦЫуЙ§ГЬЃЉЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃКМЦЫуЬт
ЮЊСЫВтЖЈФГЗлФЉзДЛЦЭЃЈЭЁЂаПКЯН№ЃЉбљЦЗжаЭЕФжЪСПЗжЪ§ЃЌБДБДЭЌбЇШЁ10gЛЦЭбљЦЗЗХШыЩеБжаЃЌдйШЁ40gЯЁбЮЫсЗжЫФДЮМгШыЩеБжаЃЌОљГфЗжЗДгІЃЌЪЕбщЪ§ОнШчЯТЃК
| | ЕквЛДЮ | ЕкЖўДЮ | ЕкЖўДЮ | ЕкЫФДЮ |
| МгШыЯЁбЮЫсжЪСПЃЈgЃЉ | 10g | 10g | 10g | 10g |
| ЪЃгрЙЬЬхЕФжЪСПЃЈgЃЉ | 8.7g | 7.4g | 6.1g | 5.45g |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃКМЦЫуЬт
ИљОнКюЕТАёжЦМюЗЈдРэЃЌЪЕбщЪвжЦБИДПМю(Na2CO3)ЕФжївЊВНжшЪЧЃКЃКНЋХфжЦКУЕФБЅКЭNaClШмвКЕЙШыЩеБжаМгШШЃЌПижЦЮТЖШдк30-35ЁцЃЌНСАшЯТЗжХњМгШыбаЯИЕФNH4HCO3ЙЬЬхЃЌМгСЯЭъБЯКѓЃЌМЬајБЃЮТ30ЗжжгЃЌОВжУЁЂЙ§ТЫЕУNaHCO3ОЇЬхЁЃгУЩйСПеєСѓЫЎЯДЕгГ§ШЅдгжЪЃЌОЙ§ДІРэКѓЃЌзЊШыеєЗЂУѓжаЃЌзЦЩе2аЁЪБЃЌЕУNa2CO3ЙЬЬхЁЃ
ЫФжжбЮдкВЛЭЌЮТЖШЯТЕФШмНтЖШЃЈgЃЉБэ
 ЮТЖШ ЮТЖШ ШмНтЖШ бЮ | 0Ёц | 10Ёц | 20Ёц | 30Ёц | 40Ёц | 50Ёц | 60Ёц | 100Ёц |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | Ђй | ЁЊЁЊ | ЁЊЁЊ | ЁЊЁЊ |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | ЁЊЁЊ |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
|
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃКМЦЫуЬт
аЁУїдкРЯЪІЕФжИЕМЯТВтвЛЦПЯЁбЮЫсЕФШмжЪжЪСПЗжЪ§ЃЌОпЬхВНжшШчЯТЃК
ВНжшвЛЃКХфжЦШмжЪжЪСПЗжЪ§ЮЊ1%ЕФЕЊбѕЛЏФЦШмвКЃЎ
ВНжшЖўЃКЯђ20 ПЫД§ВтЯЁбЮЫсжаж№ЕЮЕЮШыЩЯЪіЧтбѕЛЏФЦШмвКЃЌВЂЪЙгУpHМЦМЧТМШмвКЕФpHБфЛЏЧщПіЃЌЛцжЦЭМЯѓШчЭМЃЎ
ЃЈ1ЃЉдкВНжшвЛжаашвЊгУЕНЕФВЃСЇвЧЦїга ЃЈаДГіСНжжЃЉЃЎ
ЃЈ2ЃЉвбжЊЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃКNaOH ЪЎHCl=NaCl+H2OЃЌЧыНсКЯЭМЃЌМЦЫуИУЯЁбЮЫсЕФШмжЪжЪСПЗжЪ§ЃЎЃЈНсЙћОЋШЗЕН0.01% ЃЉ
ЃЈ3ЃЉдкЭљЯЁбЮЫсжаж№НЅЕЮШыЧтбѕЛЏФЦШмвКЕФЙ§ГЬжаЃЌЕБШмвКЕФpHДяЕН2ЪБЃЌШмвКжаЕФШмжЪга ЃЎЃЈгУЛЏбЇЪНБэЪОЃЉ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com