
为了测定某粉末状黄铜(铜、锌合金)样品中铜的质量分数,贝贝同学取10g黄铜样品放入烧杯中,再取40g稀盐酸分四次加入烧杯中,均充分反应,实验数据如下:
| | 第一次 | 第二次 | 第二次 | 第四次 |
| 加入稀盐酸质量(g) | 10g | 10g | 10g | 10g |
| 剩余固体的质量(g) | 8.7g | 7.4g | 6.1g | 5.45g |
(1)16g(2)Zn+2HCl═ZnCl2+H2↑(3)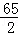 =
= (4)13.6%(5)2725t
(4)13.6%(5)2725t
解析试题分析:(1)根据第一次数据计算,参加反应的锌的质量为:10g﹣8.7g=1.3g,
设10g稀盐酸中氯化氢的质量为X,生成氯化锌的质量为Z,生成氢气的质量为m,
Zn+2HCl═ZnCl2+H2↑,
65 73 136 2
1.3g X Z m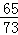 =
=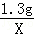 ,
,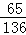 =
= ,
,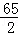 =
=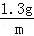 ,
,
X=1.46g,Z=2.72g,m=0.04g,
稀盐酸的质量分数为: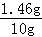 ×100%=14.6%,
×100%=14.6%,
设需浓盐酸的质量为Y,
根据稀释前后溶质质量不变有:Y×36.5%=40g×14.6%,
Y=16g.故填:16g.
(2)上述反应的化学方程式为:Zn+2HCl═ZnCl2+H2↑.故填:Zn+2HCl═ZnCl2+H2↑.
(3)10g黄铜样品中锌的质量为:10g﹣5.45g=4.55g,
设生成氢气总质量为X,
Zn+2HCl═ZnCl2 +H2↑,
65 2
4.55g X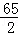 =
= ,
,
X=0.14g,故填: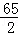 =
= .
.
(4)向第一次反应后所得溶液中加入8.74g水,则所得溶液的质量为:10g+1.3g﹣0.04g+8.74g=20g,
则所得溶液的质量分数为: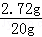 ×100%=13.6%.故填:13.6%.
×100%=13.6%.故填:13.6%.
(5)由表中数据可知,铜的质量为5.45g,
黄铜样品中铜的质量分数为: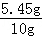 ×100%=54.5%,
×100%=54.5%,
2000t黄铜中铜的质量为:2000t×54.5%=1090t,
需要Cu2S的质量为:1090t÷(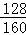 ×100%)=1362.5t,
×100%)=1362.5t,
需要含杂质50%的辉铜矿的质量为:1362.5t÷50%=2725t.故填:2725t.
考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:计算题
实验室高温煅烧125g含CaCO380%的石灰石(杂质不分解也不与酸反应),一段时间后,停止实验,冷却后用剩余的固体处理废盐酸。问能否处理含70gHCl的废盐酸,请写出计算过程。
已知:CaCO3 CaO+ CO2↑
CaO+ CO2↑
CaO+2HCl=CaCl2+H2O
Ca(OH)2+2HCl=CaCl2+2H2O
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
二氧化碳是一种宝贵的碳氧资源.它可以与氢气反应生成多种有机物,CO2转化为乙烯(C2H4)的化学方程式为:2CO2+6H2 C2H4+4H2O.若用24g H2转化CO2,则理论上能生成C2H4的质量为多少克?
C2H4+4H2O.若用24g H2转化CO2,则理论上能生成C2H4的质量为多少克?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
以下是某研究小组探究影响反应速率部分因素的相关实验数据.
| 实验序号 | 过氧化氢溶液浓度、% | 过氧化氢溶液体积/ml | 温度/C | 二氧化锰的用量/g | 收集氧气的体积/ml | 反应所需的时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 15.05 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 3.03 |
| ③ | 30 | 5 | 35 | | 2 | 48.21 |
| ④ | 30 | 5 | 55 | | 2 | 10.95 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
将12g的石灰石放入烧杯中,加入一定量的稀盐酸,待恰好完全反应后,测得产生4.4g气体(杂质不溶于水,也不参加反应)。
计算:该石灰石中钙元素的质量分数是多少?(结果保留整数)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成,取四份样品分别加稀硫酸反应,其实验数据记录如下表。
| 样品 | 第1份 | 第2份 | 第3份 | 第4份 |
| 取样品质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
| 取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
| 产生气体质量(g) | 0.4 | 0.8 | 1.0 | 1.0 |
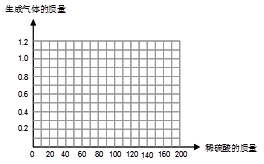
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
实验室用过量的稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀的质量关系如图所示.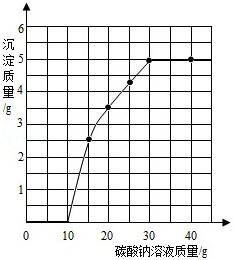
(1)实验中生成沉淀的最大质量是 g.
(2)开始加入碳酸钠溶液时,还没有产生沉淀的原因是 .
(3)计算原滤液中氯化钙的质量分数.(已知:CaCl2+Na2CO3=CaCO3↓+2NaCl)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
校化学兴趣小组的同学取60g氯化钙溶液,向其中加入适量碳酸钠溶液,反应完毕后过滤,所得固体用作制取牙膏摩擦剂的主要原料,同时所得滤液用来进行小麦选种(选种液要求氯化钠是质量分数在10%~20%之间)。实验过程中所加碳酸钠溶液的质量与生成碳酸钙沉淀的质量关系如下图所示。通过下图可知,当氯化钙恰好反应完时: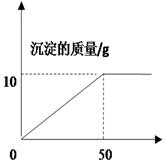
(1)消耗碳酸钠溶液的质量为 g;
(2)请通过计算回答,此时所得氯化钠溶液能否作为小麦选种液?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某同学称取一定质量的铁粉样品(含有少量不与稀硫酸反应的杂质),放入烧杯中,加入98g稀硫酸,恰好完全反应,生成气体的质量与反应时间的关系如图所示,试回答下列问题: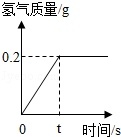
(1)根据图象,恰好完全反应时生成氢气的质量是 g;
(2)样品中铁的质量是多少?稀硫酸的溶质质量分数是多少?(写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com