
【题目】下列化学方程式符合题意且书写正确的是( )。
A. 正常的雨水略呈酸性的原因:CO2 + H2O==H2CO3
B. 生活中用天然气作燃料:C2H5OH + 3O2![]() 2CO2 + 3H2O
2CO2 + 3H2O
C. 胃舒平(含氢氧化铝)治疗胃酸过多症:Al(OH)3 + HCl =AlCl3 + H2O
D. 用大理石和盐酸制取二氧化碳:CaCO3 + 2HCl=CaCl2 + H2O + CO2
 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:初中化学 来源: 题型:
【题目】白磷、红磷都是可燃物,都可以在一定条件下燃烧。以下是利用它们的可燃性进行的三个实验,请分别回答下列问题。

(1)通过实验1可以探究燃烧的条件。烧杯中放有80℃热水,a、b、c处分别放有药品,实验中只有a处的白磷燃烧。a与c对比、a与b对比,说明燃烧需要的条件是_________________,白磷燃烧的化学方程式为__________。
(2)通过实验2可以测定_______________。待集气瓶中的红磷熄灭,冷却后打开弹簧夹,当观察到烧杯中的水进入集气瓶中,液面约上升到刻度__________处的现象时,可达到该实验目的。
(3)通过实验3可以验证质量守恒定律。实验前将白磷放入锥形瓶中,称量装置的总质量,引燃白磷,待反应后再称量装置总质量,发现托盘天平_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2014年5月7日在南京丢失的放射源铱﹣192,于5月10日安全回收.铱﹣192常用于肿瘤治疗.下图是铱﹣192在元素周期表中的信息,有关铱的说法不正确的是

A. 铱的元素符号是Ir B. 铱元素是非金属元素
C. 铱原子的原子序数为77 D. 铱元素的相对原子量为192.2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过化学反应,可以生产出自然界不存在的新材料新物质:
(1)利用赤铁矿和焦炭等在高炉可冶炼出生铁,反应原理为___________________
(2)因金属锈蚀而报废的金属设施全世界一年总量在3—6亿吨,铁生锈的主要条件是与_____直接接触,预防金属锈蚀就是要破坏生锈的条件,如自行车链条表面_____________可防锈等。
(3)在自然界中,金、银都有以单质形式的存在,铁、铝等都以化合物形式存在,这说明铁、铝等的化学活动性比金、银___________(活泼或不活泼)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是家用豆浆机,请根据图回答下列问题:

(1)制作材料中属于金属或合金的是 ______ (选填一种 物质编号),
(2)合金与组成它的纯金属相比,硬度 ______、熔点______。
(3)属于单质的是 ______ (选填一种物质编号)
(4)传统的生豆浆是用石磨来打磨的,打磨的过程是 ______变化 ;
(5)用操作将黄豆渣分离的方法类似于我们实验中的 ______ 操作.
查看答案和解析>>
科目:初中化学 来源: 题型:
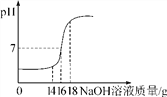
【题目】将5%的NaOH溶液逐滴加入10g稀盐酸中,边滴加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示,请回答:
(1)当恰好完全反应时,消耗NaOH溶液的质量为多少g;
(2)计算稀盐酸中溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】五氧化二钒(V2O5)是一种工业催化剂,下图是生产V2O5的工业流程,下列说法正确的是
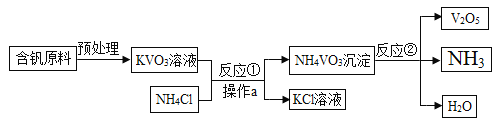
A. NH3能使干燥的红色石蕊试纸变蓝
B. 反应①中生成的副产物KCl在农业上可用作钾肥
C. 反应②的化学方程式为2NH4VO3![]() V2O5+2NH3↑+H2O
V2O5+2NH3↑+H2O
D. 操作a中需要的所有仪器为铁架台、烧杯、滤纸、玻璃棒
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明选择“铝丝和盐酸反应的快慢与什么因素有关”的课题开展探究。下表是他分别用相同质量的铝丝和足量稀盐酸反应的三组实验数据:
实验编号 | 盐酸的浓度/% | 反应温度/℃ | 铝丝消失 的时间/s |
① | 3 | 20 | 500 |
② | 6 | 20 | 300 |
③ | 6 | 30 | 80 |
(1)写出铝和盐酸反应的化学方程式:________________________________。
(2)实验②和③表明:该反应的快慢与__________有关。
(3)能表明盐酸浓度对反应快慢有影响的实验编号是________和________。
(4)如果把实验①中盐酸的浓度改为4%,请你推出铝丝消失的时间(用t表示)的取值范围:________________。
(5)该实验除了用铝丝消失的时间来衡量反应的快慢外,你还能提出新的方法来衡量该反应的快慢吗?
方法:_____________________________________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小金制作了一个如图甲所示的简易酸碱灭火器,并进行了如图乙所示的灭火操作,结束后对瓶中残留液进行了如下实验:①取少量残留液于试管中,滴加2滴紫色石蕊试液,变红色;②另取少量残留液于试管中滴加适量氯化钡溶液,有白色沉淀,则残留液中有大量的( )

A.硫酸钠 B.碳酸钠 C.盐酸 D.氯化钠
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com