
【题目】水、溶液在生产、生活中起着十分重要的作用,请根据所学知识回答问题。
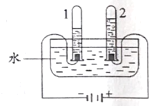
(1)氢气是理想的清洁、高能燃料。水分解可获得H2和O2。
①图中,产生氢气的试管是_____(填“1”或“2”)。
②我国开发出一种新型催化剂,实现了在光照下分解水,反应的化学方程式为_____。
(2)粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等)。某班同学在粗盐提纯实验中,为把少量可溶性杂质Na2SO4、MgCl2一并除去,将教材中实验方案修改设计如下,请据此回答问题:
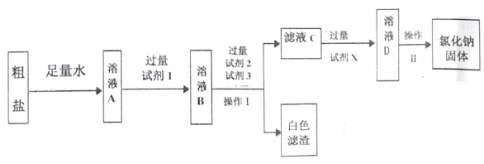
①请写出溶液A中所含的阳离子_____(用化学符号表示)。
②若试剂1是澄清石灰水,按先后顺序向溶液B加入试剂2和试剂3,则试剂2为_____。(填化学式),试剂3的作用是_____。
③请写出操作Ⅱ的名称:_____。
(3)若用所得氯化钠配制50g质量分数为6%的氯化钠溶液,需水_____mL,实验中除了用到天平、烧杯、量筒、玻璃棒等仪器外,还需用到的玻璃仪器是_____。
【答案】1 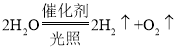 Na+、Ca2+、Mg2+ BaCl2 除去CaCl2、过量的氯化钡和氢氧化钙 蒸发结晶 47 胶头滴管
Na+、Ca2+、Mg2+ BaCl2 除去CaCl2、过量的氯化钡和氢氧化钙 蒸发结晶 47 胶头滴管
【解析】
(1)①在电解水实验中,“正氧负氢”,生成氢气和氧气的体积比约为2:1,故产生氢气的试管是1;
②水在光照和催化剂的作用下生成氢气和氧气,该反应的化学方程式为: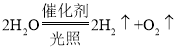 ;
;
(2)①粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等),将粗盐溶于水,溶液中含有氯化钠、氯化镁、氯化钙等,故含有的阳离子有:Na+、Ca2+、Mg2+;
②若试剂1是澄清石灰水,氢氧化钙能与氯化镁反应生成氢氧化镁和氯化钙,除去氯化镁,按先后顺序可向溶液B加入试剂2,可加入过量氯化钡,氯化钡能与硫酸钠反应生成硫酸钡白色沉淀和氯化钠,然后加入过量的试剂3碳酸钠,碳酸钠能与氯化钙反应生成碳酸钙和氯化钠,碳酸钠能与过量氯化钡反应生成碳酸钡和氯化钠,碳酸钠能与过量的氢氧化钙反应生成碳酸钙和氢氧化钠,故加入试剂3的目的是:除去氯化钙、过量的氯化钡和氢氧化钙;
③由图可知,溶液D经过操作Ⅱ变为氯化钠固体,故操作Ⅱ是蒸发结晶;
(3)若用所得氯化钠配制50g质量分数为6%的氯化钠溶液,,溶质质量=溶液质量×溶质质量分数=50g×6%=3g,溶剂质量=溶液质量=溶质质量=50g-3g=47g,即47mL;
用固体配制一定溶质质量分数的溶液,所需仪器:称量(药匙、托盘天平)、量取(量筒、胶头滴管)、溶解(烧杯、玻璃棒),故还需要用到的玻璃仪器是:胶头滴管。


科目:初中化学 来源: 题型:
【题目】向含有![]() 、
、![]() 、
、![]() 的混合溶液中加人一定量的铁粉,使其充分反应后,过滤,向滤渣中滴加稀盐酸,有气泡产生,则下列结论正确的是( )
的混合溶液中加人一定量的铁粉,使其充分反应后,过滤,向滤渣中滴加稀盐酸,有气泡产生,则下列结论正确的是( )
A.滤液中一定含![]() ,可能含
,可能含![]()
B.滤液中一定含![]() 、
、![]() 、
、![]() 、
、![]()
C.滤液中一定含![]() 、
、![]() ,可能含
,可能含![]()
D.滤液中一定含![]() 、
、![]() ,不含
,不含![]() 、
、![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学的学科特征让在原子、分子的水平上研究物成和创造物质。请从微观的角度回答下列问题。
(1)物质的结构决定性质。
①根据Na、Al的原子结构示意图![]() 可推知,金属Na、Al的化学性质不同的原因是______ 。
可推知,金属Na、Al的化学性质不同的原因是______ 。
②CO和CO2化学性质不同的原因是_______________ .
③稀盐酸和稀硫酸都可使紫色石蕊试剂变红,原因是___________________。
(2)下图是氢气在氧气中燃烧的微观示意图(图中“O”代表氢原子,“●“代表氧原子)。

①参加该化学反应的最小粒子是__________( 填微粒符号)。
②写出该反应的化学方程式 ____________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在宏观、微观和符号之间建立联系是化学特有的思维。回答下列问题:
(1)如图是钠元素与氯元素在元素周期表中的信息和与其相关的粒子结构示意图。
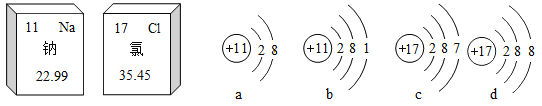
①氯原子核外电子数为__。
②氯化钠是由图中___(填字母编号)构成的。
③氧和氯两种元素最本质的区别是它们原子中的__不同。
(2)尿素(CO(NH2)2)是一种常用的化肥,工业上生产尿素的反应的微观示意图如下:
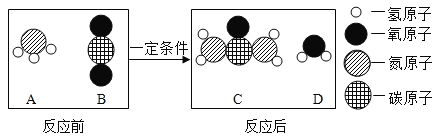
①尿素由_(填数字)种元素组成,属于___肥。
②生产尿素的反应中,参加反应的A与B的质量比为___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】从如图所示的两种粒子结构示意图中,所获取的信息正确的是( )
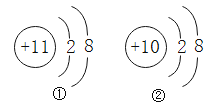
A.它们属于不同种元素
B.它们都属于非金属元素
C.它们原子的核外电子数相同
D.①表示阴离子,②表示原子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某碳酸钠样品含有少量的硫酸钠,取一定质量的该样品,完全溶解在水中配制成100g溶液,将其全部加入到50g一定质量分数的硫酸溶液中,恰好完全反应,生成的气体全部逸出后,所得溶液质量是145.6g。将所得溶液蒸干,得到15.6g硫酸钠。试计算:
(1)加入的硫酸溶液的溶质质量分数;
(2)原碳酸钠样品中硫酸钠的质量分数(计算结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】还原铁粉是化工生产及实验室中常用的还原剂。工业上以绿矾(FeSO4·7H2O)为原料制备还原铁粉的工艺流程见图1。
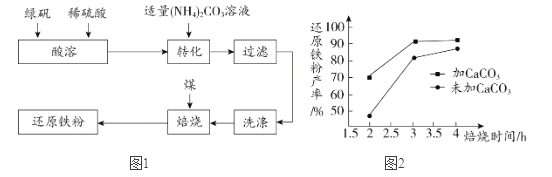
(1)转化时,将(NH4)2CO3溶液加入到FeSO4溶液中,目的是制得FeCO3。
(2)将FeCO3浊液暴露在空气中,反应的化学方程式为:![]() ,其中X是_____。
,其中X是_____。
(3)焙烧时,发生的反应有:①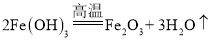 ; ②
; ②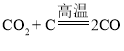 ;③
;③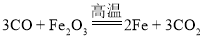 ,其中属于分解反应的是________(填序号)。
,其中属于分解反应的是________(填序号)。
(4) 在焙烧过程中需加入CaCO3进行脱硫处理。图2为加CaCO3和不加CaCO3对还原铁粉产率的影响,由图可以得出的结论是_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现欲探究某固体混合物 A 的成分,已知其中可能含有 NaCl、Na2CO3、CuO、NH4NO3、BaCl2 五种物质中的两种或多种。按图所示进行实验,出现的现象如图所示(所有可能发生的反应均恰好完全反应)。
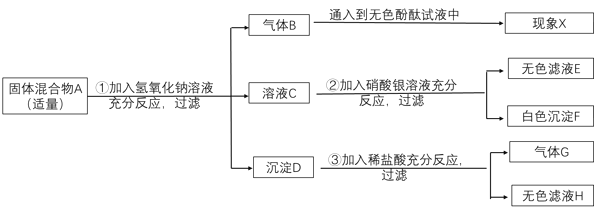
试根据实验过程和图示提供的信息,进行分析推理,填写以下空白:
(1)固体混合物中 A 中一定存在的物质有_____种。
(2)气体 B 的化学式为_________,现象 X 为____________。
(3)在溶液 C 中,一定存在的酸根离子是_____(填写离子符号), 白色沉淀 F 的化学式为________。
(4)写出步骤③中生成气体 G 的化学方程式___________。
(5)固体混合物中 A 中,一定不存在的物质是(写化学式)__________, 你做出此判断的理由是______________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了测定某硫酸铜溶液的质量分数,小杨同学取50.0g样品置于烧杯中,逐滴加入氢氧化钠溶液,加入氢氧化钠溶液质量和生成沉淀质量的关系如下图所示。请计算:
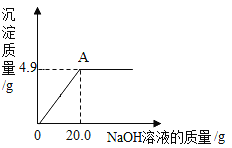
(1)NaOH的化学式量为_________。
(2)硫酸铜刚好完全反应时,所得溶液的质量为_____g(保留一位小数)。
(3)硫酸铜溶液中溶质的质量分数是________?(写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com