
| 加入稀硫酸次数 | 加入稀硫酸质量 | 剩余固体质量 |
| 第1次 | 50g | 43.5g |
| 第2次 | 100g | m g |
| 第3次 | 150g | 11g |
| 第4次 | 100g | 11g |
分析 (1)依据50g稀硫酸能够消耗的锌的质量分析m的数值;
(2)依据锌与稀硫酸反应中锌的质量可求出反应的硫酸的质量,进而可得稀硫酸的质量分数;
(3)依据最后剩余的固体物质是铜,确定金属锌的质量,进而求算生成硫酸锌的质量分析解答.
解答 解:(1)根据表格提供的数据可以看出,50g硫酸消耗金属锌的质量为:50g-43.5g=6.5g,故100g硫酸消耗锌的质量为:6.5g×2=13g,故m值为:50g-6.5g-13g=30.5g,故填:30.5;
(2)设硫酸的质量分数为x
Zn+H2SO4=ZnSO4+H2↑
65 98
6.5g 50g×x
$\frac{65}{98}=\frac{6.5g}{50g×x}$
x=19.6%,故填:19.6%;
(3)第四次反应后剩余固体是11g,故锌的总质量为:50g-11g=39g,设生成硫酸锌的质量为y,生成氢气的质量为z
Zn+H2SO4=ZnSO4+H2↑
65 161 2
39g y z
$\frac{65}{39g}=\frac{161}{y}=\frac{2}{z}$
y=96.6g
z=1.2g
故第4次反应后烧杯溶液中所含硫酸锌的溶质质量分数为:$\frac{96.6g}{39g+400g-1.2g}×100%≈22.1%$;
答:第4次反应后烧杯溶液中所含硫酸锌的溶质质量分数为22.1%.
点评 实验数据的处理:利用每次加入稀硫酸前后固体质量差即反应消耗金属的质量的关系,可判断加入稀硫酸的反应情况.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
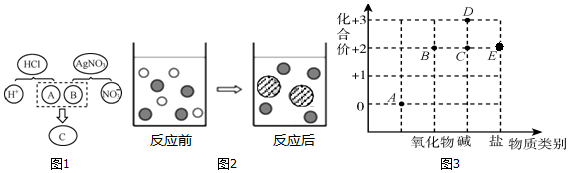
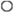 ①
① ③
③ ②
②查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用Ca(OH)2溶液除去Na2CO3溶液中的NaOH | |
| B. | 用铁粉除去FeCl2溶液中的CuCl2 | |
| C. | 用溶解、过滤、蒸发的方法除去白糖中混入的沙土 | |
| D. | 将带火星的木条伸到瓶口检验氧气是否收集满了 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 溶于水时生成了盐酸 | |
| B. | 水本来就呈酸性 | |
| C. | 组成中含有氢元素 | |
| D. | 溶于水时,在水中解离产生了氢离子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na2CO3溶液中混有Na2SO4(滴入过量氯化钡溶液) | |
| B. | CaCl2溶液中混有HCl (加入过量CaCO3固体并过滤) | |
| C. | CuO固体中混有碳粉(空气中加热) | |
| D. | CO中混有CO2 (通入NaOH溶液) |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
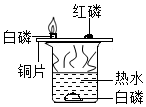 为探究燃烧的条件,某同学进行如图所示的实验.下列有关判断错误的是( )
为探究燃烧的条件,某同学进行如图所示的实验.下列有关判断错误的是( )| A. | 白磷是可燃物,红磷不是可燃物 | |
| B. | 烧杯底部的白磷不燃烧是因为没有与氧气接触 | |
| C. | 铜片上的红磷不燃烧是因为温度未达到它的着火点 | |
| D. | 热水的作用是提供热量及隔绝氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲>丙>乙 | B. | 丙>乙>甲 | C. | 甲>乙>丙 | D. | 丙>甲>乙 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 所用试剂及方法 |
| A | 二氧化碳 | 氯化氢 | 氢氧化钠溶液 |
| B | 炭粉 | 铁粉 | 磁铁吸引 |
| C | KCl | KClO3 | MnO2,加热 |
| D | 二氧化碳 | 一氧化碳 | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com