解:(1)铜做导线是利用铜的导电性;
(2)铝与氧气反应生成氧化铝,根据最小公倍数法配平即可,所以方程式是:4Al+3O
2═2Al
2O
3;
(3)只用一种金属单质,该金属就是排在中间的金属,所以该金属是铜,铜与铝的盐溶液不反应,铜与硝酸银反应生成银和硝酸铜,用观察法配平即可,所以方程式是:Cu+2AgNO
3═Cu(NO
3)
2+2Ag;除去铝表面的氧化膜一般用砂纸打磨;铝把氧化膜反应完后,会与铝反应,铝与盐酸反应生成氯化铝和氢气,所以当有气泡冒出,说明已经把氧化膜反应完了;
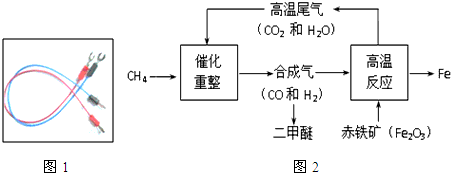
(4)①二甲醚(CH
3OCH
3)的一个分子中含有2个C,6个H,1个O,因为CO和H
2按分子个数比1:2,所以需要2个CO分子和4个H
2分子,所以多出了2个H,1个O,所以生成物中还有水(或H
2O);
②由于一氧化碳、氢气都具有还原性,都能与氧化铁反应,一氧化碳与氧化铁反应的反应物是一氧化碳和氧化铁,生成物是铁和二氧化碳,不属于置换反应,反应条件是高温,用观察法配平即可;所以方程式是:3CO+Fe
2O
3
2Fe+3CO
2.
故答案为:(1)导电; (2)4Al+3O
2═2Al
2O
3;(3)Cu+2AgNO
3═Cu(NO
3)
2+2Ag; 用砂纸打磨;有气泡产生;(4)①H
2O;②3CO+Fe
2O
3
2Fe+3CO
2.
分析:(1)铜做导线是利用铜的导电性;(2)根据铝与氧气反应的方程式考虑;(3)只用一种金属单质,该金属就是排在中间的金属,根据铜与硝酸银反应的方程式进行书写即可;除去氧化膜一般用砂纸打磨;根据盐酸与铝反应的现象考虑;(4)①根据反应前后各种原子个数和种类不变考虑;②根据置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物进行判断,并写出相应的方程式.
点评:通过回答本题知道了金属的性质,保护金属资源的途径,方程式的书写方法.

 2Fe+3CO2.
2Fe+3CO2. 2Fe+3CO2.
2Fe+3CO2.


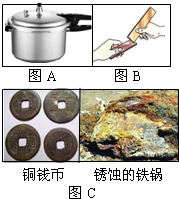 金属材料在生活、生产中应用十分广泛.
金属材料在生活、生产中应用十分广泛.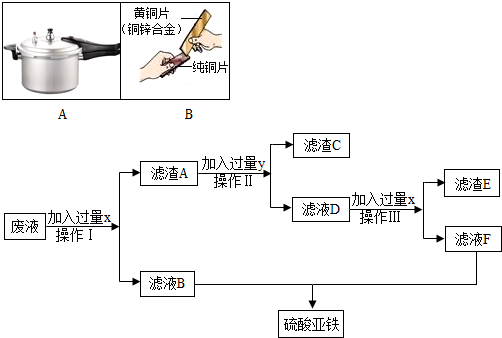
 金属材料在生活、生产中应用十分广泛.
金属材料在生活、生产中应用十分广泛. 金属材料在生活、生产中应用十分广泛.
金属材料在生活、生产中应用十分广泛.