
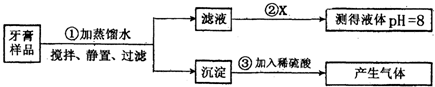
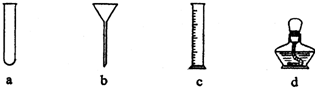


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:初中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题
| A.pH=13溶液 | B.pH=11溶液 | C.pH=14溶液 | D.pH=1溶液 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.用润湿的pH试纸精确测定不同品牌洗发液的酸碱度 |
| B.用酒精浸泡捣烂的紫罗兰花瓣自制酸碱指示剂 |
| C.用柠檬酸、果汁、白糖、水、小苏打等自制汽水 |
| D.用干电池、灯泡、导线、6B铅笔芯等验证石墨可以导电 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题
| 1 |
| 4 |

| 第一次 | 第二次 | 第三次 | |
| 所取样品的质量/g | 9 | 9 | 18 |
| 所用硫酸溶液质量/g | 60 | 80 | 50 |
| 生成氢气的质量/g | 0.6 | 0.6 | 0.6 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验内容 | 预测现象 | 结论 |
| 取少量容器中的上层溶液于试管中,加入过量的氯化钡溶液,静置 | ①若有白色沉淀,溶液呈无色 | 物质是碳酸钠 |
| ②若无沉淀生成,溶液呈红色 | 物质是氢氧化钙 | |
| ③若有白色沉淀,溶液呈红色 | ____________________ |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.酚酞溶液 | B.镁条 | C.硫酸铜溶液 | D.氯化钾溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com