
| 实验操作 | 测定结果 | 白色固体成分 |
| 用pH试纸测定反应后溶液的酸碱度,操作方法是 |
pH>7 | |
| NaCl |
| 加入稀盐酸的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 12.9 | 12.7 | 12.5 | 12.3 | 11.9 | 7.0 | 2.1 | 1.9 |
| 73 |
| 74 |
| 0.073g |
| x |
| 实验操作 | 测定结果 | 白色固体成分 |
| 用pH试纸测定反应后溶液的酸碱度,操作方法是 用洁净玻璃棒蘸取溶液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较 | pH>7 | NaOH和NaCl |
pH=7 |
NaCl |


科目:初中化学 来源: 题型:
| A、向某无色溶液中滴加酚酞试液变红,则溶液一定是碱溶液 |
| B、向某固体中滴加稀盐酸,有气泡产生,该固体一定是碳酸盐 |
| C、含碳元素的物质充分燃烧生成CO2,则燃烧能生成CO2的物质一定含碳元素 |
| D、向某溶液中加入BaCl2溶液和稀硝酸,出现白色沉淀,则该溶液一定含有SO42- |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
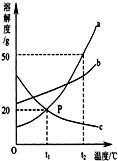 如图是a、b、c三种物质的溶解度曲线.
如图是a、b、c三种物质的溶解度曲线.查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com