
【题目】取含杂质的硫酸镁固体样品 15 g(杂质不溶于水,也不参加反应),向其中加入一定量的氢氧化钠溶液,恰好完全反应,过滤得到一定质量的滤渣和 142 g 溶质质量分数为 10%的滤液。计算:
(1)样品中硫酸镁的质量分数_____;
(2)所加入的氢氧化钠溶液的质量_____。
科目:初中化学 来源: 题型:
【题目】实验室现有一瓶水垢样品,其成分为氢氧化镁和碳酸钙。已知:氢氧化镁受热易分解,反应的化学方程式为:Mg(OH)2![]() MgO + H2O;碳酸钙高温下分解。某兴趣小组为测定其中各成分的质量分数,取12.9g水垢样品加热,加热过程中剩余固体的质量随加热时间的变化如下图所示。关于加热一段时间后剩余固体的判断,下列说法错误的是( )
MgO + H2O;碳酸钙高温下分解。某兴趣小组为测定其中各成分的质量分数,取12.9g水垢样品加热,加热过程中剩余固体的质量随加热时间的变化如下图所示。关于加热一段时间后剩余固体的判断,下列说法错误的是( )
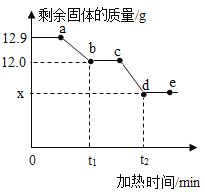
A. 图中a点剩余固体是由一种盐和一种碱组成
B. 若剩余固体中钙元素的质量分数为36.0%,则剩余固体的成分为CaCO3和MgO
C. 图中ab间任一点(不包括a、b两点)的剩余固体成分为CaCO3、MgO和Mg(OH)2
D. 若向c点的剩余固体中加入足量稀盐酸,充分反应生成CO2的质量为(12.0-x)g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小丽为确认所回收易拉罐的主要成分是铝还是铁,剪取金属片打磨后,设计了如两种不同方法进行检验,这样设计的理由是
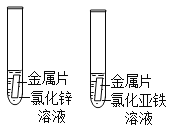
A.铁、铝有不同的物理性质
B.活泼金属易与氧气反应
C.排在前面的金属可以把酸中的氢置换出来
D.活动性较强的金属可把活动性较弱的金属从它的化合物溶液中置换出来
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组为了测定贝壳中碳酸钙的质量分数,做如下实验:取贝壳样品12g装入烧杯中,向其中加入一定质量分数的稀盐酸(杂质不溶于水也不参加反应),所加盐酸的质量与烧杯中剩余固体质量关系如下图。试计算:
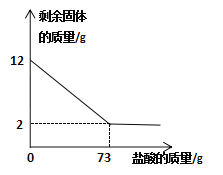
(1)贝壳中碳酸钙的质量为________g
(2)稀盐酸中溶质的质量分数______。(写出计算过程)
(3)恰好完全反应时,所得溶液中溶质的质量分数______。(计算精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某溶液可能含有硫酸铜、氯化铜、硝酸钾、硫酸、盐酸中的一种或几种,为了探究其 组成,向一定质量的该溶液中逐滴加入氢氧化钡溶液,生成沉淀的质量与所加氢氧化钡溶液的质量之间的关系如图所示。下列叙述中,正确的是

A.该溶液一定含有盐酸、氯化铜,可能含有硝酸钾
B.加入氢氧化钡溶液至过量,共发生了二个化学反应
C.反应过程生成的沉淀一定有氢氧化铜,可能有硫酸钡
D.到达 b 点时所消耗氢氧化钡溶液中溶质的质量是 17.1 g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2011年8月,云南曲靖市发生铬渣非法倾废致污事件,严重影响到珠江流域水质。铬元素是人体必需的微量元素,但铬过量会引起污染,危害人体健康。
(1)六价铬(Cr)对人体有毒,含铬废水要经化学处理后才能排放,具体的操作方法是:①加入一定量的绿矾(FeSO4·7H2O)把废水中的正六价铬转化成正三价铬离子;②加入过量的石灰水,使铬离子转变为氢氧化铬沉淀,则氢氧化铬的化学式为______;③再通过_____等基本操作除去沉淀物。
(2)不同价态的铬毒性不一样,其中六价铬的毒性最大,六价铬为吞入性和吸入性极毒物,若人体内六价铬超标,需要服用蔬菜和水果中富含的_____来缓解毒性。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了验证镁、铁、铜的活动性顺序,某同学选择了打磨过的铁丝,请你回答:
(1)该同学还需要选择的另外两种溶液是_____溶液和______溶液。
(2)根据选定的试剂,用来解释农药波尔多液不能用铁制容器盛装,则化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2014年10月24日,我国探月工程三期再入返回飞行试验器在西昌卫星发射中心用长征三号丙运载火箭成功发射升空,首次成功实现再入返回飞行试验。回答下列问题:
(1)偏二甲肼是目前国际最普遍使用的火箭燃料,氧化剂为四氧化二氮,当火箭燃料完全反应时生成三种新物质,均是空气中的无害成分,写出该反应的化学方程式为_____。通过此反应谈谈你对燃烧的概念有什么新的认识?_______。
(2)火箭燃烧时将____能转化成热能,再转换成火箭的机械能,于是火箭升空。火箭从研制到发射过程,其中一定不属于物理变化的是________(填序号)
A 铝铜合金铸造火箭发动机 B 火箭推进剂采用液氦冷却
C 第三级燃料液氢由氢气液化而成 D 点燃火箭燃料燃烧
(3)火箭特种燃料易燃、易爆、剧毒、易挥发、强腐蚀,是一种危险级别最高的化工品,燃料加注将在火箭发射前24小时进行。因此在运输、储存和加注时应采取的安全保护措施是___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2019 年 12 月 17 日,我国首艘国产航母山东舰正式入列,它和辽宁舰一起组成了我国首支双航母编队,共同守卫我国绵长的海岸线及丰富的海洋资源。

(1)可燃冰被科学家誉为“未来能源”、“21 世纪能源”。我国在南海海域试采可燃冰已获得成功,成为全球第一个在海域可燃冰试开采中获得连续稳定产气的国家。可燃冰是一种海底新型矿产资源,它是由天然气和水在低温高压条件下形成的冰状固体,其中甲烷占 80%~99.9%,(可表示为 mCH4·nH2O),能直接点燃,所以称为“可燃冰”。
①甲烷充分燃烧的化学方程式为_____________________________。
②为什么说可燃冰是清洁能源?______________________________。
(2)金属镁广泛应用于国防工业和生产生活。下图所示为从卤水(或海水)中提取镁的工艺流程:
![]()
①在上述工艺流程中,步骤①里所发生的反应属于_________反应。(选填“化合”、“分解”、“复分解”、“中和”之一)
②从海水中提取MgCl2 时,经历了“MgCl2 → Mg(OH)2↓ → MgCl2”的转化过程, 请分析这样做的目的是什么?__________。
(3)我国著名化工专家侯德榜在氨碱法基础上创立了更先进的侯氏制碱法,为世界纯碱工业技术发展做出了杰出贡献。在海水“制碱”过程中,涉及 NH4Cl、NaHCO3 等物质, 请结合如图所示的溶解度曲线,回答下列问题:
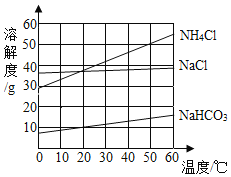
①侯氏制碱法中的“碱”是指(填化学式)___________________。
②30°C 时,将 11g NaHCO3 固体加入到 100g 水中, 充分搅拌,最终能得到__________g 溶液。
③氨碱法原理之一是:NaCl + NH3 + H2O + CO2 = NH4Cl + NaHCO3,在两种生成物中, 最先结晶析出的是_________________,请你根据溶解度曲线和产物质量关系,解释其原因:________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com