
【题目】如图是关于初中化学常见的五种物质的转化关系网络(其他反应物和生成物已略去)。其中A是黑色固体,B为红棕色固体,C、D、E常温下均为气体,C的相对分子质量大于E。请回答:
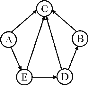
(1)A的化学式____________________;D的化学式____________________。
(2)写出B向C转化的反应方程式____________________。
【答案】(1)C O2
(2)3CO+ Fe2O3 高温 2Fe + 3CO2或3C+ 2Fe2O3 高温 4Fe + 3CO2↑
【解析】
试题分析:框图式的推断题,抓住一些特殊的反应现象、特殊的性质及特殊的反应条件等级题目的“题眼”, 该题的题眼B为红棕色固体,可判断为氧化铁,C为气体,由B转化而来,可判断为二氧化碳,A是黑色固体,可能是碳、氧化铁,二氧化锰等,但要转化为气体E,且气体E能转化为C,C的相对分子质量大于E,故可判断E应为一氧化碳,那么A应为碳,D能与E反应,且能转化为氧化铁,故可判断D为氧气
(1)A为碳,化学式为:C ;D为氧气,化学式:O2
(2)B为氧化铁,C为二氧化碳,故B向C转化的反应方程式为:3CO+ Fe2O3 高温 2Fe + 3CO2或3C+ 2Fe2O3 高温 4Fe + 3CO2↑


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】(13分)中和反应是一类重要的反应。根据要求回答问题:
(1)许多物质在溶液中以离子形式存在。下图表示HCl、NaOH溶液及两者混合后溶质在溶液中的存在情况。
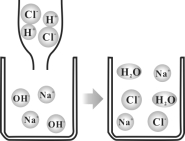
①盐酸具有酸的特性,是因为盐酸溶液中含有 (填微粒符号)。
②对比分析盐酸与氢氧化钠溶液混合前后溶液离子存在情况,可知两者反应时不会减少的离子是 。
③教材指出:酸与碱中和反应的结果是酸和碱各自的特性都消失。请结合上图并从微粒的角度分析,盐酸与氢氧化钠反应时,为何酸、碱各自的特性都消失?答: 。
(2)日常生活中,凡是使酸的酸性消失或碱的碱性消失的反应均被称为“中和”。如使用碳酸氢钠(其溶液显碱性)治疗胃酸(主要成分为盐酸)过多症,就因碳酸氢钠能使胃酸的酸性消失,而称为碳酸氢钠“中和”了过多的胃酸。现有碳酸氢钠溶液、酚酞溶液和盐酸溶液,设计实验证明碳酸氢钠溶液与盐酸反应时,碳酸氢钠溶液的碱性、盐酸的酸性都将各自消失。
操作 | 现象 | 结论 |
实验1:往装有碳酸氢钠溶液的试管中先加入2-3滴酚酞溶液,再逐滴加入盐酸直至恰好完全反应 | 滴入酚酞时的现象: ; 逐滴加入盐酸的现象: ________________。 | 两者反应时,碳酸氢钠溶液碱性消失 |
实验2: | 两者反应时,盐酸溶液酸性消失 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关实验操作的“先”与“后”的说法中,正确的是( )
A.制取气体时,先装药品,后检查装置的气密性
B.加热KClO3并用排水法收集O2实验结束时,先熄灭酒精灯,后移出导管
C.点燃CO气体前,应先检验其纯度,后点燃
D.煤气泄漏后先打开排风扇,后关闭煤气阀门
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用分子的观点解释下列现象,错误的是( )
A.热胀冷缩﹣﹣分子大小随温度的变化而改变
B.花香四溢﹣﹣分子不停地运动
C.食物腐败﹣﹣分子发生变化
D.酒精挥发﹣﹣分子不停地运动
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法符合事实的是
A、铁丝伸入盛有氧气的集气瓶中会剧烈燃烧
B、氯酸钾与二氧化锰混合后,即可产生大量氧气
C、硫燃烧后生成有刺激性气味的气体
D、铝放置在空气中不与氧气反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室制取并用排水法收集氧气的主要步骤有:
①装入药品;②检查装置气密性;③给固体药品加热;④将装置固定在铁架台上;⑤熄灭酒精灯;⑥收集气体;⑦将导管移出水槽.正确的操作顺序为( )
A.①②③④⑤⑥⑦ B.②①④③⑥⑤⑦
C.①②④③⑥⑤⑦ D.②①④③⑥⑦⑤
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】课外化学兴趣小组的同学利用某化工厂的废碱液(主要成分为Na2CO3、还含有少量NaCl)和石灰乳(氢氧化钙的悬浊液)为原料制备烧碱,并对所得的烧碱粗产品的成分进行分析和测定。
【查阅资料】①碱石灰是CaO与NaOH的固体混合物,可吸收二氧化碳和水;
②CO2+Ba(OH)2 ═ BaCO3↓+H2O。
【粗产品制备】
(1)将废碱液加热蒸发浓缩,形成较浓的溶液,冷却后与石灰乳混合,发生反应的化学方程式为 。
(2)将反应后的混合物过滤,得到的滤液进行蒸发结晶,制得NaOH粗产品。
【粗产品成分分析】
(1)取适量粗产品溶于水得澄清溶液,加入Ba(NO3)2溶液出现白色沉淀,由此该粗产品中一定不含有 ,理由是
(2)该小组同学通过对粗产品成分的实验分析,确定该粗产品中含有三种物质。
【含量测定】Na2CO3含量的测定:
该兴趣小组的同学设计了下图所示的实验装置。取20.0g粗产品,进行实验。
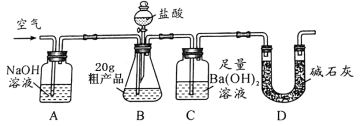
(1)实验过程中需持续缓缓通入空气,其目的是 。
(2)下列各项措施中,不影响测定准确度的是______(填标号)。
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A-B之间增添盛有浓硫酸的洗气装置
d.取消上图中D装置
(3)实验中准确称取20.0g粗产品,进行测定,测得BaCO3质量为1.97g。则粗产品中碳酸钠的质量分数为 。
(4)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数.实验证明按此方法测定的结果明显偏高,原因是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(5分)某同学设计了如下实验装置,进行碳还原性性质验证,对实验进行分析并回答:

(1)检查装置气密性的方法是:将导管浸入水中, ,说明装置气密性良好。
(2)证明碳具有还原性的实验现象是 , 。
(3)CuO发生 反应(填“氧化”或“还原”)。
(4)酒精灯加上网罩是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com