

| A. | 铁钉表面的锈迹消失,逐渐变得光亮 | |
| B. | 溶液由无色变为黄色,又由黄色变为浅绿色 | |
| C. | 一段时间后,铁钉表面有气泡生成 | |
| D. | 试管底部有红褐色沉淀生成 |
分析 生锈的铁钉表面是铁锈,里面是铁,铁锈能稀硫酸反应生成可溶性的硫酸铁和水;铁的金属活动性比氢强,能与稀硫酸反应生成硫酸亚铁和氢气,据此进行分析判断.
解答 解:A、铁锈能稀硫酸反应生成可溶性的硫酸铁和水,因此铁钉表面的锈迹消失,逐渐变得光亮,故选项说法正确.
B、稀硫酸呈无色,铁锈与稀硫酸反应生成的硫酸铁溶液呈黄色;铁与硫酸反应生成的硫酸亚铁溶液呈浅绿色,故会观察到溶液由无色变为黄色,又由黄色变为浅绿色,故选项说法正确.
C、铁的金属活动性比氢强,与稀硫酸反应生成硫酸亚铁和氢气,故会观察到一段时间后,铁钉表面有气泡生成,故选项说法正确.
D、氢氧化铁是红褐色的,此过程中没有氢氧化铁生成,因此不会观察到试管底部没有红褐色沉淀生成,故选项说法错误.
故选:D.
点评 本题难度不大,掌握酸的化学性质并能灵活运用是正确解答本题的关键.


科目:初中化学 来源: 题型:选择题
| A. | 镁在空气中燃烧 Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 | |
| B. | 生石灰与水剧烈反应 CaO+H2O=Ca(OH)2 | |
| C. | 铁钉浸入硫酸铜溶液中 2Fe+3CuSO4=3Cu+Fe2(SO4) | |
| D. | 氢氧化钠溶液和硫酸铜溶液混合 CuSO4+NaOH=CuOH↓+NaSO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
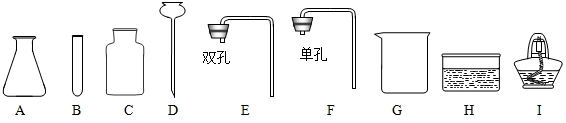
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 不放出氧气 | B. | 放出氧气速度减慢 | ||
| C. | 放出氧气的质量减少 | D. | 放出氧气的质量增多 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com