
| A. | 30% | B. | 70% | C. | 63% | D. | 无法计算 |
分析 工业上以CaO和HNO3为原料制备Ca(NO3)2•4H2O晶体.为确保制备过程中既不补充水分,也无多余的水分,也就是硝酸溶液中的水全部参与化学反应生成Ca(NO3)2•4H2O晶体,反应方程式为CaO+2HNO3+3H2O═Ca(NO3)2•4H2O,解答时可以设硝酸的质量为126g,根据化学方程式可知硝酸溶液中水的质量,据此结合质量分数的定义计算硝酸溶液中溶质的质量分数.
解答 解:工业上以CaO和HNO3为原料制备Ca(NO3)2•4H2O晶体.为确保制备过程中既不补充水分,也无多余的水分,也就是硝酸溶液中的水全部参与化学反应生成Ca(NO3)2•4H2O晶体,反应方程式为CaO+2HNO3+3H2O═Ca(NO3)2•4H2O.
设硝酸的质量为126g,则:
CaO+2HNO3+3H2O═Ca(NO3)2•4H2O
126 54
126g 54g
所以硝酸溶液中溶质的质量分数是 $\frac{126g}{126g+54g}$×100%=70%.
故选B.
点评 根据化学方程式计算溶液中溶质的质量分数,难度不大,关键是方程式的书写,旨在培养学生的理解能力和计算能力.


 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:初中化学 来源: 题型:填空题
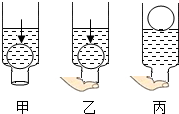 运用所学的科学知识回答:
运用所学的科学知识回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
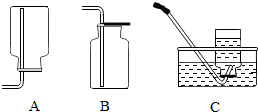 小红和她的同学学习了金属活动性及稀硫酸的一些性质后,对铜与浓硫酸能否发生反应产生了兴趣,并进行了如下探究:
小红和她的同学学习了金属活动性及稀硫酸的一些性质后,对铜与浓硫酸能否发生反应产生了兴趣,并进行了如下探究:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加热后的试管立即用冷水冲洗 | |
| B. | 猛力上下抽动试管内的试管刷 | |
| C. | 烧杯内壁附有油,用毛刷蘸上洗衣粉洗涤,再用水冲洗 | |
| D. | 仪器不必洗得很干净,加水振荡就行 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
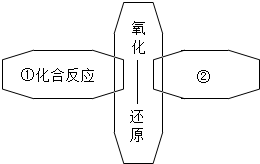 在反应前后有元素化合价发生变化的化学反应都属于氧化-还原反应.如图是化学兴趣小组通过自主学习构建的四种基本反应类型与氧化-还原反应的关系图.根据此图我能回答下列问题:
在反应前后有元素化合价发生变化的化学反应都属于氧化-还原反应.如图是化学兴趣小组通过自主学习构建的四种基本反应类型与氧化-还原反应的关系图.根据此图我能回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
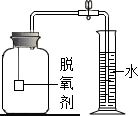 食品包装袋中常用脱氧剂.某化学兴趣小组将脱氧剂封口打开,将其倒在滤纸上,观察到脱氧剂大部分为黑色粉末,其中还夹杂着少量红色粉末.
食品包装袋中常用脱氧剂.某化学兴趣小组将脱氧剂封口打开,将其倒在滤纸上,观察到脱氧剂大部分为黑色粉末,其中还夹杂着少量红色粉末.| 实验编号 | 实验操作 | 实验现象 |
| ① | 取脱氧剂黑色粉末加入足量稀硫酸 | 粉末几乎全部溶解,只有少量黑色粉末未溶解,有气泡产生,溶液为浅绿色色 |
| ② | 实验①的残渣灼烧,将内壁有 澄清石灰水的小烧杯罩在上方 | 澄清石灰水变浑浊 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
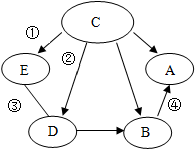 A、B、C、D、E是初中常见或学习过的5种物质,它们都含有一种相同的元素,如图表示各物质之间的转化关系.其中,A为食盐的主要成分,B中含有钡元素,D、E的溶液都有颜色,其他物质的溶液都为无色.
A、B、C、D、E是初中常见或学习过的5种物质,它们都含有一种相同的元素,如图表示各物质之间的转化关系.其中,A为食盐的主要成分,B中含有钡元素,D、E的溶液都有颜色,其他物质的溶液都为无色.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com