
分析 根据反应原理写出反应的化学方程式解答;
(1)根据检查装置气密性的方法进行分析解答;
(2)根据集气瓶内水的作用是为铁丝生锈提供水分解答;
(3)根据氧气约占空气体积的$\frac{1}{5}$解答;
根据保证本实验成功的关键是:①装置气密性好;②铁粉要足量;③要冷却至室温再读数等,结合红磷测定氧气的原理分析即可.
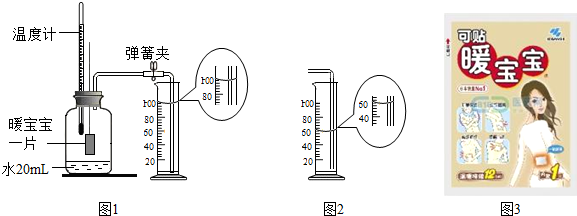
解答 解:暖宝宝中含有铁粉、活性炭、水、氯化钠等物质,遇空气发生反应的化学方程式是:4Fe+3O2+6H2O═4Fe(OH)3
(1)检查置气密性的方法是:连接好装置,把导管的一端放入水中,用手紧握试管,观察水中导管口有没有气泡冒出,如果有气泡冒出,说明装置不漏气.
(2)小组同学的设计中,集气瓶内水的作用是为铁粉生锈提供水分;
(3)根据反应前后烧杯内水的体积变化可以看出,消耗的氧气的体积是:100mL-60mL=40mL,故氧气的体积分数为:$\frac{40ml}{250mL-20mL}×$100%,即氧气约占空气体积的$\frac{1}{5}$;
实验反思:反思实验过程,你认为小组同学实验产生误差的可能原因有装置漏气,会使进入的水偏少,测定的结果偏小;发热剂没有完全生锈,没有将氧气耗尽;向发热剂中加入盐酸,如果有气泡生成,则说明有铁粉.
答案:4Fe+3O2+6H2O═4Fe(OH)3;
(1)连接好装置,把导管的一端放入水中,用手紧握试管,观察水中导管口有没有气泡冒出,如果有气泡冒出,说明装置不漏气.
(2)铁粉生锈提供水分;
(3)氧气约占空气体积的$\frac{1}{5}$;
发热剂没有完全生锈;向发热剂中加入盐酸,如果有气泡生成,则说明有铁粉.
点评 本题考查了实验步骤的设计,还对实验进行了评价,综合性比较强.实验设计题是近几年中考的重要考点之一,希望同学们前后联系,认真掌握.


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:初中化学 来源: 题型:推断题
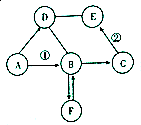 已知A、B、C、D、E、F是初中化学中常见的六种物质,其中A为-一种常见的酸,B、C、D为氧化物,E为单质且粉末为黑色,F常用于建筑材料.它们之间在一定条件下有如图所示的转化关系(图中“→”表示物质间存在转化关系,“一”表示两种物质间能发生反应,部分反应物和生成物已略去).请按要求回答下列问题:
已知A、B、C、D、E、F是初中化学中常见的六种物质,其中A为-一种常见的酸,B、C、D为氧化物,E为单质且粉末为黑色,F常用于建筑材料.它们之间在一定条件下有如图所示的转化关系(图中“→”表示物质间存在转化关系,“一”表示两种物质间能发生反应,部分反应物和生成物已略去).请按要求回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
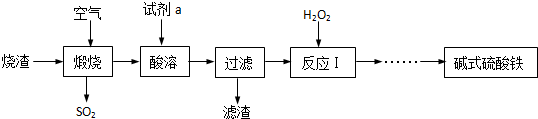
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
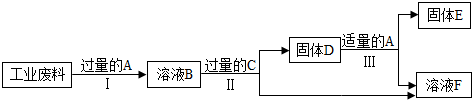
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
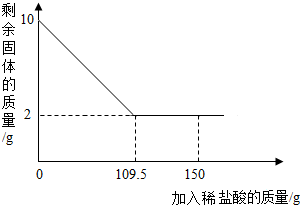 有一赤铁矿样品(主要成分为氧化铁),某学校化学兴趣小组为了测得样品中氧化铁的质量分数,进行了如下探究:小明取10g赤铁矿样品(杂质不溶于水和酸),不断加入稀盐酸到固体的质量不再减少,加入稀盐酸的量如图所示:求:
有一赤铁矿样品(主要成分为氧化铁),某学校化学兴趣小组为了测得样品中氧化铁的质量分数,进行了如下探究:小明取10g赤铁矿样品(杂质不溶于水和酸),不断加入稀盐酸到固体的质量不再减少,加入稀盐酸的量如图所示:求:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 3O--3个氧原子 | B. | CO2--1个二氧化碳分子 | ||
| C. | O2--2个氧原子 | D. | Fe+3--带3个单位正电荷的铁原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com