
碳和碳的氧化物是生活中常见的物质,也是初中化学学习的重要内容.
(1)如图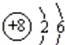 是,下列说法不正确的是 .
是,下列说法不正确的是 .
| A.氧原子的质子数为8 |
| B.氧原子在化学反应中易失去电子 |
| C.氧是地壳中含量最多的元素 |
| D.氧原子与氧离子的化学性质不同 |
(1)B;(2)二者的分子结构不同;(3)①其他条件相同时,反应物浓度越大,反应速率越快;
②2NaHCO3 Na2CO3+H2O+CO2↑;(4)CO2+NaOH═Na2CO3+H2O;
Na2CO3+H2O+CO2↑;(4)CO2+NaOH═Na2CO3+H2O;
Na2CO3+BaCl2═BaCO3↓+2NaCl;(5)一氧化碳有毒,燃烧生成二氧化碳,该气体能产生温室效应;
(6)20%.
解析试题分析:(1)根据原子结构示意图的意义可以知道:A.氧原子的质子数为8,故A说法正确;B.根据图示可以知道氧原子的最外层电子数大于4个,所以容易得到电子,故B说法错误;C.氧是地壳中含量最多的元素,故C说法正确;D.元素的化学性质取决于原子的最外层电子数,氧离子是氧原子得到电子之后而形成的,故氧原子与氧离子的化学性质不同,故D说法正确;故选B.(2)一氧化碳和二氧化碳的分子构成不同,所以它们的性质不同;(3)根据题给的条件可以知道,在反应条件相同的情况下,只有盐酸的浓度不同,而实验中观察到15%的稀盐酸与块状大理石反应制取二氧化碳,比用浓度为8%的稀盐酸与块状大理石反应制取二氧化碳的速率快,所以可以知道其他条件相同时,反应物浓度越大,反应速率越快;(4)氢氧化钠溶液可以和二氧化碳反应生成碳酸钠,而碳酸钠能够和氯化钡反应生成生成碳酸钡沉淀,可以据此写出该反应的化学方程式为:;CO2+2NaOH═Na2CO3+H2O;Na2CO3+BaCl2═BaCO3↓+2NaCl; (5)一氧化碳有毒,燃烧生成二氧化碳,该气体能产生温室效应,所以一氧化碳不是新能源的发展方向;
(6)根据题意可以知道烧杯中增加的质量即为生成的二氧化碳的质量为1.76g,
设石灰石中含有的碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 1.76g =
=
解得:x=4g
石灰石中杂质的质量分数为: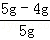 ×100%=20%
×100%=20%
答:石灰石中杂质的质量分数为20%.
考点:一氧化碳的化学性质;二氧化碳的化学性质;碱的化学性质;盐的化学性质;根据化学反应方程式的计算.


科目:初中化学 来源: 题型:计算题
有一矿山上的石灰石样品中只含杂质二氧化硅(二氧化硅是一种既不溶于水,也不与盐酸反应的固体)。小琳和她的同学想测定该样品中碳酸钙的质量分数。他们取一块石灰石样品,将其粉碎后,称出9.4g放入烧杯内(烧杯的质量为60.8g),然后慢慢加入稀盐酸,用玻璃棒搅拌至不再产生气泡为止,共用去稀盐酸97.8g。再称出反应后烧杯及其内物质的总质量为164.7g。试回答:
(1)将石灰石样品粉碎的主要目的是 。
(2)实验结束后,共放出二氧化碳 g(假设溶解在水中的二氧化碳质量忽略不计)。
(3)该石灰石样品中碳酸钙的质量分数是多少?(计算结果精确到0.1%)
(4)反应后溶液的质量为 g。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
现有一瓶标签已破损的过氧化氢溶液,为测定瓶内溶液中溶质的质量分数,取该溶液34g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是34.4g,将杯内剩余物质过滤、洗涤、干燥后得滤渣2g。计算:
(1)生成氧气的质量。
(2)瓶内过氧化氢溶液中溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
烧杯中装有一定量硫酸和硫酸铜的混合溶液,已知该溶液中含H2SO4的质量为9.8g。某同学为测定该混合溶液中硫酸铜的质量,向烧杯中逐渐加入10%的NaOH溶液,得到沉淀的质量记录如下: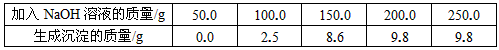
(1)得到沉淀的总质量为 g,该混合溶液中硫酸铜的质量为 g。
(2)参加反应的NaOH溶液的总质量是多少克?(要求写出计算过程)
(3)画出在该混合溶液中加入NaOH溶液质量与生成沉淀质量变化关系的曲线。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
黄铜是一种重要的金属材料,是铜和锌的合金。为了测定某黄铜样品中铜的质量分数,取10g该黄铜样品粉末加入到25g的稀硫酸中,恰好完全反应,测得产生氢气0.1g。试求:
(1)该黄铜样品中铜的质量分数。 (2)所用稀硫酸中溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某锌样品15g加入50g稀硫酸中(杂质既不溶于水,也不与稀硫酸反应),充分反应后,称得烧杯内物质的总质量为64.6g。试计算:
(1)生成氢气的体积。(精确到0.1L,在标准状况下氢气的密度为0.9g/L)
(2)锌粒中所含锌的质量分数(精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
在烧杯中加入氯化钠和碳酸氢钠的固体混合物10.0g后,再加入68.9g稀盐酸恰好完全反应.反应过程用精密仪器测得烧杯连同药品的总质量(m)与反应时间(t)的关系如图所示.烧杯连同药品的起始总质量为165.0g.反应的方程式为:NaHCO3+HCl═NaCl+H2O+CO2↑试回答下列问题:
(1)完全反应时产生二氧化碳的质量为 g
(2)原混合物中氯化钠的质量.
(3)反应后所得氯化钠溶液中溶质质量分数.
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
40g质量分数为36.5%的盐酸与25g大理石恰好完全反应(大理石中的杂质不参加反应).
(1)计算该大理石中碳酸钙的质量分数.
(2)将40g质量分数为36.5%的盐酸稀释为质量分数为10%的盐酸,需要水的质量是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
⑴一定条件下,下列物质在密闭容器内充分反应,反应前后各物质的质量如下:
| 物质 | A | B | C | D |
| 反应前的质量/g | 1.7 | 2.2 | 7.9 | 0.9 |
| 反应后的质量/g | 待测 | 6.6 | 0 | 2.7 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com