
【题目】空气中氧气含量测定的再认识。
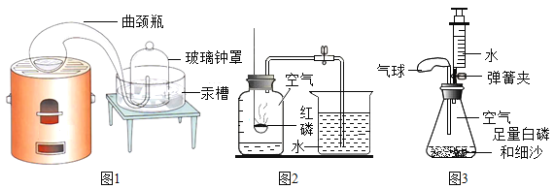
(经典赏析)教材中介绍了拉瓦锡用定量的方法研究了空气的成分(装置如图1),通过该实验拉瓦锡得出了空气中氧气约占_____的结论。
(实验回顾)
(1)实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如图2),兴趣小组用该方法测出的氧气含量常常远低于1/5.其原因可能是_____,_____(写两点)。
(2)由于红磷在空气中点燃后才放入集气瓶内,造成的实验缺陷有:①测定结果不准确;②_____。
(提出问题)能否设计一套实验装置以解决上述缺陷?
(实验改进)兴趣小组同学,设计了如图3所示装置;
(查阅资料)白磷的着火点40℃;
(实验准备)锥形瓶内空气体积为230mL,注射器中水的体积为50mL,该装置气密性良好。
(实验探究)装入药品,按图所示连按好仪器,夹紧弹簧夹,先将锥形瓶底部放入热水中,白磷很快被引燃,然后将锥形瓶从热水中取出。
(现象分析)
①锥形瓶底部放入热水中,白磷被引燃:②整个实验过程中,气球的作用是_____。
③待白磷熄灭,锥形瓶冷却到室温后,打开弹簧夹,还可观察到的现象一是:注射器中的水自动喷射出来,原因是_____。现象二是;当注射器中的水还剩约_____mL时停止流下。
【答案】![]() 红磷量不足 没有冷却至室温就打开止水夹 污染环境 缓冲作用 白磷燃烧消耗瓶中的氧气,使瓶中气压减小 4
红磷量不足 没有冷却至室温就打开止水夹 污染环境 缓冲作用 白磷燃烧消耗瓶中的氧气,使瓶中气压减小 4
【解析】
经典赏析:氧气约占空气总体积的![]() ; 故填:
; 故填:![]() ;
;
实验回顾:
(1)用红磷燃烧的方法测定空气中氧气的含量,测出的氧气含量常常远低于![]() ,其原因可能有多种:①装置漏气(若装置漏气,空气会进入集气瓶,导致瓶内压强较大,水进入就少于
,其原因可能有多种:①装置漏气(若装置漏气,空气会进入集气瓶,导致瓶内压强较大,水进入就少于![]() );②红磷量不足(红磷不足,瓶内氧气消耗不完,进入水也少于
);②红磷量不足(红磷不足,瓶内氧气消耗不完,进入水也少于![]() );③没有冷却至室温就打开止水夹(没完全冷却,瓶内压强仍较大,水进入就少于
);③没有冷却至室温就打开止水夹(没完全冷却,瓶内压强仍较大,水进入就少于![]() );
);
故填: 装置漏气;红磷量不足;没有冷却至室温就打开止水夹(任意两者)
(2)红磷在空气中点燃后再放入集气瓶内,造成的实验缺陷有:燃烧匙伸入集气瓶中时导致部分气体受热膨胀逸出,实验结果不准确;同时反应生成的五氧化二磷扩散到空气中会污染环境;
故填:污染环境;
现象
②在整个实验过程中,因为红磷燃烧放出热量,温度升高,锥形瓶中的气体膨胀,如果没有气球,瓶塞可能被气流顶出;有了气球,气体则会进行气球,避免上述情况发生。因此气球的作用是缓冲作用;
故填:缓冲作用;
③白磷熄灭、锥形瓶冷却到室温后,锥形瓶中的氧气被消耗,压强减小,故打开弹簧夹,注射器中的水自动喷射出来;
故填:白磷燃烧消耗瓶中的氧气,使瓶中气压减小;
当进入锥形瓶中的水的体积等于减少氧气的体积时,内外压强相等,水不再流入。230ml×![]() =46ml,最后注射器中的水还剩约:50ml-46ml=4ml。
=46ml,最后注射器中的水还剩约:50ml-46ml=4ml。
故填:4。


科目:初中化学 来源: 题型:
【题目】某同学在开放性科学实践活动课中,利用如图装置做了“空瓶生烟”的化学小魔术。操作步骤如下:
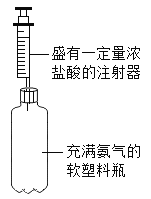
(1)将软塑料瓶中充满氨气,用胶塞塞紧。
(2)用注射器取一定量的浓盐酸。
(3)把注射器针头穿过胶塞,缓缓向瓶中注入浓盐酸,观察到空瓶中产生浓浓的白烟,发生反应的符号表达式为:NH3+HC1→NH4C1。
下列有关说法:①NH4C1为白色固体 ②该反应属于氧化反应 ③会观察到软塑料瓶变瘪的现象,正确的是( )
A.①②B.①③C.②③D.①②③
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A-F是初中化学常见的几种物质,如图为它们的转化关系(部分化学反应的反应条件、反应物、生成物未给出)。已知:A、C组成元素完全相同,且都含有两种元素;C为生活中常见的无色液体:D是一种气体。请回答有关问题:

(1)写出有关物质化学式;C_____,F_____。B物质在反应①中起_____作用。
(2)写出反应①的化学方程式_____。该反应的基本类型是_____。
(3)写出物质D的一种用途_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科学研究发现:氮气不活泼,在3000 ℃时仅有0.1%的分子分裂。在0 ℃常压条件下,向密闭容器M中充入一定量氮气,而后升高温度(不超过300 ℃,压强不变),若该密闭容器的体积增大了一倍,几位同学设想了四种M内分子变化示意图,你认为合理的是( )
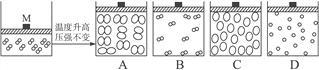
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】写出下列化学式中2的含义。
(1)2H_________。
(2)Mg2+_________。
(3)![]() O ________。
O ________。
(4)H2___________。
(5)2Cl—___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,该实验中有大量的________产生,集气瓶冷却后打开弹簧夹,水倒流入集气瓶中,约占其体积的________。如果进入集气瓶中的水量太少,可能的原因是:(写两条)
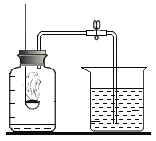
(1)_________________;
(2)_________________;
(3)该反应的化学反应式为:_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】煤是一种化石燃料,用煤作燃料生成的SO2气体会造成环境污染。有一种煤每燃烧1 t就会释放出53.3 kg SO2。如果将产生的SO2用熟石灰来完全吸收,其反应的化学方程式为:SO2+Ca(OH)2====CaSO3+H2O,那么燃烧5 t这种煤产生的SO2在理论上需用多少千克的Ca(OH)2来吸收?(计算结果取整数)__________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com