
【题目】AgNO3固体见光或受热易分解,故保存在棕色瓶中,AgNO3 见光分解时产生一种有刺激性气味的气体,该气体可能是
A. H2S B. SO2 C. N2 D. NO2
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )
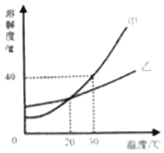
A.30℃时,甲的饱和溶液溶质质量分数为40%
B.20℃时,甲、乙的饱和溶液中所含溶质的质量一定相等
C.将等质量的甲、乙固体,分别配成30℃的饱和溶液,所需水的质量:甲>乙
D.将20℃时甲、乙的饱和溶液升温到30℃,所得甲、乙溶液的溶质质量分数相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工厂以含有FeSO4和少量H2SO4的废水为原料制备FeSO4·7H2O的步骤如下:
①调节废水pH;②过滤; ③蒸发浓缩 ④结晶池中结晶 ⑤收集晶体,洗涤、干燥
(1)调节废水pH时,适宜加入 。(填序号)
A.Fe B.Cu C.Ca(OH)2
(2)实验室中,完成过滤操作需要的玻璃仪器有玻璃棒、 和 ,过滤和蒸发操作中玻璃棒的作用分别是 、 。
(3)结晶池底部有一定坡度是主要目的是 。
(4)用冰水洗涤FeSO4·7H2O晶体的目的是 ,低温干燥的目的是 。
(5)结合下图,补充完整有硫酸亚铁溶液中晶体出FeSO4·7H2O的实验方案:
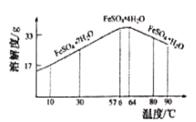
蒸发浓缩, ,过滤、洗涤、干燥。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下面是“燃烧的条件”实验活动的部分操作示意图:

(l)仪器①的名称为___________;
(2)实验一加热片刻观察到A中棉球上的酒精燃烧产生蓝色火焰,B中棉球上的水不燃烧,由此得出燃烧的条件之一是__________;
(3)实验二观察到先燃烧的物质是__________;若将铜片上的物质换成等量的木屑和煤粉进行实验,观察到木屑先燃烧,说明木屑的着火点比煤粉__________;
(4)实验三将燃着的蜡烛放在如图所示的密闭容器中,同时用氧气传感器侧出密闭容器中氧气含量的变化如右图所示,下列说法错误的是_______(填序号)。

A.蜡烛燃烧需要氧气
B.蜡烛燃烧前,密闭容器中氧气的体积分数为21%
C.蜡烛熄灭后,密闭容器中还有氧气
D.蜡烛熄灭后,密闭容器中的二氧化碳体积分数为84%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类制得并利用金属有着悠久的历史:
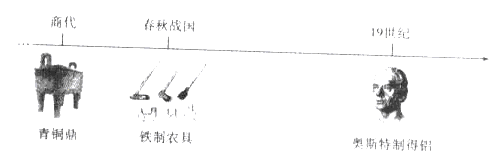
(1)利用孔雀石冶炼铜的主要反应:①Cu2(OH)2CO3![]() 2CuO+H2O+CO2↑,该反应的类型是_____反应(填“化合”、”分解”或“置换”);
2CuO+H2O+CO2↑,该反应的类型是_____反应(填“化合”、”分解”或“置换”);
② 2CuO+C![]() 2Cu+CO2↑,该反应前后铜元素化合价发生的变化是_。
2Cu+CO2↑,该反应前后铜元素化合价发生的变化是_。
( 2 )高炉炼铁的主要反应过程如下.请写出对应的化学方程式:
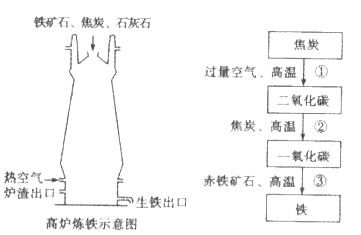
①_________;②_________;③_________。
(3)冶炼金属铝的主要反应:2Al2O3![]() 4Al+3O2↑,该反应的条件是______。下图的装置中,两种金属的活动性:Zn______ Cu (填“>”或“<”)。当电流表指针发生偏转时,化学能转化为______。
4Al+3O2↑,该反应的条件是______。下图的装置中,两种金属的活动性:Zn______ Cu (填“>”或“<”)。当电流表指针发生偏转时,化学能转化为______。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是元素周期表中1-18号元素的原子结构示意图,请回答下列问题:
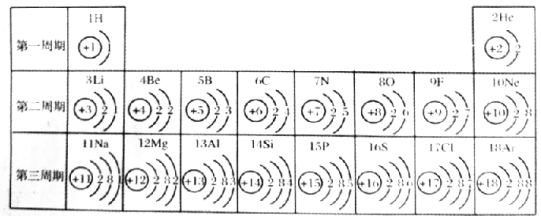
(l)原子序数为17的元素属于______(填“金属”或“非金属”)元素。表中与该元素化学性质相似的元素是_______(填元素名称)。
(2)X3-和氖原子的核外电子排布相同,则X的元素符号是______。
(3)同一周期,从左到右,各元素原子的______依次递增。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学小组欲配制49g溶质质量分数为20%的稀硫酸来进行实验,老师为它们提供了溶质质量分数为98%的浓硫酸(密度为1.84g/cm3)。
(1)通过计算,需要用到溶质质量分数为98%的浓硫酸的质量是____g。
(2)量取浓硫酸时仰视读数(其他操作正确),则配制的稀硫酸的溶质质量分数____(填“大于”、“小于”或“等于”) 20%。
(3)A和B是两个同学稀释浓硫酸操作的示意图,正确的是____(填“A”或“B”)。 . \ }
(4)玻璃棒搅拌的作用是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁的氧化物有三种,分别是FeO、Fe2O3和Fe3O4。某固体粉未可能含有一种或两种铁的氧化物。取23.2克固体粉未,向其中通入足量一氧化碳并加热(假设固体完全反应),将反应生成的气体通入足量的澄清石灰水中。生成40.0克沉淀。试计算:
(l)反应生成二氧化碳的质量为多少克?(要求写出计算过程)
(2)固体粉末中含有的铁的氧化物可能为______或_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】醋的主要成分是醋酸,其化学式为CH3COOH。醋不仅是调味品,而且有较强的灭菌、抑毒的作用。小明为判断家中的9°米醋含酸量是否合格,取l00mL米醋(见标签)于锥形瓶中,然后再向锥形瓶中逐渐加入一定溶质质量分数的碳酸氢钠溶液,反应过程中,当加入碳酸氢钠溶液的质量至以下数值时,对充分反应后锥形瓶中剩余物质的质量进行了记录,测得的部分数据如下,请根据有关信息回答问题:(提示:化学方程式为CH3COOH+NaHCO3=CH3COONa+H2O+CO2↑)
加入碳酸氢钠溶液质量(g) | 25 | 50 | 100 | 155 | 175 |
锥形瓶内剩余物质质量(g) | 123.9 | 147.8 | 195.6 | 248.4 | m |
(l)醋酸中碳、氢、氧三种元素的质量比为_________。
(2)l00mL米醋与足量碳酸氢钠溶液反应产生的二氧化碳质量为_____g,表中m 的数值为____。
(3)请通过计算判断该产品含酸量是否合格?(写出计算过程)

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com