
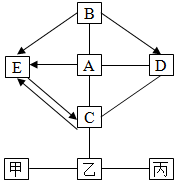
 如图中的物质为初中化学常见物质,他们之间的反应关系如图所示(“→”表示转化关系,“-”表示相互能反应,部分反应物、生成物或反应条件已略去).甲与A溶液反应得到浅绿色溶液;A、B发生中和反应,产物之一是厨房内常用的调味品;C常用于改良酸性土壤,且C的溶液与D的溶液反应可得到B;C的溶液与乙的溶液反应生成蓝色沉淀;乙与丙两种溶液反应生成两种不同颜色的沉淀.请回答:
如图中的物质为初中化学常见物质,他们之间的反应关系如图所示(“→”表示转化关系,“-”表示相互能反应,部分反应物、生成物或反应条件已略去).甲与A溶液反应得到浅绿色溶液;A、B发生中和反应,产物之一是厨房内常用的调味品;C常用于改良酸性土壤,且C的溶液与D的溶液反应可得到B;C的溶液与乙的溶液反应生成蓝色沉淀;乙与丙两种溶液反应生成两种不同颜色的沉淀.请回答:分析 甲与A溶液反应得到浅绿色溶液,A、B发生中和反应,产物之一是厨房内常用的调味品,则A、B发生中和反应生成了氯化钠,又因为A和甲反应生成浅绿色溶液,因此A是稀盐酸,甲是铁,B是氢氧化钠;
氢氧化钙常用于改良酸性土壤,因此C是氢氧化钙,氢氧化钙能和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,碳酸钠能和稀盐酸反应,氢氧化钠能和二氧化碳反应生成碳酸钠,因此D是碳酸钠;
氢氧化钙溶液与乙的溶液反应生成蓝色沉淀,说明乙中含有铜离子,乙与丙两种溶液反应生成两种不同颜色的沉淀,由此可知乙是硫酸铜,丙是氢氧化钡,这是因为硫酸铜和氢氧化钡反应生成白色沉淀硫酸钡和蓝色沉淀氢氧化铜;
氢氧化钠和二氧化碳能够生成水,稀盐酸和氢氧化钠反应能够生成水,氢氧化钙和二氧化碳反应生成能够生成水,因此E是水.
解答 解:甲与A溶液反应得到浅绿色溶液,A、B发生中和反应,产物之一是厨房内常用的调味品,则A、B发生中和反应生成了氯化钠,又因为A和甲反应生成浅绿色溶液,因此A是稀盐酸,甲是铁,B是氢氧化钠;
氢氧化钙常用于改良酸性土壤,因此C是氢氧化钙,氢氧化钙能和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,碳酸钠能和稀盐酸反应,氢氧化钠能和二氧化碳反应生成碳酸钠,因此D是碳酸钠;
氢氧化钙溶液与乙的溶液反应生成蓝色沉淀,说明乙中含有铜离子,乙与丙两种溶液反应生成两种不同颜色的沉淀,由此可知乙是硫酸铜,丙是氢氧化钡,这是因为硫酸铜和氢氧化钡反应生成白色沉淀硫酸钡和蓝色沉淀氢氧化铜;
氢氧化钠和二氧化碳能够生成水,稀盐酸和氢氧化钠反应能够生成水,氢氧化钙和二氧化碳反应生成能够生成水,因此E是水;
(1)甲的化学式是Fe;D的化学式是Na2CO3.
故填:Fe;Na2CO3.
(2)欲通过实验现象观察A和B是否恰好完全反应,实验前需要向B溶液中加入的试剂是酚酞试液,这是因为氢氧化钠溶液中加入酚酞试液时,溶液变红色,随着稀盐酸的滴加,氢氧化钠和稀盐酸反应,当红色刚刚消失时,说明氢氧化钠和稀盐酸恰好完全反应.
故填:酚酞试液.
(3)水能和氧化钙反应生成氢氧化钙,反应的化学方程式为:CaO+H2O=Ca(OH)2.
故填:CaO+H2O=Ca(OH)2.
(4)硫酸铜和氢氧化钡反应生成白色沉淀硫酸钡和蓝色沉淀氢氧化铜,反应的化学方程式为:CuSO4+Ba(OH)2=Cu(OH)2↓+BaSO4↓.
故填:CuSO4+Ba(OH)2=Cu(OH)2↓+BaSO4↓.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A、用“化学”眼光分析 | B、资源的利用和保护 |
| ①洗涤剂去油污是因为起乳化作用 ②气体受压体积缩小是因为气体分子的间隔变小 ③明矾净水是因为明矾溶于水生成胶状物 | ①爱护水资源要节约用水和防止水体污染 ②保护金属资源只能通过防止金属腐蚀实现 ③保护空气要减少有害气体和烟尘的排放 |
| C、物质的分类 | D、“低碳经济”的措施 |
| ①合成橡胶、塑料、合金都属于合成材料 ②由不同种元素组成的物质一定是化合物 ③纯碱、火碱、熟石灰都属于碱 | ①改造或淘汰高能耗、高污染企业 ②研制和开发新能源替代传统能源 ③提倡使用一次性塑料方便袋 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com