
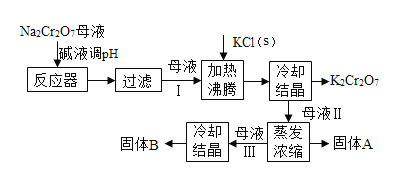
【题目】工业上用重铬酸钠(Na2Cr2O7)结晶后的母液(含少量杂质Fe3+)生产重铬酸钾(K2Cr2O7),其生产流程和相关物质的溶解度曲线及溶解度数据如图(假设流程中反应恰好完全进行):
物质 | 溶解度(g/100g H2O) | ||
0℃ | 40℃ | 80℃ | |
KCl | 28 | 40.1 | 51.3 |
NaCl | 35.7 | 36.4 | 38 |
K2Cr2O7 | 4.7 | 26.3 | 73 |
Na2Cr2O7 | 163 | 215 | 376 |
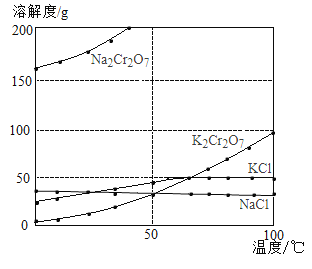
(1)由溶解度曲线可知,50℃时,K2Cr2O7、KCl、NaCl三种物质溶解度的大小关系为_____________,100℃时,用等质量的K2Cr2O7、KCl、NaCl三种固体配制成饱和溶液,溶液质量大小关系为_____________。
(2)将40℃四种物质的饱和溶液降温至0℃,溶质质量分数最小的是______________。
(3)加碱液调节pH的目的是____________。
(4)加入氯化钾固体后,反应的化学方程式为___________。根据溶解度数据可知,该反应能够发生的原因是____________。
(5)流程中要得到母液Ⅲ和固体A的操作为___________,蒸发浓缩原因是___________。
【答案】KCl>K2Cr2O7=NaCl NaCl>KCl>K2Cr2O7 K2Cr2O7 除去Fe3+ Na2Cr2O7+2KCl=K2Cr2O7↓+2NaCl 低温下K2Cr2O7溶解度远小于其他组分,随温度的降低,K2Cr2O7溶解度明显减小 趁热过滤 减少降温造成K2Cr2O7损失
【解析】
(1)根据题中溶解度曲线可知50℃时,K2Cr2O7、KCl、NaCl三种物质溶解度的大小关系为KCl>K2Cr2O7=NaCl;100℃时,K2Cr2O7、KCl、NaCl三种物质溶解度的大小关系为K2Cr2O7>KCl>NaCl,用等质量的三种固体配制成饱和溶液,所需溶剂质量的大小关系为K2Cr2O7<KCl<NaCl,故所得溶液质量大小关系为NaCl>KCl>K2Cr2O7。
(2)四种物质的溶解度均随温度的降低而减小,将40℃四种物质的饱和溶液降温至0℃,此时四种溶液仍为饱和溶液,而0℃时四种物质溶解度的大小关系为Na2Cr2O7>NaCl>KCl>K2Cr2O7,故溶质质量分数最小的是K2Cr2O7。
(3)母液中含少量杂质Fe3+,向Na2Cr2O7母液中加碱液调节pH的目的是除去Fe3+。
(4)低温下K2Cr2O7的溶解度远小于其他组分,随温度的降低,K2Cr2O7的溶解度明显减小,故向重铬酸钠母液中加入氯化钾固体,降温后会析出重铬酸钾晶体,反应的化学方程式为![]() 。
。
(5)母液Ⅱ中含有氯化钠和重铬酸钾,得到母液Ⅲ和固体A的操作为蒸发浓缩、趁热过滤;蒸发浓缩的原因是重铬酸钾在低温时溶解度减小,会造成一定的损失。


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:初中化学 来源: 题型:
【题目】在探究酸和碱的化学性质时,同学们准备了四支试管,分别装入如下图所示的物质,然后加入相应的物质进行实验。回答下列问题。
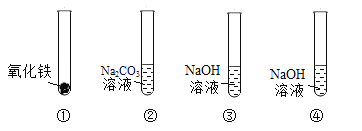
(1)小玉向试管①中加入稀硫酸后观察到的现象是_____,发生反应的化学方程式为_____。
(2)小刚向试管②中滴加稀盐酸后,发现试管中产生无色气泡。小刚对反应后试管中溶液的溶质成分产生了好奇,经过思考后,他提出以下猜想:
I.只含有NaCl
II. NaCl和HCl
III. NaCl和Na2 CO3
IV. NaCl、HCl和Na2CO3
小明认为小刚的猜想_____不合理,理由是_____。
(3)小红向试管③中加入稀盐酸后,没有观察到明显现象。为了证明NaOH溶液能够和稀盐酸发生化学反应,小红提出,可以先向装有NaOH溶液的试管中滴加几滴_____,再加入足量的稀盐酸,就可以观察到_____,从而证明二者发生了化学反应。
(4)小兰向试管④中通入CO2,一段时间后也没有观察到明显现象。她又向试管④中滴加几滴稀盐酸,也没有观察到有气泡产生。于是她得出结论,NaOH溶液与CO2不反应。但是小强不同意小兰的结论,小强的理由是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种具有氧化、吸附、凝聚、杀菌等功能的新型、高效水处理剂。在水体净化的过程中不产生任何有毒、有害的物质,具有广阔的研究开发前景。如图所示是以铁屑为原料制备K2FeO4的工艺流程图:
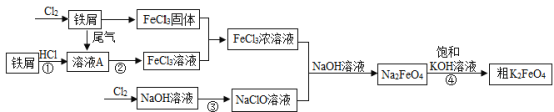
(1)溶液A中溶质的化学式为_____________________。
(2)写出步骤②发生反应的化学方程式_____________________。
(3)向氢氧化钠溶液中通入氯气,二者反应生成NaClO和一种厨房常用调味品以及一种由两种元素组成,质量比为1:8的物质,该反应的化学方程式为_____________________。
(4)步骤④发生的是复分解反应,说明Na2FeO4的溶解度比K2FeO4的溶解度_____________________(填“大”或“小”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D、E、F分别为初中常见的六物质,A、B均为白色固体,C、E均为人类生命活动不可缺少的物质,C、E为气体,D为淡黄色粉末,F与C反应的生成黑色固体,图中“→”表示一种物质能生成另一种物质,“一”表示两种物质能发生反应。下图表示物质之间的反应关系和转化关系,请回答下列问题。
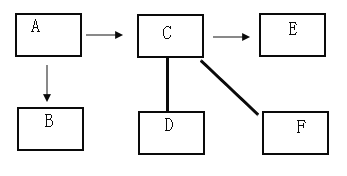
(1)请你写出图中下列物质的化学式或名称:
A_____,C_____,E_____,F_____。
(2)请写出C与D反应的实验现象_____。
(3)请写出A生成C和B的符号表达式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请结合下列实验常用装置,回答有关问题:
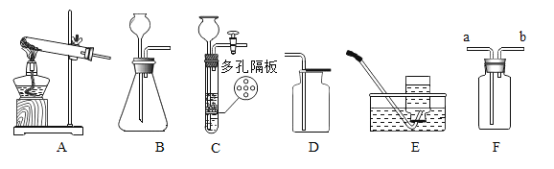
(1)写出装置B和C中相同玻璃仪器的名称______(只写一种)
(2)实验室用高锰酸钾制取氧气,应选用发生装置______(填字母序号),反应的化学文字表达式为______。
(3)若用F装置收集氧气,则气体从______端进入(填“a”或“b”)。写出实验室用过氧化氢制取氧气的化学文字表达式______。
(4)实验室如用块状固体和液体无需加热制取气体,可将B装置改进为C装置(多孔隔板用来放块状固体),其优点是_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列推理正确的是
A.因为钠的相对原子质量比铁的相对原子质量小,所以钠原子的真实质量一定比铁原子真实质量小
B.化合物是由不同种元素组成的,所以由不同种元素组成的物质一定是化合物
C.酸和碱反应生成盐和水,所以与碱反应生成盐和水的物质一定是酸
D.饱和溶液是不能再溶解这种溶质的溶液,所以饱和溶液一定比其不饱和溶液的溶质质量分数大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A-G为初中化学常见的物质,相互关系如图所示,“→”表示转化关系,“—”表示相互之间能反应(部分反应物、生成物已省略)。A是人体胃酸的主要成分,B是侯氏制碱法所生产的碱,C是加剧温室效应的主要气体,D是相对分子质量最小的氧化物,组成G单质的元素在地壳中含量居所有金属元素的第二位。
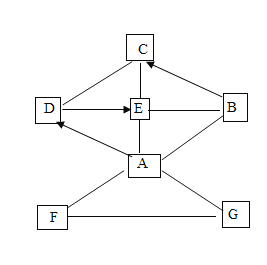
(1)写出化学式:A _____________,E________________。
(2)F所属的物质类别是_____________,G与F反应的化学方程式为_______________。
(3)B转化为C的化学方程式为____________,所属的基本反应类型是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】元素周期表是学习和研究化学的重要工具。图所示是元素周期表的一部分,下列对相关信息表述正确的是
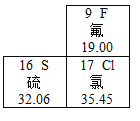
A.氟原子的核内中子数为9
B.氯原子的相对原子质量是35.45 g
C.氟元素和氯元素位于元素周期表的同一周期
D.氟、硫、氯三种元素都属于非金属元素
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种物质的溶解度曲线,据图回答下列问题:
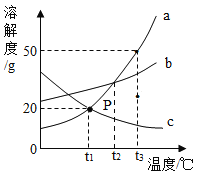
(1)三种物质的溶解度随着温度升高而减小的是____。
(2)t2℃时,物质a的溶解度与物质____的溶解度相等。
(3)t3℃时,把80g物质a加入到200g水中充分搅拌、静置,形成的是_____溶液(填“饱和”或“不饱和”)。
(4)若a中混有少量的b,最好采用____________的方法提纯a。
(5)t3℃时,将等质量a和b的饱和溶液降到t1℃时,析出晶体的质量关系正确的是__(填序号)。
A a>b B a=b C a<b D 不能确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com