
【题目】在探究酸和碱的化学性质时,同学们准备了四支试管,分别装入如下图所示的物质,然后加入相应的物质进行实验。回答下列问题。
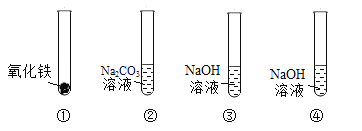
(1)小玉向试管①中加入稀硫酸后观察到的现象是_____,发生反应的化学方程式为_____。
(2)小刚向试管②中滴加稀盐酸后,发现试管中产生无色气泡。小刚对反应后试管中溶液的溶质成分产生了好奇,经过思考后,他提出以下猜想:
I.只含有NaCl
II. NaCl和HCl
III. NaCl和Na2 CO3
IV. NaCl、HCl和Na2CO3
小明认为小刚的猜想_____不合理,理由是_____。
(3)小红向试管③中加入稀盐酸后,没有观察到明显现象。为了证明NaOH溶液能够和稀盐酸发生化学反应,小红提出,可以先向装有NaOH溶液的试管中滴加几滴_____,再加入足量的稀盐酸,就可以观察到_____,从而证明二者发生了化学反应。
(4)小兰向试管④中通入CO2,一段时间后也没有观察到明显现象。她又向试管④中滴加几滴稀盐酸,也没有观察到有气泡产生。于是她得出结论,NaOH溶液与CO2不反应。但是小强不同意小兰的结论,小强的理由是_____。
【答案】红棕色固体逐渐溶解,溶液变成黄色 ![]() IV HCl和Na2CO3能够发生反应,不会共存 无色酚酞溶夜 溶液由红色变成无色 若溶液中的NaOH有剩余,滴入少量的稀盐酸,稀盐酸会先与NaOH反应,就不会观察到有气泡产生
IV HCl和Na2CO3能够发生反应,不会共存 无色酚酞溶夜 溶液由红色变成无色 若溶液中的NaOH有剩余,滴入少量的稀盐酸,稀盐酸会先与NaOH反应,就不会观察到有气泡产生
【解析】
(1)氧化铁会与稀硫酸反应生成易溶于水的硫酸铁,而硫酸铁的溶液显黄色,因此观察到的现象为红棕色固体逐渐溶解,溶液变为黄色,反应的化学方程式为![]() 。
。
(2)HCl 和Na2CO3反应生成NaCl、H2O和CO2气体。因此溶液中一定有NaCl,反应物还可能剩余,所以还可能含有HCI或Na2CO3。但HCl和Na2CO3能够发生反应,不会共存,所以猜测IV不合理。
(3)当酸碱中和反应没有明显现象时,可借助酸碱指示剂的颜色变化等来判断反应是否发生。先向装有NaOH溶液的试管中滴加几滴无色酚酞溶液,溶液会变成红色,再加入过量的稀盐酸,当NaOH被中和后,溶液不再显碱性,溶液的红色会褪去,从而证明者发生 了化学反应。
(4)CO2与NaOH 溶液反应生成易溶于水的Na2CO3,观察不到明显的现象。若溶液中含有剩余的NaOH,即溶液中含有NaOH和Na2CO3两种溶质,滴入少量的稀盐酸,稀盐酸会先与NaOH反应,就不会观察到有气泡产生。


 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:初中化学 来源: 题型:
【题目】自来水消毒过程中常发生两个化学反应,其反应的微观过程可用下图表示,下列说法正确的是
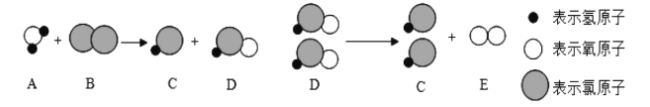
A.C与D的化学性质相比,稳定性强的是D
B.D中氯元素的化合价为-1
C.左边的第一个反应的基本类型是置换反应
D.物质B、E属于单质
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图回答问题:
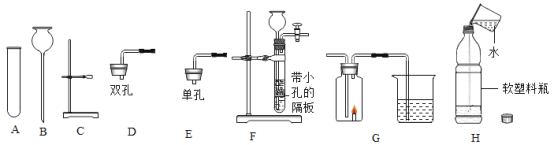
(1)实验室用锌粒和稀硫酸制取氢气,发生装置可选择图中的________(填仪器字母)进行组装,反应的化学方程式为_______________。
(2)某同学连接F、G进行实验,G中所加药品为澄清石灰水。若实验时观察到_______,证明由F制得的气体是CO2;将F中制得的CO2装满在软塑料瓶中,加入约![]() 体积的水,立即旋紧瓶盖,振荡,可能观察到的现象是_______________。
体积的水,立即旋紧瓶盖,振荡,可能观察到的现象是_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用如图所示的实验装置来测定空气里氧气的含量。请回答下列问题:
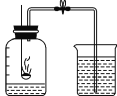
(1)实验的主要操作如下:
①点燃燃烧匙内的红磷后,立即伸入瓶中把塞子塞紧。
②用弹簧夹夹紧乳胶管。
③观察红磷燃烧现象,待红磷熄灭并冷却。
④观察集气瓶中水面的变化情况。
⑤打开弹簧夹。
其正确的实验操作顺序是_________________(填序号)。
(2)某同学采用以上同样的实验装置自主进行实验时,用木炭代替红磷,实验没有成功。请解释原因:________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。
(1)为探究催化剂的种类对氯酸钾分解速率的影响,甲设计以下对比实验:
编号 | 实验药品 | 分解温度(°C) |
Ⅰ | 3.0gKC1O3与1.0gMnO2均匀混合加热 | 150 |
Ⅱ | xg KC1O3与 1. 0g CuO均匀混合加热 | 170 |
Ⅰ中反应的化学方程式是_____________________________。
Ⅱ中x的值应为_____________________________。
[实验结论]实验 所用两种金属氧化物中,催化效果最好的是_____________________________。
(2)乙探究了影响双氧水分解速率的某种因素,实验数据记录如下:
双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2体积 | |
Ⅰ | 50.0 g | 1% | 0.1 g | 9 mL |
Ⅱ | 50.0 g | 2% | 0.1 g | 16mL |
Ⅲ | 50.0 g | 4% | 0.1 g | 31mL |
本实验中,测量O2体积的装置是__________________________________________(填编号)。
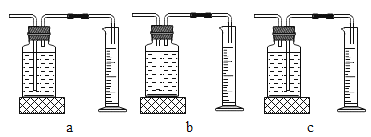
[实验结论]在相同条件下,_____________________________,双氧水分解得越快。/span>
[反思]丙用如图装置进行实验:
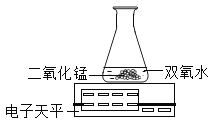
通过比较_____________________________也能达到实验目的。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】相同质量相同形状的铁和锌,分别与等质量,等浓度的稀盐酸反应,产生氢气的量与反应时间的关系如图所示,下列说法正确的是
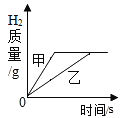
A.乙表示锌与盐酸的反应
B.铁可能与盐酸恰好完全反应,而锌有剩余
C.两个反应消耗金属的质量不相等
D.所得溶液的质量相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属在生活、生产中应用广泛。请回答下列问题:
(1)合金比纯金属的利用更广泛,主要原因是_____ (答一点)。
(2)钢铁材料可以通过铁矿石冶炼生产。请写出工业用赤铁矿炼铁的化学方程式_____。
(3)世界上每年因锈蚀而损失的金属数量巨大。金属资源的保护和回收利用成为科学研究中的重大课题。用含较多铁锈的废铁屑制作动物饲料中的添加剂硫酸亚铁晶体的工艺流程如图所示[已知![]() ]:
]:
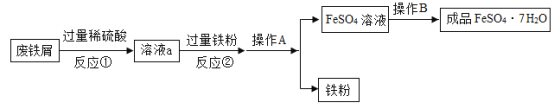
a.操作A的名称是_____。
b.溶液a中的溶质为_____。
c.反应②加入过量铁粉的目的是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属是一种重要的自然资源,回答下列有关金属的问题。
(1)生铁和钢性能不同的原因是_______;
(2)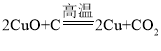 反应中,CuO发生_____反应(填“氧化”或“还原”);
反应中,CuO发生_____反应(填“氧化”或“还原”);
(3)把镁粉和锌粉的混合物放入硝酸银溶液中,充分反应,过滤,得到滤渣和滤液,取滤渣加盐酸,产生气泡,滤渣中一定含有的物质有_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
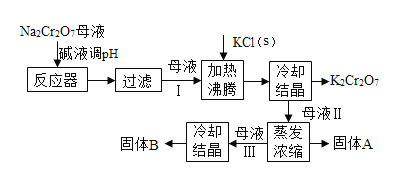
【题目】工业上用重铬酸钠(Na2Cr2O7)结晶后的母液(含少量杂质Fe3+)生产重铬酸钾(K2Cr2O7),其生产流程和相关物质的溶解度曲线及溶解度数据如图(假设流程中反应恰好完全进行):
物质 | 溶解度(g/100g H2O) | ||
0℃ | 40℃ | 80℃ | |
KCl | 28 | 40.1 | 51.3 |
NaCl | 35.7 | 36.4 | 38 |
K2Cr2O7 | 4.7 | 26.3 | 73 |
Na2Cr2O7 | 163 | 215 | 376 |
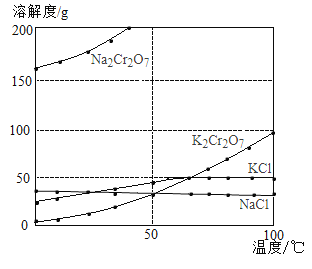
(1)由溶解度曲线可知,50℃时,K2Cr2O7、KCl、NaCl三种物质溶解度的大小关系为_____________,100℃时,用等质量的K2Cr2O7、KCl、NaCl三种固体配制成饱和溶液,溶液质量大小关系为_____________。
(2)将40℃四种物质的饱和溶液降温至0℃,溶质质量分数最小的是______________。
(3)加碱液调节pH的目的是____________。
(4)加入氯化钾固体后,反应的化学方程式为___________。根据溶解度数据可知,该反应能够发生的原因是____________。
(5)流程中要得到母液Ⅲ和固体A的操作为___________,蒸发浓缩原因是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com