
【题目】A~G是初中常见的七种物质,其中A是胃液的主要成分,B、E是无色气体。它们之间的部分关系如图所示(部分反应物、生成物及反应条件已略去,所有反应均在溶液中进行),图中“一”表示相连的两种物质之间可以发生反应,“→”表示一种物质可以通过一步反应转化为另一种物质。请回答下列问题:
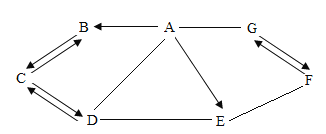
(1)写出下列物质(或溶质)的化学式A:________________E:_______________。
(2)写出G转化为F的实验现象_______________。
(3)写出其中化合反应的化学方程式_______________(一个即可);
(4)将图中未画出的反应关系用“一”补完整。_______________
【答案】HCl CO2 无色溶液中产生白色沉淀 ![]() 或
或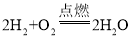

【解析】
A~G是初中常见的七种物质,其中A是胃液的主要成分,则A是HCl;A可转化为B、E,且B、E是无色气体,则为氢气和二氧化碳;A可与D、G反应,则二者可为盐和碱,因为D、E可以反应,则E是二氧化碳,D为一种碱;E、F能发生发应,说明F也为一种碱,F、G可以反应,则F是氢氧化钠、G为碳酸钠;D为氢氧化钙;B为氢气,B、C可相互转化,C、D可以相互转化,则C为水,代入验证,推导正确。
(1) A是稀盐酸,化学式为HCl;E是二氧化碳,化学式是CO2。
(2)碳酸钠与氢氧化钙(合理即可)反应生成碳酸钙和氢氧化钠,现象是无色溶液中产生白色沉淀。
(3)其中化合反应的化学方程式![]() 或
或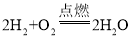 ;
;
(4) C和E、D和G、A和F能发生反应



 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】图中字母代表含硫元素的物质,下列判断错误的是
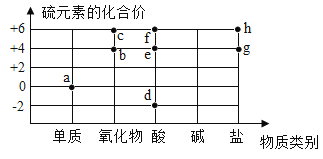
A.物质a在纯氧中燃烧可以生成物质b
B.物质c是二氧化硫
C.物质d中硫元素的化合价为-2价
D.物质d、e和f中一定那含有氢元素
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3)制取绿矾(FeSO4·7H2O),主要流程如下:
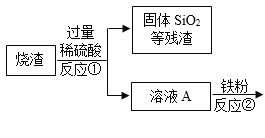
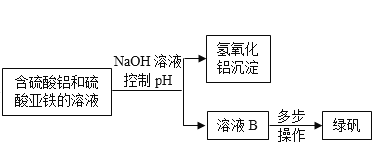
(1)反应①和反应③后都要进行的操作是________________。
(2)反应②中,往溶液A中加铁粉的原因之一是______,写出反应的化学方程式______,此反应的类型是______________。
(3)溶液B中含有的微粒有_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某白色固体可能含有CaCO3、MgCl2、BaCl2、Na2SO4、NaOH中的一种或几种,为了确定其成分,实验过程如下:
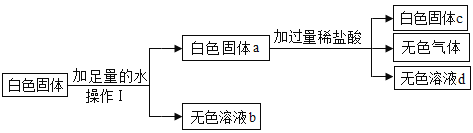
(1)根据题中给出的条件判断,原白色固体中一定含有_____。
(2)为了确定原白色固体中可能存在的物质是否存在,取无色溶液d样品,滴加过量氢氧化钠溶液,若观察到有白色沉淀产生,则原白色固体还含有_____。
(3)若所得的溶液b中只含有一种溶质,对于无色溶液b和白色固体a的用途不合理的是_____。
A除去CaCl2溶液中的稀盐酸:向溶液中加入过量的白色固体a
B鉴别稀盐酸和氢氧化钠溶液:取样,分别滴加无色溶液d
C检验氢氧化钠是否变质:取样,滴加过量的无色溶液d
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体的溶解度曲线如下图所示,t2°C时,分别取含水100g的甲、乙物质的饱和溶液,将其降温至0°C,下列说法中正确的是( )
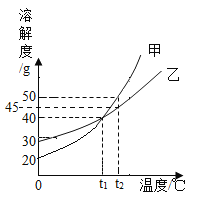
A.t1°C时, 甲的饱和溶液中溶质和溶液的质量比为1:2
B.降温过程中,所得溶液质量甲始终大于乙
C.降温至t1°C时, 所得溶液溶质质量分数相等,且溶液中溶质质量甲等于乙
D.降温至0°C时,溶液中析出固体的质量一定为甲小于乙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】近年比较流行的“自热火锅”给人们生活带来方便。“自热火锅”主要由料包和发热包(主要成分为生石灰、焙烧硅藻土、活性炭、铁粉、铝粉、碳酸钠等)组成,食用方法如图所示。请回答:
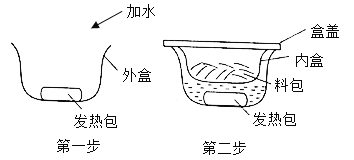
(1)发热包发热的一种原理是生石灰与水反应放热。化学方程式为:_____。
(2)焙烧硅藻土、活性炭都有_____的结构,能起到吸附作用。
(3)“自热火锅”的内、外盒由聚丙烯塑料材质制成,随意丢弃会带来_____问题。聚丙烯塑料属于_____(填字母)
A 金属材料
B 有机合成材料
C 复合材料
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小苏打和食盐是厨房中常见物质。现有一包白色固体,可能由碳酸氢钠、氯化钠中的一种或两种物质组成。某科学小组同学展开了系列研究。
(一)定性分析
(实验目的)确定白色固体的组成
(实验方案):如图1所示
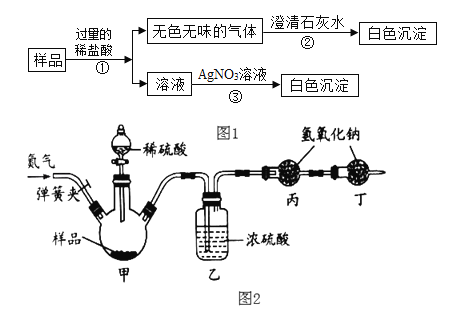
(实验结论)小明同学经过上述实验得出结论:该白色固体由碳酸氢钠、氯化钠两种物质组成。
(1)步骤①发生反应的化学方程式是_____;
(2)步骤②中的澄清石灰水也可以用其它碱溶液代替,如_____;
(3)科学小组认真研究讨论后认为,此方案不能得出小明同学的结论。一致认为将上述方案中使用的一种试剂进行调换,如仍出现上述现象,则小明同学的结论正确。调换措施是_____。
(二)定量分析
(实验目的)测定该白色固体中碳酸氢钠的质量分数
(实验方案)该小组利用图2所示的实验装置(固定装置已略去,装置气密性良好)进行实验,每一步反应均完全进行。
(1)首先称取a克该样品放入装置甲中,然后进行有关实验操作,正确的顺序是_____(填序号,可重复选择)
a.称量装置丙的质量
b.打开弹簧夹,通入足量的氮气,关闭弹簧夹
c.打开分液漏斗的活塞,注入足量的稀硫酸,关闭活塞
(2)如果没有装置乙,会造成测定结果_____(填“偏大”“偏小”或“不变”);
(3)装置丁的作用是_____。
(三)拓展交流
经査阅材料:将二氧化碳气体持续通入一定量的氢氧化钠溶液中会先后发生以下两个化学反应:
①2NaOH+CO2=Na2CO3+H2O ②Na2CO3+CO2+H2O=2NaHCO3
小明同学将5g二氧化碳气体通入100g 5%的氢氧化钠溶液中,充分反应后,所得溶液的溶质是_____(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化铵和硝酸钾溶解度曲线如图所示,下列叙述正确的是( )
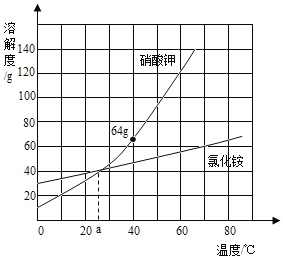
A.硝酸钾的溶解度比氯化铵的大
B.a℃时,氯化铵与硝酸钾溶液中溶质的质量分数相等
C.将20℃的硝酸钾不饱和溶液升温可以变为饱和溶液
D.40℃时,50g水中加入50g硝酸钾,充分搅拌,得到质量分数为39.02%的硝酸钾溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氧化铁(Fe2O3)在工业上又叫氧化铁红,是不溶于水的红棕色粉末,常用于油漆、油墨、橡胶等工业中,也是常用催化剂,在空气中灼烧亚铁化合物或氢氧化铁等可得高纯氧化铁。以下是用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2)为原料制备高纯氧化铁的生产工艺流程。提示信息:(NH4)2CO3溶液呈碱性,40℃以上时(NH4)2CO3分解。
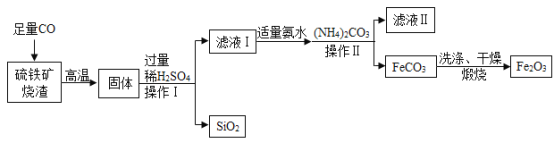
(1)实验室中,步骤I、步骤Ⅱ中实现固液分离的操作为______________。
(2)高温时硫铁矿烧渣中的Fe2O3与CO发生反应的化学方程式为_______________________。
(3)加入(NH4)2CO3后,该反应必须控制的条件是________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com