
实验小组的同学研讨初中常见酸、碱、盐之间的反应关系时,做了如下实验,实验中的每一步均有明显现象,实验操作及部分现象如下图所示.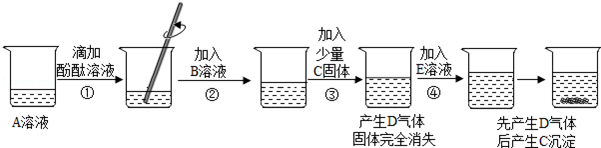 回答下列问题:
回答下列问题:
(1)A溶液一定呈 性(填“酸”或“中”或“碱”).
(2)气体D的化学式为 .
(3)步骤②的实验现象为 .
(4)E溶液中的溶质可能是 .
(5)B溶液的溶质由两种元素组成,④中产生气体的反应的化学方程式为 .
(6)实验后将盛有C固体烧杯中的上清液取出少量,继续加入E溶液,仍有C固体析出,已知A与E中的阳离子相同,则实验后所得溶液含有的溶质为 .
(1)碱;(2)CO2;(3)红色液体变为无色;(4)Na2CO3;(5)Na2CO3+2HCl═2NaCl+H2O+CO2↑;(6)NaCl、CaCl2、酚酞.
解析试题分析:(1)碱遇到酚酞变红,A溶液一定呈碱性;(2)酸和碳酸盐反应放出二氧化碳,气体D的化学式为:CO2;(3)酸性溶液遇到酚酞试液不变色,所以步骤②的实验现象为红色液体变为无色;(4)碳酸钠和酸反应生成二氧化碳,和可溶性钙盐反应生成碳酸钙沉淀,E溶液中的溶质可能是Na2CO3;(5)碳酸钠和盐酸反应生成氯化钠、水和二氧化碳;④中产生气体的反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;(6)实验后将盛有C固体烧杯中的上清液取出少量,继续加入E溶液,仍有C固体析出,说明有氯化钙存在,同时有生成的氯化钠和酚酞,实验后所得溶液含有的溶质为:NaCl、CaCl2、酚酞.
考点:物质的鉴别、推断;酸碱指示剂及其性质;盐的化学性质;书写化学方程式、文字表达式、电离方程式.


科目:初中化学 来源: 题型:探究题
(11分)氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过以下操作流程:
(1)操作①中必须用到的一种仪器是 (填序号)。
A.研钵 B.量筒 C.烧杯 D.试管
(2)小燕完成该实验部分操作过程如图所示,其有明显错误 (填字母序号)。
(3)操作⑤中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外还可采取
等措施。
(4)实验结束后称量获得的精盐,并计算精盐的制得率,发现制得率较低,其可能原因是 (填序号)。
A.食盐没有全部溶解即过滤 B.蒸发时食盐飞溅剧烈
C.蒸发后,所得精盐很潮湿 D.器皿上沾有的精盐没全部转移到称量纸上
(5)小燕查阅相关资料得知:粗盐中除含泥沙等不溶性杂质外,还含有少量的MgCl2、CaCl2等可溶性杂质;为了得到较纯净的氯化钠,小燕将除去泥沙的“精盐”又作了如下处理(假定杂质只有MgCl2、CaCl2两种):
①提供的试剂:Na2CO3溶液、K2CO3溶液、NaOH溶液、KOH溶液、饱和NaCl溶液。
从提供的试剂中选出a所代表的试剂是 、 。
②在滤液中加盐酸的作用是 、 (用化学方程式表示)。
(6)井水中也因为含有较多的MgCl2、CaCl2而不能直接饮用,上海世博园内安装的“直饮水”机,采用“活性炭+超滤层+紫外线”净水工艺。活性炭在此起 作用。
(7)已知硫酸钠的溶解度随温度变化的曲线如右图所示。40℃时,100g蒸馏水中溶解 g
硫酸钠达到饱和。将该饱和溶液升高温度至90℃,
观察到的现象是 。
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
酸、碱、盐是重要的化合物,它们之间能发生复分解反应。
(1)复分解反应发生的条件是有沉淀析出,或有气体放出,或有 生成。
(2)某化学小组进行“酸和碱的中和反应”实验:将盐酸滴入一定量氢氧化钠溶液中,实验无明显现象。为确定反应后溶液中有哪些成分,同学们进行了实验探究。请填写下表:
| 实验操作 | 测定结果 | 溶液成分 |
| ①用pH试纸测定反应后溶液的酸碱度,操作方法是 。 | ②若pH>7 | |
| ③若 | NaCl |

查看答案和解析>>
科目:初中化学 来源: 题型:探究题
某研究性学习小组学习了工业“侯氏制碱法”的原理后,知道如下反应:
NaCl + NH3 + CO2 + H2O = NaHCO3↓+ NH4Cl 。
【提出问题】能否在实验室模拟“侯氏制碱法”制取NaHCO3的过程呢?
【实验验证】如下图是该学习小组进行模拟实验时所用到的部分主要装置和药品。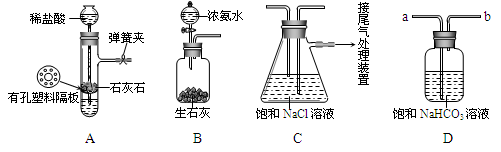
请回答下列问题:
⑴ 检验A装置气密性的方法是:塞紧带长颈漏斗的橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于试管内的水面,停止加水后,若 ,说明装置不漏气。
⑵该实验中用B装置制取的气体是 (填化学式),B装置中盛装浓氨水的仪器名称为 ,本实验中使用该仪器的优点是 。
⑶D是连接在装置A与装置C之间的气体净化装置,进气口是 (填a或b),D的作用是除去HCl气体,反应的化学方程式为 。
⑷实验时先向饱和NaCl溶液中通入较多的NH3(溶液显碱性),再通入足量的CO2,其原因是 (填写序号)。
① 使CO2更易被吸收 ② NH3比CO2更易制取 ③ CO2的密度比NH3大
⑸用 的方法将生成的NaHCO3晶体从混合物中分离出来。
【得出结论】利用“侯氏制碱法”在实验室可以制取NaHCO3 。
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
小明在实验室发现一瓶氢氧化钠固体没有塞上瓶塞,于是他和他的同学一起对这瓶氢氧化钠固体展开探究,请你与他们一起进行探究。
【提出问题】这瓶氢氧化钠固体是否变质?
【查阅资料】CaCl2溶液呈中性。
【猜想与假设】
①氢氧化钠没有变质;②该氢氧化钠部分变质;③该氢氧化钠 。
【设计实验】取氢氧化钠固体样品溶于水配成溶液A,进行如下实验:
| 实验步骤 | 实验现象 | 结论及解释 |
| (1)取少量溶液A于试管中,向其中滴加足量的稀盐酸; | 有气泡产生 | 猜想 不成立 |
| (2)另取少量溶液A于试管中,向其中滴加足量的氯化钙溶液; | 产生 | 反应的化学方程式为: |
| (3)将步骤(2)所得的混合液静置,向上层清液中滴加无色的酚酞溶液。 | 溶液呈红色 | 猜想 成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
已知NaOH容易与空气中的CO2作用而变质。小军同学在实验室发现一瓶敞口放置的NaOH固体后,设计方案,对这瓶NaOH固体变质情况进行了如下实验探究: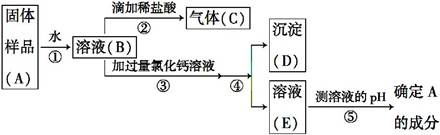
回答下列问题:
1)上述实验操作的名称分别是操作① ,④ 。
2)根据上述实验,可以确定该固体 变质(选填“已”或“未”)。
3)步骤③中加过量氯化钙溶液的目的是 。
4)若测得E的pH=7,则A的成分 ,
若测得E的pH>7,则A的成分 。
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
学完酸碱盐知识后,小美对妈妈焙制糕点用的小苏打很感兴趣,她把小苏打带到实验室与小刚一起进行探究.
(1)小美取少量小苏打溶于水,滴加酚酞试液后,溶液变红,说明小苏打的水溶液显 性;
(2)小刚在烧杯内放入少量小苏打,向其中滴加稀盐酸,立即有 产生,说明小苏打能与酸反应.在医疗上可以用小苏打治疗 ;
(3)小美想:糕点非常松软,是不是小苏打受热分解产生了CO2气体呢?于是她如图装置对小苏打进行加热,一段时间后,导管口的确有气泡冒出,澄清石灰水变浑浊,同时试管口有水珠生成.当导管口不再有气泡产生时,试管内仍有白色固体,她猜测剩余固体可能是:①NaOH;②Na2CO3;③NaCl.小刚认为猜想 一定不正确,理由是 .小刚从试管内取少量白色固体溶于水,滴加酚酞,溶液变红,他判断该固体为NaOH,小美认为他的实验设计不合理,因为 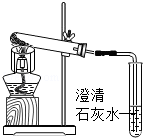
(4)小美和小刚继续探究固体成分,设计了如下实验:
| 操作步骤 | 实验现象 | 结论 |
| 取少量白色固体于试管中,加水溶解,向其中滴加 溶液 | 产生白色沉淀 | 试管内剩余的固体为Na2CO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:信息分析题
(7分)已知下图中A、B、C、D、E、F、G、H是八种固体,A是含有四种元素的盐,C是
厨房中常见的调味品,D、H是黑色固体单质,F是红棕色固体氧化物,乙、丙是组成元素相同的气态氧化物。试推断: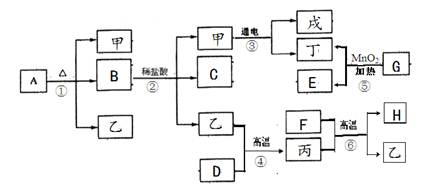
(1)写出A的俗名 ,C的化学式 ,F的化学式 ;
(2)反应③的基本反应类型为 ;
(3)写出②、⑤、⑥的化学方程式
② ,
⑤ , ⑥ 。
查看答案和解析>>
科目:初中化学 来源: 题型:信息分析题
(10分)某粗盐中主要成分为NaCl ,还含有的少量MgCl2、CaCl2和少量泥沙。为了除去杂
质,得到纯净的氯化钠,进行如下实验。
(1)除难溶性杂质。将5g的粗盐溶解于足量水中,需用玻璃棒不断搅拌,目的是 ;进行过滤操作时,需要的玻璃仪器有烧杯、玻璃棒和 ;过滤后,将滤液转移到 (填仪器名称)进行加热蒸发,得到固体精盐4g。若所得精盐的产率偏低,可能的原因是 (填字母)。
A.部分粗盐未溶解 B.蒸发时未使用玻璃棒进行搅拌,导致液滴飞溅 C. 过滤时,滤纸破损了
(2)除可溶性杂质。经过上述操作后,精盐中仍存在少量的MgCl2、CaCl2未除去,现设计如下实验进行提纯,提纯的流程如下:
回答下列问题:
①用NaOH为了除去MgCl2杂质,反应的化学方程式为____________________ _。
②NaOH和Na2CO3如果添加过量了,需往滤液中加入适量___________除去。
③过滤后,所得滤渣中含有的物质是 (填化学式)。
④从滤液中得到氯化钠固体的主要操作是蒸发,为了获得纯净的氯化钠,应蒸发至__ _(填序号)。
A.完全蒸干时停止加热 B.快干时停止加热,利用余热蒸干
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com