
【题目】某大型化工厂处理回收含铜废料的生产流程如下:回答下列问题
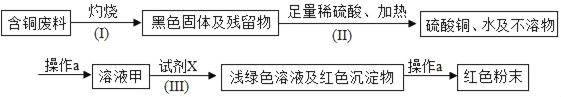
(1)操作a用到玻璃棒,其作用是_____;
(2)流程(Ⅰ)中与铜有关的化学方程式为_____;
(3)流程(Ⅱ)中加入足量稀硫酸的目的是_____;
(4)为达到回收铜的目的,流程(Ⅲ)中加入的试剂X为_____;
(5)工业生产中该流程可能有何缺点?_____。
【答案】过滤 2Cu+O2![]() 2CuO 将氧化铜全部转化成硫酸铜 Fe 红色粉末中混有铁粉,导致铜粉不纯
2CuO 将氧化铜全部转化成硫酸铜 Fe 红色粉末中混有铁粉,导致铜粉不纯
【解析】
由流程图可知:铜和氧气在加热的条件下生成氧化铜,氧化铜和硫酸反应生成硫酸铜和水;不溶性固体与液体分开的方法叫过滤,流程Ⅲ中加入过量的铁粉,铁与硫酸铜反应生成铜和硫酸亚铁;流程中,因为铁粉过量,红色粉末中混有铁粉,导致铜粉不纯。
(1)将固体与液体分离的方法叫过滤;故填:过滤
(2)铜和氧气在加热的条件下生成氧化铜,化学方程式为:2Cu+O2![]() 2CuO;故填:2Cu+O2
2CuO;故填:2Cu+O2![]() 2CuO
2CuO
(3)氧化铜和硫酸反应生成硫酸铜和水,加入过量硫酸是为了将氧化铜全部转化成硫酸铜;故填:将氧化铜全部转化成硫酸铜
(4)流程Ⅲ中加入过量的铁粉,铁与硫酸铜反应生成铜和硫酸亚铁溶液;过滤即可得到铜。故填:Fe
(4)流程中,因为铁粉过量,红色粉末中混有铁粉,导致铜粉不纯。故填:红色粉末中混有铁粉,导致铜粉不纯


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:初中化学 来源: 题型:
【题目】现有盐酸和CaCl2的混合溶液,向其中逐滴滴入Na2CO3溶液,生成沉淀质量与滴入Na2CO3溶液质量的变化关系如右图所示。下列说法错误的是
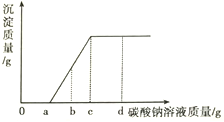
A. 滴加碳酸钠溶液质量为a~c克时,溶液中发生的反应为CaCl2+Na2CO3=2NaCl+CaCO3↓
B. 滴加碳酸钠溶液质量至b克时,溶液中含有三种溶质
C. 滴加碳酸钠溶液质量至a克时,溶液质量比原混合溶液质量大
D. 滴加碳酸钠溶液质量至c克时,溶液呈中性
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验操作符合规范要求,能达到目的是( )
A. 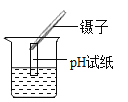 测定溶液的PH
测定溶液的PH
B. 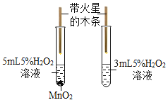 证明MnO2的催化作用
证明MnO2的催化作用
C. 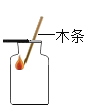 证明CO2已集满
证明CO2已集满
D. 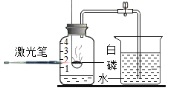 测定空气中O2的含量
测定空气中O2的含量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种不含结晶水的固体的溶解度曲线如图所示.下列说法中正确的是
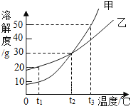
A. t3℃下质量相同的甲、乙饱和溶液分别降温至t2℃,析出的溶质质量相等
B. t2℃时,甲、乙饱和溶液溶质质量分数都为23.1%
C. t3℃时,甲的饱和溶液溶质与溶液的质量比为1:3
D. t1℃时,甲的溶解度大于乙的溶解度
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究性学习小组研究CuSO4溶液与NaOH溶液反应产物的组成与性质。
(信息速递):
1氢氧化铜在80℃时可以完全分解,Cu(OH)2![]() CuO+H2O
CuO+H2O
2碱式硫酸铜为浅绿色固体,化学式为aCu(OH)2·bCuSO4,兼有硫酸铜和氢氧化铜共有的化学性质,温度达653℃时CuSO4开始分解,可表示为 CuSO4![]() CuO+SO3↑,产生的SO3被碱石灰(CaO与NaOH的固体混合物)能完全吸收
CuO+SO3↑,产生的SO3被碱石灰(CaO与NaOH的固体混合物)能完全吸收
3配制波尔多液:1份硫酸铜、1份生石灰和100份水,分别配制硫酸铜溶液和石灰乳,然后将两者在木桶里混合并充分搅拌。
(实验探究):甲、乙同学实验如图:

(现象与分析):
①甲实验中会出现蓝色沉淀,化学方程式为______;乙同学实验中,____用量明显不足,则生成了浅绿色沉淀。
②配制石灰乳时反应的化学方程式为____,不能用铁桶配制波尔多液的原因是____。
(拓展探究):该小组同学欲测定碱式硫酸铜(aCu(OH)2·bCuSO4)的组成,将上述实验中的浅绿色沉淀过滤、洗涤、烘干。
(方案一):沉淀法
③加入足量的稀盐酸,发生了中和反应,反应的化学方程式为____。
④加入过量的氯化钡溶液目的是____。
⑤误差与分析(填“偏大”、“偏小”或“无影响”)
若将BaCl2溶液改为Ba(NO3)2溶液,则a∶b的值将____;
若将样品从天平转移到烧杯中时有少量洒落,则a∶b的值将____。
(方案二):热分解法 该小组同学设计如下图装置,测定9.08 g碱式硫酸铜的组成。

(实验数据)加热至固体完全分解后,测得C装置质量增重2.68g
(问题讨论)
⑥实验前先打开A、B装置之间导气管上玻璃旋塞,缓缓____(填操作),其目的是____;装置D中碱石灰的作用____。
⑦当加热至200℃,装置B中浅绿色固体____(填变化现象);要使得碱式硫酸铜完全分解,控温电加热器需要控制的温度至少达____。
⑧根据上述方案一或方案二的数据,计算a∶b的值。____(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是( )
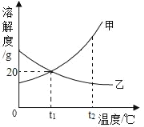
A. t1℃时,甲乙的溶解度相等,它们饱和溶液的溶质质量分数也相等,都为20%
B. t1℃时,30g甲加入到50g水中最多可得80g溶液
C. t2℃,甲、乙两物质的饱和溶液分别降温到t1℃时,所得溶液中溶质质量分数的大小关系是:甲>乙
D. t2℃,等质量的甲、乙两物质的饱和溶液分别降温到t1℃时,所得溶液质量的大小关系为:甲>乙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是实验室制取气体时常用的装置,根据装置回答下列问题:
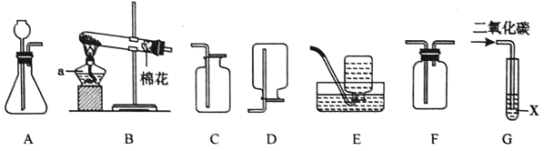
(1)仪器a的名称是____________。
(2)实验室用高锰酸钾制取氧气的发生装置是____(填装置编号,下同),其反应的化学方程式为_______;某同学利用装置E收集气体,但所收集的气体不纯,那么他可能的错误操作是____。
(3)实验室制取二氧化碳的化学方程式为__________,收集装置是________;若用F装置收集二氧化碳,二氧化碳气体应该从_________(填“长”或“短”)导管导入。
(4)图G中,若X是石蕊试液,可观察现象是_________,其原因是_______(用化学方程式表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小川同学用实验探究铁、镁、铜三种金属的活动性顺序时,将有关反应记录如下:
Fe+2HCl=FeCl2+H2↑ Mg+2HCl=MgCl2+H2↑ Fe+CuSO4= FeSO4+Cu Cu+2HCl![]() 不反应
不反应
(1)从上述反应中,可获得的信息有(至少两条)____________;
(2)通过观察实验现象,能说明镁比铁活泼的依据是____________;如果补充一个实验(用化学方程式)___________,也能说明镁比铁活泼。
(3)用金属活动顺序解释生活中的一些现象,如:_____________
(4)使用铁锅有利于人体健康,主要原因是______________
(5)人们大量使用的是合金,这是因为合金具有更多优良性能,如钢比纯铁的硬度_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知碳酸氢钠受热易分解,而碳酸钠热稳定性好.取碳酸氢钠和碳酸钠的混合物10.0g,加热到固体质量不再改变为止,得剩余固体6.9g.下列说法正确的是( )
A. 剩余固体为混合物
B. 反应后生成CO2的质量为3.1g
C. 原混合物中NaHCO3和Na2CO3质量比为21:29
D. 反应前后的固体分别与相同浓度稀盐酸恰好完全反应所需盐酸质量相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com