
【题目】 通过一年的学习,我们认识了很多化学方程式。下列应用和相应的原理及基本反应类型均正确的是
A.酸雨的形成 CO2+H2O====H2CO3 化合反应
B.用过氧化氢溶液制氧气 2H2O2![]() 2H2O+O2 分解反应
2H2O+O2 分解反应
C.用铁制容器盛放稀盐酸 Fe+2HCl=====FeCl2+H2↑ 置换反应
D.误服氯化钡后用硫酸镁解毒 BaCl2+MgSO4======MgCl2+BaSO4↓ 复分解反应
科目:初中化学 来源: 题型:
【题目】空气是一种宝贵的自然资源,要保护空气,防止污染空气。
(1)分离液化空气可获得氮气和_____________两种主要气体;氮气用作保护气,说明氮气_____________________________。
(2)利用膜分离技术,在一定压力下让空气通过具有富集氧气功能的薄膜,能得到含氧量较高的富氧空气,该过程发生_____________变化。
(3)某燃煤电厂富氧燃烧技术原理图如下:

①富氧燃烧与普通燃烧相比,能提供更多的O2,使锅炉中的CO充分燃烧,请写出CO燃烧的化学方程式___________________。
②采用该技术有利于对CO2捕捉、封存和利用,减少碳排放,获得的CO2可用于制干冰,干冰的用途之一是_________________________。捕捉CO2也可用NaOH溶液,请写出对应的化学方程式_______________________________。
③采用图中工艺,可以使煤燃烧产生的氮氧化物和_________气体的排放总量大大下降,从而有效防止了酸雨的形成。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用分子的观点解释下列现象,错误的是
A. 热胀冷缩──分子大小随温度的变化而改变 B. 花香四溢──分子不停地运动
C. 食物腐败──分子发生了变化 D. 水结成冰──分子间隔发生变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“鱼浮灵”主要成分是过碳酸钠(xNa2CO3yH2O2),俗称固体双氧水。兴趣小组对其进行以下探究:
[性质探究]
(1)取少量“鱼浮灵”于试管中加水,有持续细小气泡缓慢放出;向试管中加入少量MnO2粉末,产生大量气泡。将带火星木条伸入试管,木条 ,说明有O2生成。
(2)取实验(1)中上层清液,测得溶液PH>7;向溶液中滴加足量稀盐酸,产生大量气泡;将产生的气体通入澄清石灰水中,出现浑浊现象,说明有 生成。
结论:过碳酸钠具有Na2CO3和H2O2的双重化学性质。
[工业制备]
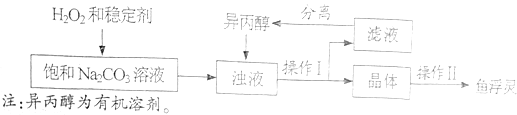
(3)稳定剂的作用是 ;稳定剂中MgCl2和Na2SiO3发生复分解反应,生成一种难溶物将过碳酸钠粒子包裹住,该反应的化学方程式为 。
(4)浊液中加入异丙醇的作用是 。
(5)操作Ⅱ中洗涤晶体的试剂最好选用 (填字母)。
A.饱和NaCl溶液 B水 C异丙醇 D稀盐酸
(6)根据下表数据,你认为上述制备反应的最佳温度范围是 ℃。
温度范围/℃ | 5~10 | 10~15 | 15~20 | 20~25 |
活性氧含量/% | 13.94 | 14.02 | 15.05 | 14.46 |
“鱼浮灵”的产率/% | 85.49 | 85.78 | 88.38 | 83.01 |
注:活性氧含量是指产品中能转化为O2的氧元素的质量分数。
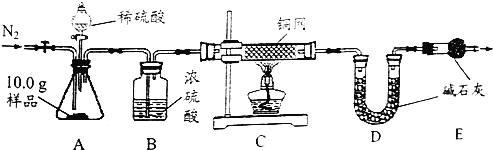
[组成测定]利用下图装置进行产品中活性氧含量测定和过碳酸钠(xNa2CO3yH2O2)组成的测定(杂质对测定无影响)。
查阅资料:①“鱼浮灵”中活性氧含量≥13.0%是一等品,≥10.5%是合格品。
②过碳酸钠能与酸反应放出CO2和O2。
(7)实验前先缓慢通N2一段时间,加热铜网至红热后,再缓慢滴入过量稀硫酸,直至A中样品完全反应;继续缓慢通N2,其目的是 。
(8)若先滴入稀硫酸,后加热铜网,会导致x:y的值 (填“偏大”或“偏小”)。
(9)装置B的作用是 (填序号)
①除去气体中的水蒸气 ②便于观察和控制气流速度
(10)实验测得C装置中铜网增重1.2g,D装置增重2.2g。该产品中活性氧含量为 %;属于 (填“一等品”或“合格品”);x:y= 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(5分)金属在生产生活中得到广泛应用。
(1)铝可以制成铝箔,这是利用了金属铝具有良好的 。
(2)铁制品生锈的条件是 ,可以用稀酸清除铁锈,写出清除铁锈的化学方程式 。
(3)我国是世界上最早采用湿法冶金提取铜的国家,铁和硫酸铜溶液反应的化学方程式为 。
(4)现有两种金属单质组成的混合物。向100 g某稀盐酸中加入该混合物,混合物的质量与生成氢气的质量关系如图所示。

下列说法不正确的一项是 。
a.若混合物为Zn、Al,则m可能是0.2 g
b.若混合物为Zn、Cu,则m=0.2 g
c.若混合物为Fe、Al,则稀盐酸中溶质质
量分数一定大于7.3%
d.若混合物为Fe、Cu,m=0.1 g,则混合物中Fe的质量分数为50%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分析推理是化学学习过程中的常用方法。下列推理正确的是
A.纯碱的水溶液呈碱性,所以纯碱属于碱类
B.分子、原子可以构成物质,所以物质一定是由分子、原子构成的
C.酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
D.化合物是含有不同种元素的纯净物,所以含有不同种元素的纯净物一定是化合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硒对人体有防癌、抗癌作用,如图1是硒元素在元素周期表中的部分信息,图2是硒原子的结构示意图,请回答:

(1)硒是人体必需的 (“微量”或“常量”)元素.
(2)由图1可知,硒元素的相对原子质量是 .
(3)图3中A、B、C三种元素中与硒元素化学性质相似的是 (“A”、“B”或“C”)元素.
(4)图3中C元素原子在化学反应中容易 (“得到”或“失去”)电子,该元素与人体内含量最高的金属元素形成化合物的化学式为 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(8分) 水是生命之源,也是人类最宝贵的资源。用你学过的化学知识回答下列问题:
(1)欲除去水中不溶性杂质,需进行过滤操作,该操作过程中玻璃棒所起的作用是 。
(2)硬水中含有较多可溶性钙、镁化合物,硬水会给生活和生产带来许多麻烦。区分软水和硬水常用的物质是 ,生活中可用 来降低水的硬度。
(3)根据下图回答下列问题。

① 试管A中的气体的名称是 ,写出电解水反应的符号表达式 ,该实验证明水是由
两种元素组成的。
(4) 淡水资源有限,要节约用水,你认为可采取哪些节水措
施(举1例)? 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com