
| 实验步骤 | 实验现象 | 结论 |
| 剪下一片变黑的铜片,放入盛有足量稀硫酸的试管中,微热 | 铜片表面黑色固体全部消失,露出红色的铜,溶液变色. | 此黑色固体是(填化学式) |


 学业测评一课一测系列答案
学业测评一课一测系列答案科目:初中化学 来源: 题型:
| 实验步骤 | 实验现象 | 结论 |
| 剪下一片变黑的铜片,放入盛有足量稀硫酸的试管中,微热 | 铜片表面黑色固体全部消失,露出红色的铜,溶液变 蓝 蓝 色. | 此黑色固体是 CuO CuO (填化学式) |
查看答案和解析>>
科目:初中化学 来源: 题型:
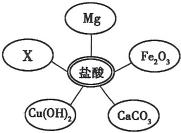 (2011?吉林)同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行探究.
(2011?吉林)同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行探究.| 方案 | 加入试剂 | 分离方法 | 方案评价 |
| 适量Ca(NO3)2溶液 | 过滤、蒸发结晶 | 不可行,理由是 引进新杂质(或有NaNO3,生成或引进NO根离子) 引进新杂质(或有NaNO3,生成或引进NO根离子) | |
| 过量的 盐酸(或稀HCl或HCl) 盐酸(或稀HCl或HCl) | 蒸发结晶 | 可行 |
查看答案和解析>>
科目:初中化学 来源: 题型:
(2011?大庆)同学们为探究不同金属的活动性强弱,设计了如下实验方案,下列方案中实验设计、现象、结论均正确的一组是( )
|
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤 | 观察到的现象 |
| ①在试管中取少量盐酸,插入铁丝,充分作用 | 有气泡冒出,溶液变为浅绿色 有气泡冒出,溶液变为浅绿色 |
| ②在①所得的溶液中,插入 铜丝 铜丝 ,充分作用. |
无明显现象 |
| ③在②所得的溶液中插入 铝丝 铝丝 ,充分作用. |
铝丝表面有一层黑色物质 铝丝表面有一层黑色物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com