
【题目】氯化钠是日常生活中的必需品,某氯化钠样品中除含氯化钠外,还含有少量的CaCl2和MgCl2以及不溶性杂质,以下是提纯该样品的操作流程图
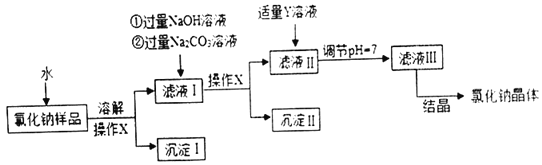
下列说法不正确的是( )
A. 操作X的名称是过滤
B. Y溶液中溶质的化学式是HCl
C. 上述操作流程中共发生3个复分解反应
D. 该流程发生的化学反应中,NaOH+HCl=NaCl+H2O属于中和反应
科目:初中化学 来源: 题型:
【题目】同学们从山上采集到一种石灰石样品,为了测定石灰石样品中碳酸钙的质量分数(石灰石中的杂质不与盐酸反应,也不溶于水),取45g石灰石样品,逐渐加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示,请计算:

(1)45g这种石灰石样品中碳酸钙的质量是_____g
(2)本实验是否可以用稀硫酸代替稀盐酸完成实验,并说明理由_____。
(3)列式计算45g石灰石与稀盐酸恰好完全反应时,所得溶液中溶质的质量分数?_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
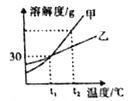
A.甲物质的溶解度大于乙物质的溶解度
B.两种物质的溶解度都随着温度的升高而增大
C.t1℃时,60g甲加入到100g水中,充分溶解,得到160g溶液
D.甲、乙的饱和溶液从t2℃降温到t1℃,析出晶体的质量:甲一定小于乙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象中有关量的变化趋势与对应叙述关系正确的是( )
A. 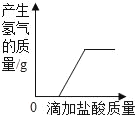 向一定质量表面生锈的铁片中滴加盐酸至过量
向一定质量表面生锈的铁片中滴加盐酸至过量
B. 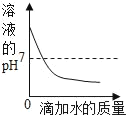 向一定质量的稀硫酸中滴加水
向一定质量的稀硫酸中滴加水
C. 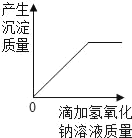 向硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液
向硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液
D. 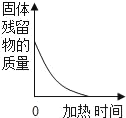 加热高锰酸钾
加热高锰酸钾
查看答案和解析>>
科目:初中化学 来源: 题型:
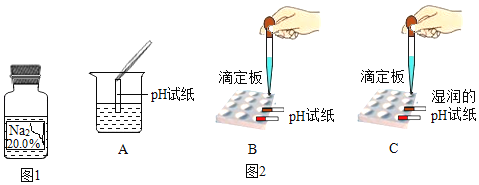
【题目】实验室中有一瓶标签受损的无色溶液,如图1所示,老师提示这是一瓶初中常用的溶液,要求同学们确认其溶质成分。
【提出猜想】①氯化钠②氢氧化钠③硫酸钠④碳酸钠
【查阅资料】氯化钠和硫酸钠溶液pH=7可溶性硫酸盐遇到可溶性的钡盐会产生白色沉淀。
【讨论分析】经过讨论,同学们一致认为猜想_____(填序号)不成立,其原因是_____。
【实验探究】为了进一步确认其成分,同学们继续进行探究:
实验步骤 | 实验现象 | 实验结论 |
(1)取该溶液少许于试管中,向其中滴加稀盐酸 | 无明显现象 | 猜想_____不成立 |
(2)取该溶液少许于试管中,向其中滴加氯化钡溶液 | _____________ | 猜想③成立 |
假如猜想④成立,写出(1)中发生的反应方程式_____。
【反思与交流】有同学提出用测pH的方法也可以确定该无色溶液,如图2所示是几位同学的实验过程,其中正确的是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校社会大课堂活动组织同学们走进了污水处理厂。

(1)参观污水的第一道处理工序时,现场弥漫着难闻的气味,同学们不禁掩住口鼻。从微粒的角度说明能闻到气味的原因是________。
(2)污水的第一道处理工序是经过格栅,格栅是带有规则分布的方形网格,其作用是_______。
(3)二次沉淀池的主要作用是分离出活性污泥。活性污泥的作用是利用微生物将污水中的一些有害物质在氧气的作用下经过生物降解转化为沼气。沼气(主要成分为甲烷)可作为能源使用。沼气燃烧的化学反应方程式为____。
(4)某工厂在排放含硫酸的酸性废水时用氢氧化钠进行处理,其反应的化学方程式为_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据KNO3、NaCl两种物质的溶解度曲线,回答下列问题:

(1)20℃时,KNO3的溶解度约为_____g。
(2)在10℃时,将25gKNO3放入100g水中,充分搅拌后,所得溶液中溶质的质量分数为_____。
(3)KNO3溶液中混有少量的NaC1,要得到较纯净的KNO3,提纯过为:蒸发浓缩、_____,再过滤。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人体缺乏维生素C(简称Vc)可能患坏血病,如图为某种“维生素C”说明书的一部分,请回答:

(1)“Vc”属于_____(填“有机”“无机”)化合物。
(2)“Vc”中碳氢氧原子的个数比是_____。
(3)“Vc”中含量最高的是_____元素。
(4)若正常成年人每天最低需要补充“Vc”60mg时,这些“Vc”完全由图中“维生素C”来补充时,则每次至少服用_____片。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学小组同学对NaOH的化学性质进行如下实验探究。
实验一:NaOH溶液与CO2的反应,装置及实验测定结果如下
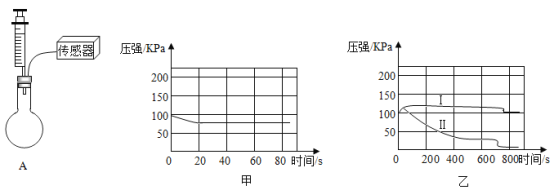
(1)某同学检验A装置气密性(夹持仪器省略),甲图象说明装置气密性良好,该同学进行的操作是_____。
(2)在烧瓶中充满CO2图乙是用注射器向瓶中分别注入同体积水和NaOH溶液得到的压强变化图象,其中表示CO2与NaOH溶液发生反应的是_____(填“Ⅰ”或“Ⅱ”),该反应的化学方程式为_____。
实验二:NaOH溶液与Fe2(SO4)3溶液的反应
(3)实验操作如图B所示,反应的化学方程式为_____。

(4)充分反应后得到的无色溶液中一定含有的离子是_____(填离子符号)。
实验三:NaOH溶液与盐酸的反应
室温下,取10份相同体积溶质质量分数为10%的NaOH溶液于10个烧杯中,分别滴加一定体积溶质质量分数为10%的盐酸,并测定溶液温度,记录数据如下:
加入盐酸体积/mL | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
测得溶液温度 | 25.2 | 28.6 | 32.0 | 36.0 | 38.2 | 36.7 | 35.7 | 34.7 | 33.7 | 32.9 |
(5)加入盐酸体积在12﹣20mL之间时,溶液温度下降的原因可能是①_____②_____。
(6)根据碱与酸反应的性质,可将Al(OH)3制成抗胃酸(主要成分为HCl)药剂,请回答:
①Al(OH)3的相对分子质量_____。
p>②0.25g Al(OH)3能消耗胃酸中的HCl_____g(结果精确到0.01)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com