
分析 向盐酸和MgSO4溶液中加入Ba(OH)2后,Ba2+与溶液中的SO42-反应生成既不溶于水又不溶于酸的BaSO4沉淀,OH-先跟盐酸的H+发生中和反应;若OH-先和Mg2+产生沉淀Mg(OH)2,由于HCl的存在,HCl能将生成Mg(OH)2溶解,故OH-先跟盐酸的H+反应,待H+完全反应,OH-与Mg2+开始生成Mg(OH)2沉淀.
解答 解:(1)硫酸镁与氢氧化钡反应生成氢氧化镁和硫酸钡,化学方程式为:MgSO4+Ba(OH)2═BaSO4↓+Mg(OH)2↓
(2)向盐酸和MgSO4溶液中加入Ba(OH)2后,Ba2+与溶液中的SO42-反应生成既不溶于水又不溶于酸的BaSO4沉淀,OH-先跟盐酸的H+发生中和反应;若OH-先和Mg2+产生沉淀Mg(OH)2,由于HCl的存在,HCl能将生成Mg(OH)2溶解,所以刚开始向混合液中滴入少许Ba(OH)2溶液时,产生沉淀的化学式为BaSO4;
(3)50g质量分数分别为7.3%盐酸和24%MgSO4的混合溶液中,氯化氢的质量=50g×7.3%=3.65g,硫酸镁的质量=50g×24%=12g;向盐酸和MgSO4溶液中加入Ba(OH)2后,Ba2+与溶液中的SO42-反应生成既不溶于水又不溶于酸的BaSO4沉淀,OH-先跟盐酸的H+发生中和反应,待H+完全反应,OH-与Mg2+开始生成Mg(OH)2沉淀;
设与3.65g氯化氢完全反应,需要质量分数为3.42%的Ba(OH)2的质量为x,
2HCl+Ba(OH)2═BaCl2+H2O
73 171
3.65g 3.42%×x
$\frac{73}{3.65g}$=$\frac{171}{3.42%×x}$
x=250g
Ba(OH)2溶液体积为:$\frac{250g}{1.0g/c{m}^{3}}$=250cm3=250mL
(4)当2HCl+Ba(OH)2═BaCl2+H2O,BaCl2+MgSO4═BaSO4↓+MgCl2,由以上两个方程式得出关系式:2HCl~BaSO4~MgSO4~MgCl2
设生成硫酸钡的质量为x,反应掉的硫酸镁的质量为y,生成的氯化镁质量为z
所以:2HCl~BaSO4~MgSO4~MgCl2
73 233 120 95
3.65g x y z
$\frac{73}{3.65g}$=$\frac{233}{x}$=$\frac{120}{y}$=$\frac{95}{z}$
解得:x=11.65g y=6g z=4.75g
这时的溶液是硫酸镁和氯化镁的混合溶液,当加入氢氧化钡溶液时产生了硫酸钡沉淀和氢氧化镁沉淀;当硫酸镁完全反应后,再加入氢氧化钡溶液时只产生氢氧化镁沉淀,当氯化镁完全反应后再加入氢氧化钡溶液时 不再产生沉淀.溶液中硫酸镁的质量为12g-6g=6g;
设6g的硫酸镁与氢氧化钡反应生成的生成的硫酸钡为p,氢氧化镁为q,氢氧化钡溶液的质量为m
MgSO4+Ba(OH)2═BaSO4↓+Mg(OH)2↓
120 171 233 58
6g m p q
$\frac{120}{6g}$=$\frac{171}{m}$=$\frac{233}{p}$=$\frac{58}{q}$
解得:m=250g p=11.65g q=2.9g
当加入250g+250=500g的Ba(OH)2溶液时产生的是硫酸钡和氢氧化镁沉淀,沉淀质量为11.65g+11.65g+2.9g=26.2g;
故答案为:
(1)MgSO4+Ba(OH)2═BaSO4↓+Mg(OH)2↓
(2)BaSO4
(3)250mL
(4)26.2g
点评 解答本题的关键是分清:当溶液中含有盐酸时,加入氢氧化钡溶液,不产生氢氧化镁沉淀,只产生硫酸钡沉淀;当溶液中的盐酸完全反应了,这时加入氢氧化钡溶液产生的沉淀是氢氧化镁和硫酸钡的混合物


 天天练口算系列答案
天天练口算系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
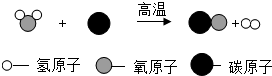 为减少污染、提高煤的利用率,可将其转化为可燃性气体,其微观示意图如图所示,下列说法正确的是( )
为减少污染、提高煤的利用率,可将其转化为可燃性气体,其微观示意图如图所示,下列说法正确的是( )| A. | 图中表示化合物的是“ ” ” | |
| B. | 该反应类型为分解反应 | |
| C. | 该反应中反应物两种微粒的个数比为1:1 | |
| D. | 反应前后分子的种类和数目保持不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氯化钠是由钠离子和氯离子构成的 | B. | 汞是由汞原子构成的 | ||
| C. | 干冰是由碳原子和氧原子构成的 | D. | 金刚石是由碳原子构成的 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 1g和9g | B. | 3g和7g | C. | 2g和8g | D. | 4g和6g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com