
| 实验 步骤 | ① | ② | ③ |
| 实验 现象 | 溶液变为红色 | 稀酸中的铁片表面都有气泡产生; 铜片表面都没有明显现象 | 溶液由红色变为无色 |
| 分析 与 结论 | 结论:稀酸能与指示剂作用 | 铁与稀硫酸反应的化学方程式为 Fe+H2SO4═FeSO4+H2↑ 结论:稀酸能与较活泼金属反应 | 结论: 酸能与碱发生中和反应 |
分析 【实验目的】从后面是实验内容和结论可以分析出本实验目的.
【实验内容】根据酸的化学性质回答,①酸能使紫色石蕊试液变红,②酸能与活泼金属反应放出氢气,③酸碱能发生中和反应生成盐和水.
【实验思考】酸具有通性的原因是酸中都含有氢离子,即氢元素.
解答 解:【实验目的】可根据该实验的内容及其结论逆向推导为:探究稀酸的通性.
【实验内容】根据实验步骤的内容依次判断,步骤①:石蕊试液分别滴入稀硫酸、盐酸中,溶液都变为红色;步骤②:铁在金属活动性顺序中排在H的前面,铁能置换稀硫酸或盐酸里的氢,反应时铁片表面都有氢气的气泡产生,铁与稀硫酸反应生成硫酸亚铁和氢气;步骤③:在含有酚酞试液的氢氧化钠溶液中分别滴入盐酸和稀硫酸,溶液由红色变为无色,说明酸能与碱反应.
【实验思考】从物质组成的角度解释稀酸具有酸的通性的原因是酸都含有氢元素.
故答案为:【实验目的】探究(或认识)稀酸的通性;
【实验内容】
| 实验步骤 | |||
| 实验现象 | 红 | 气泡 | |
| 分析与结论 | Fe+H2SO4═FeSO4+H2↑ | 与碱发生中和反应 |
点评 学会从现象得出结论,有结论推出物质的性质,进而找出物质具有此性质的原因,这是认识物质的方法.


科目:初中化学 来源: 题型:选择题
 要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )
要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )| A. | ①②③ | B. | ①②④ | C. | ②③④ | D. | ①③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 碳在氧气中燃烧发出白光,生成二氧化碳 | |
| B. | 镁在空气中燃烧发出耀眼的白光,生成白色固体 | |
| C. | 细铁丝在氧气中燃烧,火星四射,生成黑色固体 | |
| D. | 硫在空气中燃烧,发出淡蓝色火焰,生成有刺激性气味的气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 含硫物质 | K2SO4 | MnSO4 | CaSO4 | CaSO3 | FeSO4 | Fe2(SO4)3 |
| 溶解性 | 溶 | 溶 | 微溶 | 难溶 | 溶 | 溶 |
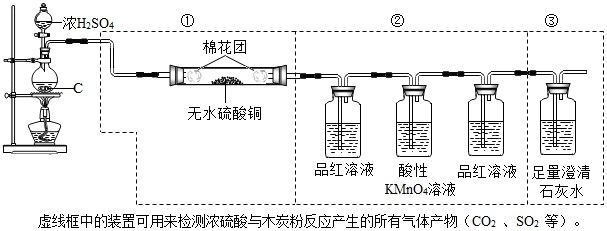
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com