
| 实验步骤 | 实验现象 | 结 论 |
| ①取混合后的白色粉末于试管中,滴加稀盐酸,将产生的气体通入澄清的石灰水. | 有气体产生 澄清的石灰水变浑浊 |
混合后的白色粉末中可能有: 碳酸钠、碳酸氢钠、碳酸钙 |
| ②取混合后的白色粉末于试管中,加水充分溶解. | 试管底部有难溶物出现,试管外壁无明显变化 |
混合后的白色粉末中一定有: 碳酸钙 一定没有: 氢氧化钠 |
| ③取步骤②的上层清液于试管中,滴加酚酞试剂. | 溶液变成红色 |
混合后的白色粉末中 可能有碳酸钠或碳酸氢钠 |


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:阅读理解
| 实验步骤 | 实验现象 | 结论 |
在小木条上蘸少量浓硫酸,放在玻璃片上观察 在小木条上蘸少量浓硫酸,放在玻璃片上观察 | 小木条变黑(或碳化) 小木条变黑(或碳化) | 浓硫酸有强烈的腐蚀性,使用时应十分小心 |
| 采取措施 | 依据原理 | 效果评价 | 反应类型 |
| 向硫酸所流经范围抛撒大量氢氧化钠小颗粒 | 硫酸与氢氧化钠反应 | 将硫酸转化为无害物质,可消除污染 | 复分解反应 复分解反应 |
| 采取措施 | 依据原理 | 效果评价 |
向硫酸所流经范围抛撒大量氢氧化钙粉末 向硫酸所流经范围抛撒大量氢氧化钙粉末 | 硫酸与氢氧化钙反应 硫酸与氢氧化钙反应 | 将硫酸转化为无害物质,可消除污染 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验步骤 | 实验现象 | 结论 |
在小木条上蘸少量浓硫酸,放在玻璃片上观察 |
小木条变黑(或碳化) |
浓硫酸有强烈的腐蚀性,使用时应十分小心 |
| 采取措施 | 依据原理 | 效果评价 | 反应类型 |
| 向硫酸所流经范围抛撒大量氢氧化钠小颗粒 | 硫酸与氢氧化钠反应 | 将硫酸转化为无害物质,可消除污染 | 中和反应 或复分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 清洁剂 | 彩漂液 |
漂白水 |
| 功 能 | 漂洗衣物,使色彩鲜艳 | 漂除衣物污渍 |
| 有效成分 | H2O2 | NaClO |
| ||
| ||

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 “水是生命之源”.请回答下列与水有关的问题:
“水是生命之源”.请回答下列与水有关的问题:| 加热 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 亚硝酸钠 | 氯化钠 | |
| 溶解性 | 15℃时溶解度为81.5g | 15℃时溶解度为35.8g |
| 熔点 | 271℃ | 801℃ |
| 沸点 | 320℃时发生分解,有氧气等气体产生 | 1413℃,不易分解 |
| 实验装置 | 实验主要过程 |
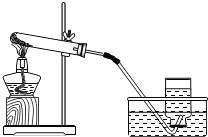 |
①检查装置气密性.操作如下:先将导管伸入液面下,用手紧握试管.观察到 ②加入药品,加热,导管口有大量气泡生成 ③收集气体. ④停止加热.熄灭酒精灯前,应 |
| 实验操作步骤 | 实验现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com