
����Ŀ���Ȼ�����һ����Ҫ�Ļ���ԭ�ϡ�����Ȼ�����Һ���Ƶ��������������ƺ���������Ӧ�Ļ�ѧ����ʽΪ2NaCl+2H2O![]() Cl2��+H2��+2NaOH����ȡһ���������Ȼ�����Һ���е�⣬���Ȼ�����ȫ��Ӧʱ���õ�85.4g��Һ������������������ʱ��Ĺ�ϵ��ͼ��ʾ�������:
Cl2��+H2��+2NaOH����ȡһ���������Ȼ�����Һ���е�⣬���Ȼ�����ȫ��Ӧʱ���õ�85.4g��Һ������������������ʱ��Ĺ�ϵ��ͼ��ʾ�������:
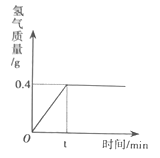
(1)�Ȼ�����ȫ��Ӧʱ����������������_________g��
(2)�Ȼ�����ȫ��Ӧʱ�������������Ƶ�������_________��?
(3)ԭ�Ȼ�����Һ�����ʵ�����������_________?
���𰸡� 0.4 16 23.4%
�����������ݷ�Ӧ�Ļ�ѧ����ʽ�����ṩ�����ݼ���������1����ͼ��֪���Ȼ�����ȫ��Ӧʱ������������������0.4g����2���������������Ƶ�������x����������������Ϊy���Ȼ��Ƶ�����Ϊz��
2NaCl+2H2O![]() Cl2��+H2��+2NaOH
Cl2��+H2��+2NaOH
117 71 2 80
z y 0.4g x
![]()
x=16g
y=14.2g
z=23.4g
��3��ԭ�Ȼ�����Һ�����ʵ���������Ϊ![]() ��100�� =23.4%
��100�� =23.4%
��(2)�Ȼ�����ȫ��Ӧʱ�������������Ƶ�������16����(3)ԭ�Ȼ�����Һ�����ʵ�����������23.4%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɰ��������ѧ�����ϵ�һ���ش�ͻ�ƣ�����ᷢչ����������˾��ס��ϳɰ��Ĺ�������ͼ���£�
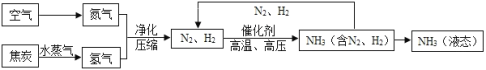
(1)���������ɵİ�(NH3)����ũҵ���Ǻϳ�_________(���������������������ط���)��ԭ�ϡ�
(2)��ȡ�����ķ�Ӧ����Ϊ��C + H2O![]() CO + H2�����з�����ԭ��Ӧ��������_____________��
CO + H2�����з�����ԭ��Ӧ��������_____________��
(3)д��N2��H2��Ӧ����NH3�Ļ�ѧ����ʽ_________________________________��
(4)�������п�ѭ��ʹ�õ�������___________________��
(5)���е㲻ͬ��������뿪����������Һ�����뷨���±��Ǹ����ʵķе㡣
���� | H2 | N2 | O2 | NH3 |
�е� | �C 252�� | �C 195.8�� | �C 183�� | �C 33.35�� |
������¶�t��![]() ʱ���ɽ�������N2��O2���롣Ҫ������NH3��N2��H2���뿪����Ӧ���¶ȿ�����_________(�����)��
ʱ���ɽ�������N2��O2���롣Ҫ������NH3��N2��H2���뿪����Ӧ���¶ȿ�����_________(�����)��
A��![]() B��
B��![]() C��
C��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������������Σ��ǻ�ѧѧ���������߲���ļ�ֵ����һ��ʵ����У�С���ͬѧ��һ��ι���ij������˾����ҶԿ�ʯѡȡ��ұ�������ֵĹ�������(��ͼ)�������ֵ�����ȣ�����ȫ�µ���ʶ��
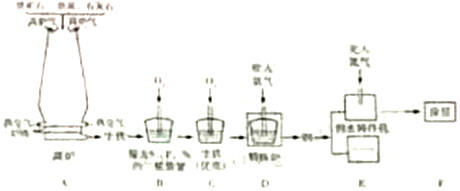
(1)�ó�����ʯұ���ķ�Ӧԭ����_________________________(�û�ѧ����ʽ��ʾ)�� (2)�����������̣�����װ���з�����Ӧ�Ļ�ѧ����ʽ��________________(дһ��)��
(3)����¯�д������ʹ��ˮѭ�����������ɷ־��Ȼ�ϣ��൱�ڻ�ѧʵ����________������(��һ������������)��
(4)�ڸ�ˮ�������У����¸ּӹ��ɸ������ʱ�����뵪����������_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�dz��л�ѧ������ʵ��װ�á���ش��������⣺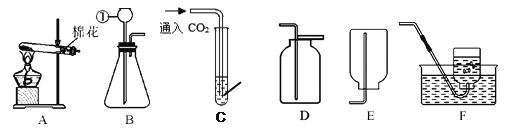
(1)�����ٵ�������_______________��
(2)ʵ�����ø��������ȡ�����Ļ�ѧ����ʽΪ________________���������Ӧ����Ϊ_______��Ӧ�����Թܿڷ�һС������������_________________��
(3)Ҫ�ռ��ϴ�����������Ӧѡ����ռ�װ��Ϊ______(��װ�õ���ĸ��ţ���ͬ)�����ø�װ���ռ��������ж������ռ�����������________________________________��
(4)��Cװ����ͨ�������̼���壬�۲쵽��ɫʯ����Һ��ɺ�ɫ��ԭ���ǣ��û�ѧ����ʽ��ʾ��____________��
(5)ʵ��������ˮ�����ƺͼ�ʯ�����ֹ����ϼ�����ȡ���顣���飨CH4����һ����ɫ��ζ���ܶȱȿ���С��������ˮ�����塣ʵ����Ҫ��ȡ���ռ�����Ӧѡ���װ�������_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ���ý�ͷ�ι���װ�й���Ĺ��ƿ�еμ�Һ�壬ʹ��������ʹ�õĹ����Һ�������:(��д���������)
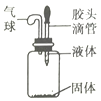
(1)____________�� (2)___________�� (3) ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��С������H2O2��Һ��O2��ʵ��̽����������й��̣��ش��й����⡣
��1��MnO2����������5mL5%��H2O2��Һ�м�������MnO2�����������������ݡ�
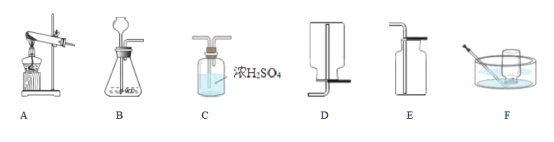
��д����H2O2��Һ�Ʊ�O2�Ļ�ѧ����ʽ��____________________________________��
����������Ӧԭ���Ʊ����ռ�һƿ�����O2��������װ��ͼ��ѡ����װһ��װ�ã�������˳��Ϊ_______�� __________�� ________�����ţ���Ϊ��ȷ��ʵ��ɹ�����װҩƷ֮ǰӦ��_________��
�ۼ���O2�ķ�����___________________________ ����ľ����ȼ����֤���ռ�������ΪO2��
��2��FeCl3��Һ������
��5mL5%��H2O2��Һ�м���2��һ��Ũ�ȵ� FeCl3��Һ�����������������ݡ�
����֪��FeCl3��Һ����Ҫ������������H2O��Fe3+��Cl-
�����⣩��������H2O2��Һ�ķֽ�������ã�
�����裩����һ��������H2O
�������������Fe3+
��������������Cl-
���������ټ���һ�����ܳ�����������__________________________________________��
��ʵ�飩
���� | ���� |
�����������䣬��H2O2��Һ�м���NaCl��Һ | �����Ա仯 |
�����������䣬��H2O2��Һ�м���Na2SO4��Һ | �����Ա仯 |
�����������䣬��H2O2��Һ�м���Fe2(SO4)3��Һ | ���������������� |
�����ۣ��ڼ���___������������һ����һ�ּ��費������
�۴����Ƚϴ�ѭ�����õĽǶȷ�����_____���ѧʽ�����ʺ����÷�Ӧ�Ĵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʽ̼��þ[Mg2(OH)2CO3]������þ(MgO2)������Ҫ����ԭ�ϡ�
(1)����Mg2(OH)2CO3�õ��������������һ�ֳ����������壬����ʹ����ʯ��ˮ����ǡ�����ʱ��Ӧ�Ļ�ѧ����ʽΪ_______��
(2)������ʵ�������ù����м�˫��ˮ��ֽ��裬������ӦMgO + H2O2 == MgO2+ H2O,�¶����ߣ�˵���÷�Ӧ______����(�����ų�������������)��
(3)ʵ�����ڲⶨMgO2����ʱ��Ҫ�õ���������10%��ϡ����110g��������37%��Ũ���������ƣ���Ҫ��ˮ_______g��(����������һλС��)
(4)MgCl2���Ʊ�Mg2(OH)2CO3��ԭ�ϡ����ú�̼��þ84%����þ���Ʊ�MgCl2����Ӧ���£�MgCO3 + Cl2 + CO ==== MgCl2 + 2CO2 (�����ʲ��μӷ�Ӧ)������19��MgCl2��Ҫ��������þ��_________�֣�(д���������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Na2CO3��CaCO3��ɵĻ�����У����ⶨ����̼Ԫ�ص���������Ϊ11.65%�������������������У���NaԪ�ص�������������CaԪ�ص���������������Ԫ�ص�������������CaCO3��������������Na2CO3��������������Na2CO3��CaCO3�������ȣ���ȷ�����ǣ� ��
A��������ȷ�� B��ֻ�Т���ȷ��
C��ֻ�Тܢݢ���ȷ�� D������ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����¡�����Ũ�ȡ��Ӵ�ѹǿ��ʹ�ô������������ѧ��Ӧ���ʡ��ְ�þ��Ͷ��ʢ��ϡ������Թ��У��Թ���起��̡��������������ʱ仯���(v)�ͷ�Ӧ���е�ʱ��(t) �Ĺ�ϵ��ͼ��ʾ��������˵���������(����)
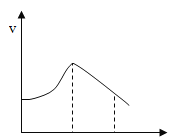
A. ��Ӧ��������Һ��pH������ B. t1��t2���ʱ仯����Ҫԭ���Ƿ�Ӧ������϶�
C. t2��t3���ʱ仯����Ҫԭ���������Ũ����С D. t1��t2���ʱ仯����Ҫԭ���Ƿ�Ӧ����ʹ��Һ�¶�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com